POKRAČUJÍCÍ LÉKAŘSKÉ VZDĚLÁNÍ
ČLÁNEK
Důležité komplikací chronického onemocnění ledvin
van der WaltI; C R SwanepoelII; B MahalaIII; M MeyersIV
Korespondence
ABSTRAKT
komplikace chronického onemocnění ledvin (CKD) jsou dyslipidémie hyperkalémie, metabolická acidóza, anemie a kostní a minerální poruchy. Dyslipidemie může být léčena látkami snižujícími lipoproteiny s nízkou hustotou. Statiny jsou neúčinné ve stádiích 4 a 5 CKD, ale jsou indikovány k prevenci progrese onemocnění v dřívějších stádiích. Nedávno se ukázalo, že chronická acidóza je rizikovým faktorem progrese renální dysfunkce CKD. Proto je léčba povinná. Prakticky by to mělo sestávat z 1-2 hromadných čajových lžiček hydrogenuhličitanu sodného 2-3krát denně, což je levná a bezpečná terapie, která nezvyšuje krevní tlak navzdory zvýšené hladině sodíku. Cílové hladiny hemoglobinu se podle mezinárodních pokynů pohybují mezi 10 g / dL a 12 g/dl. Sérové hladiny fosfátů je zvýšen ve stádiu CKD 4, a to zejména ve stádiu CKD 5, která je spojena s koronární krkavici a jiných cévních kalcifikací a může vyústit v ischemickou chorobou srdeční, infarktu myokardu a mozkové mrtvice. Zvýšená hladina parathormonu (sekundární hyperparatyreóza) je také hlavním rizikovým faktorem kardiovaskulárních onemocnění a je spojena se zvýšenou hypertenzí a rezistencí k léčbě anémie spojené s CKD.
Dyslipidémie
Chronické onemocnění ledvin (CKD) je spojena se změnami v lipoproteinové struktury a funkce, včetně:
- menší high-density lipoprotein cholesterol
- zvýšená intermediate-density lipoprotein
- zvýšená proatherogenic lipidové částice.
Význam dyslipidémie ovládání
- Úspěšné léčbě dyslipidemií je známo, že snížení kardiovaskulárních onemocnění (CVD) riziko a měly by také zpomalit pokles funkce ledvin.
- protože bylo prokázáno, že statiny snižují vylučování bílkovin nebo albuminu močí, doporučují se pro CKD s proteinurií.
- Poznámky k použití statinů ve stupních 3-5 CKD jsou uvedeny v tabulce 1.
- současné užívání statinů a fibrátů zvyšuje riziko rabdomyolýzy.
Cíl pro low-density lipoprotein cholesterol
- Onemocnění Ledvin Výsledky Quality Initiative (KDOQI) pokyny doporučují následující pro terapie dyslipidemií v ČKD: v případech, low-density lipoprotein cholesterolu (LDL-C) <3.5 mmol/L, prvním krokem je změna životního stylu; v případě LDL-C >3,5 mmol/L, terapie by měla být zvažována kromě toho, aby změna životního stylu, včetně stravy terapie, kontrola váhy a cvičení.
- je nezbytné, aby byl LDL-C snížen na <1,8 mmol / L.
KDOQI pokyny pro snížení cholesterolu u pacientů s CKD(2013):
- pacienti ve věku >50 let by měli dostávat statin.
- pacienti ve věku 18-49 let by měli dostat statin, pokud je přítomna jiná komorbidita.
- příjemci transplantace ledvin by měli dostat statin.
léčba hyperkalemie a metabolické acidózy
hyperkalemie
- jak CKD postupuje ve stadiu, jsou pozorovány acidóza a hyperkalemie. Hyperkalémie je definována jako hladina draslíku v séru >5,5 mmol / L. hyperkalémie >7 mmol / L může potenciálně způsobit srdeční zástavu; takové případy by měly být považovány za naléhavé.
- je-li pozorována závažná hyperkalémie, i přes absenci snížené funkce ledvin, je třeba zvážit pseudohyperkalemii, artefakt způsobený hemolýzou vzorku krve.
- hyperkalemie je rizikovým faktorem arytmií. V případě těžké hyperkalemie by nouzové hladiny měly být potvrzeny abnormalitami EKG, jako je stanování t-vln, prodloužení PQ-krát, následované vymizením P-vlny a rozšířením komplexu QRS. Pacienti s život ohrožujícími nálezy EKG, bradykardií a hypotenzí by měli být léčeni okamžitě a následnou léčbou ve spojení s nefrologem.
- Droga-přiměl hyperkalémie v CKD je většinou způsobená renin-angiotenzin-aldosteron inhibitory, jako jsou ACE inhibitory, blokátory receptorů angiotensinu II (o arb) a spironolakton nebo nadměrný příjem draslíku-obsahující potraviny. Mezi další příčiny patří podávání β-blokátorů, digoxinu, nesteroidních protizánětlivých léků (NSAID), trimethoprimu nebo pentamidinu.
- CKD způsobená diabetickou nefropatií může být spojena s hyporeninemickým hypoaldosteronismem, který může způsobit hyperkalemii navzdory relativně dobře zachované funkci ledvin. Toto je známé jako renální tubulární acidóza typu IV.
nouzová léčba
- prvním krokem je stabilizace myokardu. Intravenózní podání glukonátu vápenatého nemění draslík v plazmě, ale přechodně zlepšuje EKG. Podávání glukonátu vápenatého 20 mL intravenózně po dobu 1 minuty se může opakovat, pokud nedojde ke zlepšení EKG během 3-5 minut.
- druhým krokem je přesun draslíku z extracelulárního do intracelulárního prostoru, aby se pokusili rychle snižovat sérové hladiny draslíku. To lze provést třemi různými způsoby:
- intravenózní inzulín v kombinaci s glukózou. Spravovat 10 U krátkodobě působící inzulin v kombinaci s 50 mL 50% glukózy jako bolus, následovaný intravenózní infuze 5% glukózy, aby se zabránilo hypoglykémii.
- β2-agonista. Podávejte 20 mg salbutamolu, β2-agonisty, inhalací po dobu 10 minut, s nástupem účinku přibližně 30 minut. (To se obvykle nevyžaduje.)
- hydrogenuhličitan sodný u pacientů s chronickým onemocněním ledvin, kteří ještě nejsou na dialýze. Podávání bikarbonátu může snížit hladinu draslíku v séru zvýšením vylučování draslíku ledvinami. Účinek je velmi pomalý a není použití v akutní situaci, pokud má pacient závažné metabolické acidózy, která potřebuje hydrogenuhličitan léčby.
- jakmile byla provedena předchozí dočasná opatření, provádějí se další intervence k odstranění draslíku z těla.
- kličková diuretika jsou úspěšná pouze u pacientů s adekvátní funkcí ledvin.
- pryskyřičný výměník polystyrenu sodného (kexelát) odstraňuje draslík z krve do střeva výměnou za stejné množství sodíku. Pomalu působí a plazmatický draslík začne klesat pouze během 1-2 hodin. Může být podáván perorálně nebo jako retenční klystýr. Uvedené množství se pohybuje od 30 g do 60 g. To se může opakovat, ale má tendenci způsobovat zácpu.
- hemodialýza je volbou léčby u pacientů s pokročilým chronickým onemocněním ledvin a těžkou hyperkalemií.
prevence
- dietní poradenství v oblasti omezení draslíku.
- Vyhněte se lékům, které interferují s renálním vylučováním draslíku, např. draslík šetřící diuretika, NSAID, ACE inhibitory, ARB.
- Vyhněte se lékům, které interferují s posuny draslíku z intracelulárního do extracelulárního kompartmentu, např.
- u vybraných pacientů s dostatečnou zbytkovou funkcí ledvin může být ke stimulaci vylučování draslíku močí použita léčba kličkovým diuretikem.
Metabolická acidóza
Metabolická acidóza je charakterizována:
- nízký arteriální krev pH (acidémií) (<7.35)
- snížené sérové HCO3 – koncentrace
- snížení pCO2 (respirační kompenzaci).
systémové účinky
metabolická acidóza může vést k různým změnám v tkáních a orgánech, např.:
- kardiovaskulární změny, například tachykardie, bradykardie, hypotenze a srdeční selhání
- život ohrožující hyperkalémie
- nevolnost, zvracení a bolest břicha
- zmatenost, deprese centrálního nervového systému.
přidružené příznaky a příznaky budou záviset na rychlosti a velikosti poklesu pH a základní patologie.
uremická acidóza
metabolická acidóza se vyskytuje při selhání ledvin v důsledku snížené schopnosti vylučovat H+ nebo neschopnosti produkovat amoniak.
v časných stádiích CKD (GFR <40 mL / min) se může projevit metabolická acidóza s normální aniontovou mezerou (AG). S progresí CKD (GFR <20 mL/min) může dojít k metabolické acidóze s vysokým AG.
u pokročilého CKD je zvýšená AG typická díky přítomnosti zadržených kyselin, jako jsou sírany, fosfáty, urát a hippurát.
principy léčby
pacienti s metabolickou acidózou jsou často velmi nemocní a jejich stav má tendenci se rychle zhoršovat.
rutinní podávání hydrogenuhličitanu sodného je kontroverzní, i když je třeba provést nápravu těžké acidózy.
možné komplikace při podávání hydrogenuhličitanu sodného zahrnují objemové přetížení, zejména u pacientů s poruchou funkce ledvin nebo srdce, hypernatrémii, hypokalémii, hypokalcémii a alkalózu.
požadované množství hydrogenuhličitanu (mmol) lze odhadnout následovně:
Cílová plazmatická HCO3 – (mmol/L) – aktuální plazmatická HCO3 – (mmol/L) x 40% tělesné hmotnosti (kg).
anémie u CKD
anémie je nejčastější komplikací CKD a je spojena s výrazně sníženou kvalitou života. Úspěšná léčba anémie u onemocnění ledvin může snížit pokles funkce ledvin. Cílové hladiny hemoglobinu jsou 10-12 g / dL při léčbě anémie u CKD. Léčba je nákladná, a proto je racionální zvážení povinné.
renální anémie
renální anémie je typicky normochromní normocytární. Je způsobena hlavně zhoršenou produkcí erytropoetinu ledvinami a částečně uremickými toxiny. Další příčiny, které mohou hrát roli v CKD, zejména u dialyzovaných pacientů, jsou:
- erytropoetin odpor (nejvýznamnější)
- kostní dřeň toxinů (žádný byl izolován zatím)
- fibróza kostní dřeně, sekundární hyperparatyreózy
- probíhající zánětlivé procesy, např. neléčená infekce
- haematinic nedostatek (železa, kyseliny listové a vitaminu B12)
- zvýšená červených krvinek ničení
- abnormální červené buněčné membrány, což způsobuje zvýšené osmotické křehkosti
- zvýšená ztráta krve z okultní gastrointestinální krvácení a odběr vzorků krve a během hemodialýzy
- ACE inhibice.
Erytropoetin je glykoproteinový hormon, který stimuluje produkci červených krvinek vazbou na receptory pro erytropoetin, který se nachází na raných erytroidních progenitorových buňkách v kostní dřeni.
vazba erytropoetinu na tyto progenitorové buňky je chrání před apoptózou, a proto umožňuje dělení a zrání buněk na červené krvinky. U CKD mohou být hladiny erytropoetinu normální, ale nedostatečné pro stupeň anémie. Mechanismy narušující tvorbu erytropoetinu u nemocných ledvin zůstávají špatně pochopeny. Inhibice erytropoézy uremickými inhibitory je také možná a může významně přispívat k anémii CKD; tyto faktory nebyly identifikovány. Dialýza může zlepšit renální anémii a účinnost přípravků stimulujících erytropoetin. U pacientů s onemocněním ledvin se mohou vyvinout chronické infekce a jiná chronická onemocnění. Chronické onemocnění přispívá v takových případech k anémii. Anémie chronického onemocnění je zprostředkována zánětlivými cytokiny prostřednictvím inhibice tvorby a účinnosti erytropoetinu a snížené dostupnosti železa.
Hepcidin je klíčovým mediátorem metabolismu železa. Při zánětlivých stavech hepcidin blokuje vstřebávání železa ve střevě a podporuje sekvestraci železa v makrofágech.
jiné příčiny
anémie spojená s chronickým onemocněním ledvin je s největší pravděpodobností renální anémie; rozdíl u jiných nemocí však musí být považován za pravdivý pro stupně 1-3 CKD.
hodnocení anémie u CKD pacientů by mělo obsahovat kompletní krevní obraz s červených krvinek indexy (průměrná korpuskulární koncentrace hemoglobinu, středního objemu erytrocytů). Renální anémie je obvykle normochromní a normocytární. Nedostatek vitaminu B12 a kyseliny listové může vést k makrocytóze, zatímco nedostatek železa nebo dědičné poruchy hemoglobinu mohou vyvolat mikrocytózu. Měly by být provedeny studie železa, aby se vyhodnotila hladina železa v tkáňových zásobách nebo přiměřenost zásobování železem pro erytropoézu.
anémie může znamenat výskyt podvýživy nebo systémového onemocnění. Je nezávislým rizikovým faktorem pro hospitalizaci, CVD a úmrtnost. ACE inhibitory mohou zhoršit anémii.
Léčba anémie chrání srdce
anémie zhoršuje srdeční selhání. Léčba anémie je prospěšná pro střední délku života a může také zlepšit prognózu CVD. U pacientů s hladinou hemoglobinu v cílovém rozmezí se zlepšuje kvalita života.
Cílové úrovně hemoglobinu
Onemocnění Ledvin Zlepšení Globální Výsledek (KDIGO) pokyny uvádějí, že hladina hemoglobinu v rozmezí od 10,0 g/dL až 12 g/dL u CKD pacientů na dialýze. Hladiny před dialýzou by měly být 10 g / dl.
sdílení rolí mezi nefrology a lékaři primární péče
doporučuje se včasné doporučení nefrologovi. Po rozhodnutí o strategii léčby pokračují nefrologové a lékaři primární péče v řízení ve spolupráci.
hodnocení nedostatku železa
vyhodnocení deficitu železa a správného přísunu železa je důležité při léčbě anémie. Anémie se může zlepšit podáváním doplňků železa, i když pacient zjevně nemá nedostatek železa, protože použití rekombinantního erytropoetinu může způsobit relativní nedostatek železa.
pokyny KDOQI pro rekombinantní lidský erytropoetin u CKD jsou:
- sérový feritin >100 ng / mL před dialýzou
- sérový feritin >200 ng / mL u dialyzovaných pacientů
- saturace transferinu >20%.
železo může být podáváno buď intravenózně nebo perorálně. Intravenózní železo je účinnější, zejména u dialyzovaných pacientů a pacientů léčených erytropoetinem.
Použití exogenního erytropoetinů
v současné době Existuje řada erytropoetin stimulující přípravky jsou k dispozici, včetně starší, kratší působící léky a nové, déle působící ty. Vhodné činidlo a dávka závisí na řadě faktorů, včetně nákladů, účinnosti a pohodlí. Protože tyto léky jsou drahé a mají vedlejší účinky, jejich řízení je nejlepší ponechat na nefrologovi.
poruchy kostí a minerálů
hyperfosfatemie je klíčovou abnormalitou, která spouští kaskádu metabolických příhod, což má za následek kostní minerální hustotu CKD.
fosfát se zachovává, protože se zhoršuje funkce ledvin-podobně jako kreatinin. Tato retence je zřejmá, jakmile je dosaženo stupně 3b CKD. Postupně se bude zhoršovat, jak se blíží konečná fáze, a musí být snížena na normální limity.
vysoce fosfátová strava stimuluje osteocyty k produkci fibroblastového růstového faktoru 23, který zase inhibuje hydroxylaci vitaminu D na aktivní 1,25 vitamín D3. Bez vitaminu D3 se snižuje absorpce vápníku a remodelace kostí. Výsledná hypokalcemie je hlavním stimulem pro uvolňování parathormonu (PTH)s následným rozvojem onemocnění ledvin. Sérová alkalická fosfatáza je markerem zvýšeného kostního obratu. Proto vysoké hladiny v krvi vykazují aktivitu PTH.
je třeba poznamenat, že jak hyperfosfatemie, tak nedostatek vitaminu D3 vedou ke zvýšené sekreci PTH.
zpočátku může být stimul pro sekreci PTH kontrolován zvýšením sérového vápníku, snížením hladin fosfátů v krvi a předepisováním vitaminu D3. Toto je sekundární hyperparatyreóza (Tabulka 2). Nicméně, s časem a nekontrolované, dlouhodobé stimulace sekrece PTH, hormony příštítných staňte autonomní a fázi autonomní hyperparatyreózy je dosaženo (Tabulka 3). Paratyroidektomie může být nyní nezbytná nebo musí být podána drahá kalcimimetika, aby se pokusilo Obnovit neuspořádané metabolické prostředí.


existuje nejistota ohledně interpretace měření hladiny vitaminu D3. Pokud mají být měřeny, doporučuje se pro posouzení hladiny 25-OH-vitaminu D3.
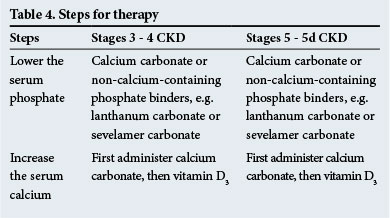
terapie
kroky léčby jsou uvedeny v tabulce 4. Non-vápník-obsahující fosfáty jsou doporučovány, když tam je významný metastatické kalcifikace a/nebo při hyperkalcémii je přítomen.
Calcimimetics, který vnímavost příštítných tělísek sérového vápníku, jsou užitečné předepsat v hyperparatyreózy, kdy sérové hladiny PTH jsou vysoké (2 – 9 krát vyšší, než je normální rozmezí – podívejte se s laboratoří pro normální rozmezí). Hrají roli při snižování hladin PTH v jakékoli klinické situaci, ke které dochází u CKD.
následná měření krve
jsou uvedena v tabulce 5.
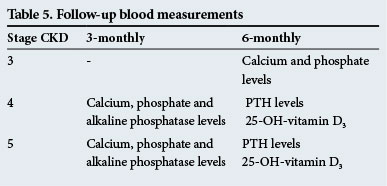
Tyto navazující časy jsou pouze orientační a testy by měly být prováděny častěji, pokud existují významné odchylky.
zvláštní poznámky
- zahrnují nefrologa brzy v průběhu CKD.
- Vyhněte se nadměrnému potlačení příštítných tělísek, protože to povede k dynamickému onemocnění kostí.
- přesná úroveň PTH, na které je diagnostikována sekundární a autonomní hyperparatyreóza, je nejistá kvůli různým testům. Biochemie, jak je uvedeno výše (spolu s rentgenovými snímky kostí), musí být použita k pomoci při diagnostice.
- buďte si vědomi trendů hladin alkalické fosfatázy v séru; hladina může být v normálním rozmezí, ale může se zdvojnásobit oproti předchozímu čtení.
- osteoporóza doprovází onemocnění kostí, které se vyskytuje u CKD. Bisfosfonáty se nesmí používat ve stádiích 3-5 pacientů s chronickým renálním onemocněním.