jatkuva lääketieteellinen koulutus
artikkeli
kroonisen munuaissairauden tärkeitä komplikaatioita
i van der WaltI; CR SwanepoelII; B MahalaIII; A M MeyersIV
kirjeenvaihto
Abstrakti
kroonisen munuaissairauden komplikaatioita ovat dyslipidemia hyperkalemia, metabolinen asidoosi, anemia sekä luuston ja mineraalien häiriöt. Dyslipidemiaa voidaan hoitaa pienitiheyksisillä lipoproteiineja alentavilla lääkkeillä. Statiinit ovat tehottomia CKD: n vaiheissa 4 ja 5, mutta ne on tarkoitettu taudin etenemisen estämiseen varhaisemmissa vaiheissa. Kroonisen asidoosin on viime aikoina osoitettu olevan riskitekijä CKD: n munuaisten vajaatoiminnan etenemisessä. Siksi hoito on pakollista. Käytännössä tämän pitäisi koostua 1 – 2 kasatusta teelusikallista natriumbikarbonaattia 2-3 kertaa päivässä, mikä on edullinen ja turvallinen hoito, joka ei nosta verenpainetta huolimatta lisääntyneestä natriumpitoisuudesta. Hemoglobiinin tavoitetaso on kansainvälisten ohjeiden mukaan 10-12 g/dL. Seerumin fosfaattipitoisuus nousee vaiheessa 4 ja erityisesti vaiheessa 5, joka liittyy sepelvaltimon kaulavaltimoon ja muihin verisuonten kalkkeutumiin ja voi johtaa iskeemiseen sydänsairauteen, sydäninfarktiin ja aivohalvaukseen. Lisäkilpirauhashormonitason nousu (sekundaarinen lisäkilpirauhasten liikatoiminta) on myös merkittävä sydän-ja verisuonitautien riskitekijä, ja siihen liittyy kohonnut verenpaine ja vastustuskyky kroonista munuaistautia sairastavan anemian hoidossa.
dyslipidemia
krooniseen munuaissairauteen liittyy lipoproteiinin rakenteen ja toiminnan muutoksia, mm.:
- pienentynyt suuritiheyksinen lipoproteiinikolesteroli
- lisääntynyt välitiheyksinen lipoproteiini
- lisääntynyt proatherogeeniset lipidihiukkaset.
Dyslipidemiakontrollin merkitys
- dyslipidemian onnistuneen hoidon tiedetään alentavan sydän-ja verisuonitautien (CVD) riskiä ja hidastavan myös munuaisten toiminnan heikkenemistä.
- koska statiinien on osoitettu vähentävän proteiinin tai albumiinin erittymistä virtsaan, niitä suositellaan kroonista munuaistautia sairastaville potilaille, joilla on proteinuria.
- statiinin käyttöä vaiheissa 3 – 5 kroonista munuaistautia koskevat huomautukset on esitetty taulukossa 1.
- statiinien ja fibraattien samanaikainen käyttö lisää rabdomyolyysin riskiä.
LD-density-lipoproteiinikolesterolin tavoitearvo
- munuaissairauden tulokset Quality Initiative (KDOQI)-ohjeissa suositellaan seuraavaa dyslipidemian hoidossa kroonista munuaistautia sairastavilla potilailla: LDL-kolesterolin (LDL-kolesterolin) <3 tapauksessa.Jos LDL-kolesteroli on >3, 5 mmol/L, lääkitystä tulee harkita elämäntapamuutoksen lisäksi, mukaan lukien ruokavaliohoito, painonhallinta ja liikunta.
- LDL-kolesterolin alentaminen tasolle <1, 8 mmol/l on tärkeää
KDOQI-ohjeet kroonista munuaistautia sairastavien potilaiden kolesteroliarvojen alentamiseksi (2013):
- alle 753>50-vuotiaille potilaille tulee antaa statiinia.
- 18 – 49-vuotiaille potilaille tulee antaa statiinia, jos potilaalla esiintyy muuta oheissairautta.
- Munuaisensiirtopotilaille tulee antaa statiinia.
hyperkalemian ja metabolisen asidoosin hoito
hyperkalemia
- kroonista munuaistautia sairastavan potilaan edetessä vaiheittain havaitaan asidoosia ja hyperkalemiaa. Hyperkalemia määritellään seerumin kaliumtasoksi >5, 5 mmol/L. hyperkalemia >7 mmol/L voi mahdollisesti aiheuttaa sydänpysähdyksen; tällaisia tapauksia tulee hoitaa hätätapauksina.
- jos vaikeaa hyperkalemiaa havaitaan munuaisten vajaatoiminnasta huolimatta, tulee harkita pseudohyperkalemiaa, joka on verinäytteen hemolyysistä johtuva artefakti.
- hyperkalemia on rytmihäiriöiden riskitekijä. Jos potilaalla on vaikea hyperkalemia, hätätaso tulee varmistaa EKG-poikkeavuuksilla, kuten T-aaltojen nousulla, PQ-aikojen pidentymisellä, jota seuraa P-aallon häviäminen ja QRS-kompleksin laajeneminen. Potilaat, joilla on hengenvaarallisia EKG-löydöksiä, bradykardiaa ja hypotensiota, on hoidettava viipymättä, minkä jälkeen heidät on hoidettava yhdessä nefrologin kanssa.
- lääkkeen aiheuttama hyperkalemia kroonista munuaistautia sairastavissa oireyhtymissä johtuu useimmiten reniini-angiotensiini-aldosteronin estäjistä, kuten ACE: n estäjistä, angiotensiini II-reseptorin salpaajista (ARBs) ja spironolaktonista tai liiallisesta kaliumia sisältävien ruokien nauttimisesta. Muita syitä ovat β-salpaajien, digoksiinin, steroideihin kuulumattomien tulehduskipulääkkeiden (NSAID), trimetopriimin tai pentamidiinin antaminen.
- diabeettisen nefropatian aiheuttamaan kroonista munuaistautia sairastavaan oireyhtymään voi liittyä hyporeniineemistä hypoaldosteronismia, joka saattaa aiheuttaa hyperkalemiaa suhteellisen hyvin säilyneestä munuaistoiminnasta huolimatta. Tätä kutsutaan tyypin IV munuaistubulusten asidoosiksi.
Ensihoito
- ensimmäinen vaihe on sydänlihaksen vakauttaminen. Laskimoon annettu kalsiumglukonaatti ei muuta plasman kaliumia, mutta parantaa ohimenevästi EKG: tä. Kalsiumglukonaatin 20 mL: n antaminen laskimoon 1 minuutin aikana voidaan toistaa, jos EKG ei parane 3 – 5 minuutin kuluessa.
- toinen vaihe on siirtää kalium solunulkoisesta solunsisäiseen osastoon, jotta seerumin kaliumpitoisuus voidaan laskea nopeasti. Tämä voidaan tehdä kolmella eri tavalla:
- laskimoon annettava insuliini yhdistettynä glukoosiin. Annetaan 10 U lyhytvaikutteista insuliinia yhdistettynä 50 mL: aan 50% dekstroosia boluksena, minkä jälkeen annetaan 5% dekstroosia laskimonsisäisenä infuusiona hypoglykemian estämiseksi.
- β2-agonisti. Anna 20 mg salbutamolia, β2-agonistia, hengitettynä 10 minuutin aikana ja vaikutus alkaa noin 30 minuuttia. (Tätä ei yleensä tarvita.)
- natriumbikarbonaatti kroonista munuaistautia sairastavilla potilailla, jotka eivät vielä ole dialyysihoidossa. Bikarbonaatin anto voi alentaa seerumin kaliumpitoisuutta tehostamalla kaliumin erittymistä munuaisten kautta. Vaikutus on hyvin hidas, eikä sitä voida käyttää akuutissa tilanteessa, ellei potilaalla ole vaikeaa metabolista asidoosia, joka tarvitsee bikarbonaattihoitoa.
- kun aiemmat väliaikaiset toimenpiteet on suoritettu, ryhdytään lisätoimenpiteisiin kaliumin poistamiseksi elimistöstä.
- Loop-diureetit tehoavat vain potilailla, joilla on riittävä munuaistoiminta.
- hartsinvaihdin natriumpolystyreenisulfonaatti (Käkelaatti) poistaa kaliumia verestä suoleen vastineeksi yhtä suuresta määrästä natriumia. Se on hidasvaikutteinen ja plasman kaliumpitoisuus alkaa laskea vasta 1 – 2 tunnin kuluessa. Se voidaan antaa suun kautta tai retentio peräruiskeena. Annettu määrä vaihtelee 30 grammasta 60 grammaan. Tämä voi toistua, mutta yleensä aiheuttaa ummetusta.
- hemodialyysi on valinta potilaille, joilla on pitkälle edennyt kroonista munuaistautia ja vaikea hyperkalemia.
ehkäisy
- ravintoneuvonta kaliumrajoituksesta.
- Vältä lääkkeitä, jotka vaikuttavat kaliumin erittymiseen munuaisten kautta, esim.kaliumia säästävät diureetit, tulehduskipulääkkeet, ACE: n estäjät, ARBs.
- Vältä lääkkeitä, jotka häiritsevät kaliumin siirtymistä solunsisäisestä lokeroon, esim.epäselektiivisiä β-salpaajia.
- valituilla potilailla, joilla on riittävästi jäljellä munuaistoimintaa, voidaan käyttää loop-diureettihoitoa kaliumin erittymisen stimuloimiseksi virtsaan.
metabolinen asidoosi
metaboliselle asidoosille on ominaista:
- Alhainen valtimoveren pH (asidemia) (<7.35)
- alentunut seerumin HCO3-pitoisuus
- laski pCO2: ta (hengityskompensaatiosta).
Systeemiset vaikutukset
metabolinen asidoosi voi aiheuttaa erilaisia muutoksia kudoksissa ja elimissä, esim.:
- kardiovaskulaariset muutokset, kuten takykardia, bradykardia, hypotensio ja sydämen vajaatoiminta
- hengenvaarallinen hyperkalemia
- pahoinvointi, oksentelu ja vatsakipu
- sekavuus, johon liittyy keskushermoston lamaantuminen.
siihen liittyvät oireet ja merkit riippuvat pH: n laskun nopeudesta ja suuruudesta sekä taustalla olevasta patologiasta.
ureeminen asidoosi
metabolinen asidoosi esiintyy munuaisten vajaatoiminnassa johtuen heikentyneestä kyvystä erittää H+ tai kyvyttömyydestä tuottaa ammoniakkia.
CKD: n alkuvaiheessa (GFR <40 mL/min) saattaa ilmetä metabolinen asidoosi, johon liittyy normaali anionivaje (AG). CKD: n edetessä (GFR <20 mL/min) seurauksena voi olla korkea AG-metabolinen asidoosi.
pitkälle edenneessä KREATIINIKINAASIASSA AG: n nousu on tyypillistä, koska siinä on jäljellä happoja, kuten sulfaatteja, fosfaatteja, uraattia ja hippuraattia.
hoitoperiaatteet
metabolista asidoosia sairastavat potilaat ovat usein hyvin sairaita ja heidän tilansa huononee yleensä nopeasti.
natriumbikarbonaatin rutiiniannostus on kiistanalainen, vaikka se on tehtävä vaikean asidoosin korjaamiseksi.
natriumbikarbonaatin antoon liittyviä mahdollisia komplikaatioita ovat volyymin liikakuormitus erityisesti potilailla, joilla on munuaisten tai sydämen vajaatoiminta, hypernatremia, hypokalemia, hypokalsemia ja alkaloosi.
tarvittavan bikarbonaatin määrä (mmol) voidaan arvioida seuraavasti:
tavoiteplasma HCO3- (mmol/l) – nykyinen plasman HCO3- (mmol/l) x 40% kehon painosta (kg).
anemia kroonista munuaistautia sairastavilla potilailla
anemia on kroonista munuaistautia sairastavien potilaiden yleisin komplikaatio, ja siihen liittyy huomattavasti heikentynyt elämänlaatu. Munuaissairauden anemian onnistunut hoito saattaa vähentää munuaisten toiminnan heikkenemistä. Kroonista munuaistautia sairastavan anemian hoidossa hemoglobiiniarvon tavoitetaso on 10-12 g / dL. Hoito on kallista ja siksi järkevä harkinta on pakollista.
Renaalinen anemia
Renaalinen anemia on tyypillisesti normokromaattinen normosyyttinen. Se johtuu pääasiassa munuaisten heikentyneestä erytropoietiinituotannosta ja osittain ureemisista toksiineista. Muita syitä, joilla voi olla merkitystä kroonista munuaistautia sairastaville potilaille, ovat:
- erytropoietiiniresistenssi (merkittävin)
- luuydinmyrkyt (yhtäkään ei ole vielä eristetty)
- luuydinfibroosi, sekundaarista lisäkilpirauhasten liikatoimintaan
- jatkuvaa tulehdusprosessia, esim. hoitamattomat infektiot
- hematiinipuutos (raudan, folaatin ja B12-vitamiinin puute)
- lisääntynyt punasolujen tuhoutuminen
- epänormaalit punasolukalvot aiheuttaen lisääntynyttä osmoottista haurautta
- lisääntynyttä verenhukkaa piilevästä ruoansulatuskanavan verenvuodosta ja verinäytteiden ottamisesta sekä hemodialyysin aikana
- ACE: n esto.
erytropoietiini on glykoproteiinihormoni, joka stimuloi punasolujen tuotantoa sitoutumalla erytropoietiinireseptoreihin, jotka sijaitsevat luuytimen varhaisissa punasolujen kantasoluissa.
erytropoietiinin sitoutuminen näihin kantasoluihin säästää ne apoptoosilta ja mahdollistaa siten solujen jakautumisen ja kypsymisen punasoluiksi. Kroonista munuaistautia sairastavien erytropoietiinitasot voivat olla normaalit, mutta riittämättömät anemian asteeseen. Erytropoietiinin tuotantoa heikentävät mekanismit sairaissa munuaisissa tunnetaan huonosti. Myös ureemisten inhibiittorien aikaansaama erytropoieesin inhibitio on mahdollista ja se saattaa myötävaikuttaa merkittävästi kroonista munuaistautia koskevaan anemiaan; näitä tekijöitä ei ole tunnistettu. Dialyysi voi parantaa renaalista anemiaa ja erytropoietiinia stimuloivien aineiden tehoa. Potilaille, joilla on munuaissairaus, voi kehittyä kroonisia infektioita ja muita kroonisia sairauksia. Krooninen sairaus edistää tällaisissa tapauksissa anemiaa. Kroonisen sairauden anemia välittyy tulehduksellisista sytokiineista erytropoietiinin tuotannon ja tehon estymisen sekä raudan saatavuuden heikkenemisen kautta.
Hepsidiini on raudan aineenvaihdunnan keskeinen välittäjä. Tulehdustiloissa hepsidiini estää raudan imeytymistä suolistossa ja edistää raudan sitomista makrofageihin.
muita syitä
kroonista munuaistautia sairastava anemia on todennäköisin; ero muihin sairauksiin on kuitenkin pidettävä paikkansa vaiheissa 1-3 CKD.
kroonista munuaistautia sairastavien potilaiden anemian arvioinnissa tulee ottaa huomioon täydellinen verenkuva punasoluindekseineen (keskimääräinen hemoglobiinipitoisuus, keskimääräinen tilavuus). Renaalinen anemia on yleensä normokromaattinen ja normosyyttinen. B12-vitamiinin ja folaatin puutos voi johtaa makrosytoosiin, kun taas raudanpuute tai perityt hemoglobiinihäiriöt voivat tuottaa mikrosytoosia. Rautakokeilla tulee arvioida kudosvarastojen rautapitoisuutta tai raudansaannin riittävyyttä erytropoieesiin.
anemia saattaa viitata aliravitsemukseen tai systeemiseen sairauteen. Se on itsenäinen sairaalahoidon, CVD: n ja kuolleisuuden riskitekijä. ACE: n estäjät voivat pahentaa anemiaa.
anemian hoito suojaa sydäntä
anemia pahentaa sydämen vajaatoimintaa. Anemian hoito edistää elinajanodotetta ja voi myös parantaa CVD: n ennustetta. Elämänlaatu paranee niillä, joiden hemoglobiinitaso on tavoitealueella.Kroonista munuaistautia sairastavilla dialyysipotilailla
hemoglobiinin tavoitetaso
munuaissairaus parantamassa maailmanlaajuista hoitotulosta (Kdigo) koskevien ohjeiden mukaan hemoglobiinitason tulisi olla 10, 0 g/dL-12 g/dL. Pre dialyysihoitoa edeltävän tason tulee olla 10 g/dL.
roolien jakaminen nefrologien ja perusterveydenhuollon lääkäreiden kesken
nefrologin varhainen lähettäminen on suositeltavaa. Kun hoitostrategia on päätetty, nefrologit ja perusterveydenhuollon lääkärit jatkavat hoitoa yhteistyössä.
raudanpuutteen arviointi
raudanpuutteen ja oikean raudansaannin arviointi on tärkeää anemian hoidossa. Koska yhdistelmä-DNA tekniikalla valmistetun erytropoietiinin käyttö voi aiheuttaa suhteellista raudanpuutetta, rautalisän antaminen saattaa parantaa anemiaa silloinkin, kun potilaalla ei ilmeisesti ole raudanpuutosta.
rekombinantin ihmisen erytropoietiinin kdoqi-ohjeet kroonista munuaistautia sairastaville potilaille ovat::
- seerumin ferritiini >100 ng/mL ennen dialyysihoitoa
- seerumin ferritiini >200 ng/mL dialyysipotilailla
- transferriinin saturaatio >20%.
rautaa voidaan antaa joko laskimoon tai suun kautta. Laskimoon annettu rauta on tehokkaampaa erityisesti dialyysipotilailla ja erytropoietiinihoitoa saavilla potilailla.
eksogeenisten erytropoietiinien käyttö
tällä hetkellä on saatavilla useita erytropoietiinia stimuloivia aineita, mukaan lukien vanhemmat, lyhytvaikutteisemmat ja uudet, pitempivaikutteiset lääkkeet. Sopiva aine ja annos riippuvat useista tekijöistä, kuten kustannuksista, tehokkuudesta ja mukavuudesta. Koska nämä lääkkeet ovat kalliita ja niillä on sivuvaikutuksia, niiden hallinta on parasta jättää nefrologille.
luuston ja mineraalien häiriöt
hyperfosfatemia on keskeinen poikkeavuus, joka käynnistää metabolisten tapahtumien sarjan ja johtaa luun mineraalitiheyteen.
fosfaatti säilyy munuaisten toiminnan heikentyessä-paljolti samalla tavalla kuin kreatiniinikin. Tämä säilyttäminen on ilmeistä vaiheessa 3b CKD on saavutettu. Se pahenee asteittain loppuvaiheen lähestyessä, ja se on laskettava normaaleihin rajoihin.
runsas fosfaattidieetti stimuloi osteosyyttejä tuottamaan fibroblastikasvutekijä 23: A, joka puolestaan estää D-vitamiinin hydroksyloitumista aktiiviseksi 1, 25 D3-vitamiiniksi. Ilman D3-vitamiinia kalsiumin imeytyminen ja luun uudelleenmuodostus heikkenevät. Tästä aiheutuva hypokalsemia on merkittävä lisäkilpirauhashormonin (PTH) vapautumista kiihdyttävä tekijä, ja sitä kautta kehittyy munuaistauti. Seerumin alkalinen fosfataasi on luun liikevaihdon lisääntymisen merkkiaine. Siksi korkea veren pitoisuus osoittaa PTH-aktiivisuutta.
sekä hyperfosfatemia että D3-vitamiinin puutos lisäävät PTH: n eritystä.
PTH: n eritystä stimuloiva vaikutus voidaan aluksi saada hallintaan lisäämällä seerumin kalsiumpitoisuutta, vähentämällä veren fosfaattipitoisuutta ja määräämällä D3-vitamiinia. Tämä on sekundaarinen lisäkilpirauhasten liikatoiminnan vaihe (Taulukko 2). Kuitenkin ajan ja kontrolloimattoman, pitkäaikaisen PTH: n erityksen stimulaation myötä lisäkilpirauhashormoneista tulee autonomisia ja autonomisen hyperparatyreoosin vaihe saavutetaan (Taulukko 3). Lisäkilpirauhasen poisto voi nyt olla tarpeen tai kalliita kalsimimeettisiä lääkkeitä on annettava, jotta häiriintynyt metabolinen ympäristö voidaan palauttaa.


D3-vitamiinitason mittausten tulkintaan liittyy epävarmuutta. Jos ne on mitattava, 25-OH-D3-vitamiinitasoja suositellaan arvioitavaksi.
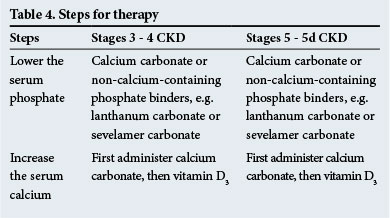
hoito
hoidon vaiheet on esitetty taulukossa 4. Ei-kalsiumia sisältäviä fosfaatinsitojia suositellaan silloin, kun esiintyy merkittävää metastasoitunutta kalkkeutumista ja/tai kun esiintyy hyperkalsemiaa.
Lisäkilpirauhasia seerumin kalsiumpitoisuudelle herkistäviä Kalsimimeetteja on hyödyllistä määrätä lisäkilpirauhasten liikatoiminnassa, kun seerumin PTH – pitoisuus on korkea (2 – 9 kertaa yli normaalin vaihteluvälin-tarkista laboratoriosta normaalit vaihteluvälit). Niillä on rooli PTH: n vähenemisessä kaikissa kliinisissä tilanteissa, joita esiintyy CKD: ssä.
veren seurantamittaukset
nämä on esitetty taulukossa 5.
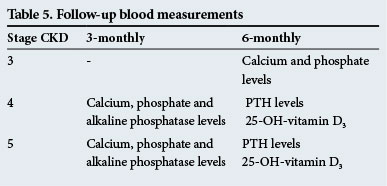
nämä seuranta-ajat ovat vain ohjeita, ja testit on tehtävä useammin, jos niissä on merkittäviä poikkeavuuksia.
erityismaininta
- liittyy NEFROLOGIIN CKD: n alkuvaiheessa.
- lisäkilpirauhasten liiallista suppressiota tulee välttää, sillä se johtaa dynaamiseen luusairauteen.
- tarkka PTH-taso, jolla sekundaarinen ja autonominen lisäkilpirauhasen liikatoiminta diagnosoidaan, on epävarmaa vaihtelevien määritysten vuoksi. Edellä kuvattua biokemiaa (yhdessä luiden röntgenkuvien kanssa) on sitten käytettävä diagnoosin apuna.
- ole tietoinen seerumin alkalisen fosfataasin pitoisuuksien suuntauksista; pitoisuus voi olla normaalitasolla, mutta se voi olla kaksinkertaistunut edellisestä lukemasta.
- osteoporoosiin liittyy kroonista munuaistautia sairastava luustosairaus. Bisfosfonaatteja ei saa käyttää kroonista munuaistautia sairastavien potilaiden vaiheissa 3 – 5.