FORTSATT MEDISINSK UTDANNING
ARTIKKEL
Viktige komplikasjoner av kronisk nyresykdom
i van Der WaltI; C R SwanepoelII; B MahalaIII; A M MeyersIV
Korrespondanse
ABSTRACT
komplikasjonene ved kronisk nyresykdom (ckd) er dyslipidemi hyperkalemi, METABOLSK ACIDOSE, ANEMI og bein-og mineralforstyrrelser. Dyslipidemi kan behandles med lipoproteinsenkende midler med lav tetthet. Statiner er ineffektive i trinn 4 og 5 CKD, men er indikert for å forhindre sykdomsprogresjon i tidligere stadier. Kronisk acidose har nylig vist seg å være en risikofaktor i utviklingen AV CKD nyresvikt. Derfor er behandling obligatorisk. Praktisk sett bør dette bestå av 1-2 hakkede teskjeer natriumbikarbonat 2 – 3 ganger per dag, noe som er en billig og sikker terapi som ikke øker blodtrykket til tross for det økte natriumnivået. Målnivåer av hemoglobin, i henhold til internasjonale retningslinjer, er mellom 10 g / dL og 12 g / dL. Serumfosfatnivået økes i STADIUM 4 CKD, og spesielt i stadium 5 CKD, som er forbundet med koronar karotid og andre vaskulære forkalkninger og kan resultere i iskemisk hjertesykdom, hjerteinfarkt og hjerneslag. Et forhøyet paratyreoideahormonnivå (sekundær hyperparatyreoidisme) er også en viktig risikofaktor for kardiovaskulær sykdom og er forbundet med økt hypertensjon og resistens mot behandling AV CKD-assosiert anemi.
Dyslipidemi
Kronisk nyresykdom (CKD) er forbundet med endringer i lipoproteinstruktur og funksjon, inkludert:
- redusert lipoproteinkolesterol med høy tetthet
- økt lipoprotein med middels tetthet
- økte proaterogene lipidpartikler.
Signifikans av dyslipidemi control
- Vellykket behandling av dyslipidemi er kjent for å redusere kardiovaskulær sykdom (CVD) risiko og bør også forsinke nedgangen i nyrefunksjon.
- siden statiner har vist seg å redusere utskillelse av protein eller albumin i urin, anbefales de for CKD med proteinuri.
- Merknader om statinbruk i trinn 3-5 CKD er gitt I Tabell 1.
- Samtidig bruk av statiner og fibrater øker risikoen for rabdomyolyse.
Mål for low-density lipoprotein kolesterol
- Retningslinjene For Nyresykdommer Utfall Quality Initiative (KDOQI) anbefaler følgende for dyslipidemi terapi I CKD: i tilfeller av low-density lipoprotein kolesterol (LDL-C) <3.5 mmol / L, det første trinnet er livsstilsendring; I TILFELLER AV LDL-C >3.5 mmol / L, bør medisinering vurderes i tillegg til livsstilsendring, inkludert diettbehandling, vektkontroll og trening.
- DET er viktig at LDL-C senkes til < 1,8 mmol / L.
kdoqi retningslinjer for kolesterolsenkning hos CKD-pasienter (2013):
- Pasienter > 50 år bør få et statin.
- Pasienter i alderen 18-49 år bør få statin hvis det foreligger en annen komorbiditet.
- Nyretransplanterte mottakere bør få et statin.
Behandling av hyperkalemi og metabolsk acidose
Hyperkalemi
- etter HVERT som CKD utvikler seg i stadium, observeres acidose og hyperkalemi. Hyperkalemi er definert som et serumkaliumnivå >5,5 mmol/L. Hyperkalemi >7 mmol / L kan potensielt forårsake hjertestans.
- hvis alvorlig hyperkalemi observeres, til tross for fravær av nedsatt nyrefunksjon, bør pseudohyperkalemi, en artefakt på grunn av hemolyse av blodprøven, vurderes.
- Hyperkalemi er en risikofaktor for arytmier. Ved alvorlig hyperkalemi skal nødnivåene bekreftes VED EKG-abnormiteter som telting Av t-bølger, forlengelse av PQ-tider, etterfulgt Av forsvinning Av p-bølgen og utvidelse AV QRS-komplekset. Pasienter med livstruende EKG-funn, bradykardi og hypotensjon bør behandles raskt, etterfulgt av behandling sammen med en nefrolog.
- Legemiddelindusert hyperkalemi ved CKD forårsakes hovedsakelig av renin-angiotensin-aldosteronhemmere som ACE-hemmere, angiotensin II-reseptorblokkere (Arb) og spironolakton eller overdrevent inntak av kaliumholdige matvarer. Andre årsaker inkluderer administrering av β-blokkere, digoksin, ikke-steroide antiinflammatoriske legemidler (NSAIDs), trimetoprim eller pentamidin.
- CKD forårsaket av diabetisk nefropati kan være forbundet med hyporeninemisk hypoaldosteronisme, som kan forårsake hyperkalemi til tross for relativt godt bevart nyrefunksjon. Dette er KJENT som TYPE IV renal tubulær acidose.
Akuttbehandling
- det første trinnet er å stabilisere myokardiet. Intravenøs administrering av kalsiumglukonat endrer ikke plasmakalium, men forbedrer ekg midlertidig. Administrasjonen av kalsiumglukonat 20 mL intravenøst over 1 minutt kan gjentas hvis DET ikke er noen forbedring I EKG innen 3-5 minutter.
- det andre trinnet er å skifte kalium fra det ekstracellulære til det intracellulære rommet for å forsøke å raskt redusere serumkaliumnivået. Dette kan gjøres på tre forskjellige måter:
- Intravenøst insulin kombinert med glukose. Administrer 10 E korttidsvirkende insulin kombinert med 50 mL 50% dekstrose som bolus, etterfulgt av en intravenøs infusjon av 5% dekstrose for å forhindre hypoglykemi.
- β 2-agonist. Administrer 20 mg salbutamol, en β 2-agonist, ved innånding over 10 minutter, med virkningstid ca. 30 minutter. (Dette er vanligvis ikke nødvendig.)
- Natriumbikarbonat hos CKD-pasienter som ennå ikke er i dialyse. Bikarbonatadministrasjon kan redusere serumkalium ved å øke renal kaliumutskillelse. Effekten er svært langsom og ikke i bruk i en akutt situasjon med mindre pasienten har alvorlig metabolsk acidose som trenger bikarbonatbehandling.
- når de tidligere midlertidige tiltakene er utført, gjennomføres ytterligere tiltak for å fjerne kalium fra kroppen.
- Loop diuretika er kun vellykket hos pasienter med tilstrekkelig nyrefunksjon.
- harpiks exchanger natrium polystyren sulfonat (Kexelate) fjerner kalium fra blodet inn i tarmen i bytte for en lik mengde natrium. Det er sakte virkende og plasmakaliumet begynner bare å synke innen 1-2 timer. Det kan gis oralt eller som en retensjonsemne. Mengden gitt varierer fra 30 g til 60 g. Dette kan gjentas, men har en tendens til å forårsake forstoppelse.
- Hemodialyse er den foretrukne behandlingen for pasienter med avansert CKD og alvorlig hyperkalemi.
Forebygging
- Kostholdsrådgivning om kaliumrestriksjon.
- Unngå medisiner som forstyrrer renal utskillelse av kalium, f. eks. kaliumsparende diuretika, NSAIDs, ACE-hemmere, Arb.
- Unngå legemidler som forstyrrer kaliumforskyvninger fra intracellulære til ekstracellulære rom, f. eks. ikke-selektive β-blokkere.
- hos utvalgte pasienter med tilstrekkelig gjenværende nyrefunksjon kan behandling med et sløyfediuretikum brukes til å stimulere utskillelse av kalium i urin.
Metabolsk acidose
Metabolsk acidose er karakterisert ved:
- lavt arterielt blod pH (acidemi) (<7.35)
- redusert serum HCO3-konsentrasjon
- redusert pCO2 (fra respiratorisk kompensasjon).
Systemiske effekter
Metabolsk acidose kan føre til en rekke forandringer i vev og organer, f. eks.:
- kardiovaskulære endringer som takykardi, bradykardi, hypotensjon og hjertesvikt
- livstruende hyperkalemi
- kvalme, oppkast og magesmerter
- forvirring, med depresjon i sentralnervesystemet.
de tilknyttede symptomer og tegn vil avhenge av hastigheten og omfanget av fall i pH og av den underliggende patologi.
Uremisk acidose
Metabolsk acidose oppstår ved nyresvikt på grunn av redusert evne Til å skille Ut H+ eller manglende evne til å produsere ammoniakk.
i de tidlige stadier AV CKD (GFR < 40 mL / min) kan metabolsk acidose med normalt aniongap (AG) bli tydelig. Etter HVERT som CKD utvikler seg (GFR <20 mL / min), kan en høy AG metabolsk acidose oppstå.
i avansert CKD er en økt AG typisk på grunn av tilstedeværelsen av beholdte syrer som sulfater, fosfater, urat og hippurat.
behandlingsprinsipper
Pasienter med metabolsk acidose er ofte svært syke og tilstanden har en tendens til å forverres raskt.
rutinemessig administrasjon av natriumbikarbonat er kontroversielt, selv om det må gjøres for å korrigere alvorlig acidose.
de potensielle komplikasjonene ved administrering av natriumbikarbonat inkluderer volumoverbelastning, spesielt hos pasienter med nedsatt nyre-eller hjertefunksjon, hypernatremi, hypokalemi, hypokalsemi og alkalose.
nødvendig mengde bikarbonat (mmol) kan estimeres som følger:
målplasma hco3- (mmol/L) – nåværende plasma HCO3- (mmol/L) x 40% kroppsvekt (kg).
Anemi ved CKD
Anemi er den vanligste komplikasjonen VED CKD og er forbundet med sterkt redusert livskvalitet. Vellykket behandling av anemi ved nyresykdom kan redusere nedsatt nyrefunksjon. Målet hemoglobinnivåer er 10 – 12 g/dL ved behandling av anemi I CKD. Behandlingen er kostbar og derfor er rasjonell vurdering obligatorisk.
nyreanemi
Nyreanemi er typisk normokromisk normocytisk. Det skyldes hovedsakelig nedsatt produksjon av erytropoietin i nyrene og delvis av uremiske toksiner. Andre årsaker som kan spille en rolle I CKD, spesielt hos dialysepasienter, er:
- erytropoietin resistens (mest signifikant)
- benmargtoksiner (ingen har blitt isolert ennå)
- benmargsfibrose, sekundært til hyperparatyreoidisme
- pågående inflammatoriske prosesser, f. eks. ubehandlede infeksjoner
- hematinmangel (jern, folat og vitamin B12)
- økt destruksjon av røde blodlegemer
- unormale røde cellemembraner som forårsaker økt osmotisk skjørhet
- økt blodtap fra okkult gastrointestinal blødning og blodprøvetaking og under hemodialyse
- ACE-hemming.
Erytropoietin er et glykoproteinhormon som stimulerer produksjonen av røde blodceller ved å binde seg til erytropoietin-reseptorer, lokalisert på tidlige erytroide stamceller i benmargen.
bindingen av erytropoietin til disse stamceller sparer dem fra apoptose og tillater derfor celledeling og modning i røde celler. Ved CKD kan erytropoietinnivået være normalt, men utilstrekkelig for graden av anemi. Mekanismene som svekker erytropoietin produksjon i syke nyrer forblir dårlig forstått. Hemming av erytropoiesis med uremiske hemmere er også mulig og kan i stor grad bidra til ANEMI av CKD; slike faktorer er ikke identifisert. Dialyse kan forbedre nyreanemi og effekten av erytropoietin-stimulerende midler. Pasienter med nyresykdom kan utvikle kroniske infeksjoner og andre kroniske sykdommer. Kronisk sykdom bidrar til anemi i slike tilfeller. Anemi av kronisk sykdom medieres av inflammatoriske cytokiner gjennom hemming av erytropoietin produksjon og effekt og redusert jerntilgjengelighet.
Hepcidin er nøkkelmediatoren for jernmetabolisme. I inflammatoriske tilstander blokkerer hepcidin jernabsorpsjon i tarmen og fremmer jernsekvestrasjon i makrofager.
Andre årsaker
Anemi assosiert med CKD er mest sannsynlig renal anemi; imidlertid må differensialet for andre sykdommer anses som sant for trinn 1-3 CKD.
evalueringen av anemi hos PASIENTER MED CKD bør inkludere en fullstendig blodtelling med røde celleindekser(gjennomsnittlig hemoglobinkonsentrasjon i kroppen, gjennomsnittlig volum i kroppen). Renal anemi er vanligvis normokromisk og normocytisk. Vitamin B12 og folatmangel kan føre til makrocytose, mens jernmangel eller arvelige sykdommer i hemoglobin kan produsere mikrocytose. Jernstudier bør utføres for å vurdere nivået av jern i vevsforretninger eller tilstrekkelig jernforsyning for erytropoiesis.
Anemi kan bety tilstedeværelse av underernæring eller systemisk sykdom. Det er en uavhengig risikofaktor for sykehusinnleggelse, CVD og dødelighet. ACE-hemmere kan forverre anemi.
Behandling av anemi beskytter hjertet
Anemi forverrer hjertesvikt. Behandling av anemi er gunstig for forventet levealder og kan også forbedre prognosen FOR CVD. Livskvaliteten er forbedret for de med et hemoglobinnivå innenfor målområdet.
målnivå for hemoglobin
Retningslinjene For Nyresykdomsforbedrende Globalt Utfall (Kdigo) angir at hemoglobinnivået skal variere fra 10,0 g/dL til 12 g/dl hos PASIENTER MED KRONISK NYRESVIKT som får dialyse. Pre-dialyse nivåer bør være på 10 g / dL.
Rolledeling mellom nephrologists og fastleger
Tidlig henvisning til en nefrolog er tilrådelig. Når behandlingsstrategien er bestemt, fortsetter nephrologists og primary care physicians ledelsen i partnerskap.
Evaluering av jernmangel
Evaluering av jernunderskudd og riktig jerntilførsel er viktig ved behandling av anemi. Anemi kan bedres ved administrering av jerntilskudd, selv når pasienten tilsynelatende ikke har jernmangel, da bruk av rekombinant erytropoietin kan forårsake relativ jernmangel.
kdoqi-retningslinjene for rekombinant humant erytropoietin ved CKD er:
- serum ferritin > 100 ng / mL før dialyse
- serum ferritin > 200 ng/mL hos dialysepasienter
- transferrinmetning > 20%.
Jern kan gis enten intravenøst eller oralt. Intravenøst jern er mer effektivt, spesielt for dialysepasienter og de som behandles med erytropoietin.
bruk av eksogene erytropoietiner
det finnes for tiden en rekke erytropoietinstimulerende midler tilgjengelig, inkludert eldre, korttidsvirkende legemidler og nye, langtidsvirkende. Passende middel og dose avhenger av en rekke faktorer, inkludert kostnad, effekt og bekvemmelighet. Da disse stoffene er dyre og har bivirkninger, er deres ledelse best overlatt til en nephrologist.
Bone and mineral disorders
Hyperfosfatemi Er nøkkelen abnormitet som setter av en kaskade av metabolske hendelser, noe som resulterer i bentetthet AV CKD.
Fosfat beholdes da nyrefunksjonen forverres-mye det samme som kreatinin beholdes. Denne retensjonen blir tydelig når trinn 3b CKD er nådd. Det vil gradvis forverres når sluttstadiet nærmer seg og må senkes til innenfor normale grenser.
en høy fosfat diett stimulerer osteocytter til å produsere fibroblast vekstfaktor 23 som i sin tur hemmer hydroksylering av vitamin d til aktiv 1,25 vitamin D3. Uten vitamin D3 reduseres kalsiumabsorpsjonen og benremodelleringen. Den resulterende hypokalsemi er en viktig stimulans for frigjøring av paratyreoideahormon (PTH), med påfølgende utvikling av nyrebeinsykdom. Serum alkalisk fosfatase er en markør for økt benomsetning. Derfor viser høye blodnivåer pth-aktivitet.
Merk at både hyperfosfatemi og vitamin D3-mangel fører til økt pth-sekresjon.
Innledningsvis kan stimulansen for pth-sekresjon kontrolleres ved å øke serumkalsiumet, redusere fosfatnivåene i blodet og foreskrive vitamin D3. Dette er det sekundære hyperparathyroidismetrinnet (Tabell 2). Men med tiden og ukontrollert, langvarig stimulering av pth-sekresjon, blir parathyroidhormonene autonome og scenen for autonom hyperparathyroidisme er nådd(Tabell 3). Parathyroidektomi kan nå være nødvendig eller dyre kalsimimetiske legemidler må administreres for å forsøke å gjenopprette det uordnede metabolske miljøet.


det er usikkerhet om tolkningen av vitamin D3 nivåmålinger. Hvis de skal måles, anbefales 25-OH-vitamin D3 nivåer for vurdering.
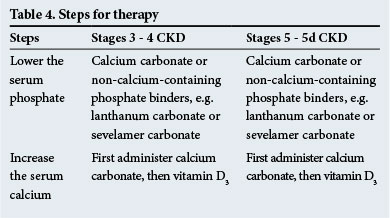
Terapi
trinnene for behandling er vist I Tabell 4. Ikke-kalsiumholdige fosfatbindemidler anbefales når det er signifikant metastatisk forkalkning og / eller når hyperkalsemi er til stede.
Calcimimetics, som sensibiliserer parathyroidkjertlene til serumkalsium, er nyttige for å foreskrive i hyperparathyroidisme når serumets pth-nivåer er høye (2-9 ganger over normalområdet-sjekk med laboratoriet for normale områder). De har en rolle å spille i avtagende pth-nivåer i noen av de kliniske situasjonene som oppstår i CKD.
Blodoppfølging
disse er gitt I Tabell 5.
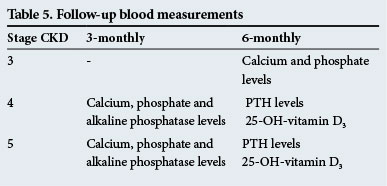
disse oppfølgingstidene er bare retningslinjer, og testene bør utføres oftere hvis det er betydelige abnormiteter.
Spesielle punkter å merke
- Involvere en nephrologist tidlig i LØPET AV CKD.
- Unngå over-undertrykkelse av parathyroidkjertlene, da dette vil føre til dynamisk bein sykdom.
- det nøyaktige PTH-nivået hvor sekundær og autonom hyperparatyreoidisme er diagnostisert er usikkert på grunn av varierende analyser. Biokjemien, som beskrevet ovenfor (sammen med røntgenbilder av bein), må da brukes til å bistå i diagnosen.
- vær oppmerksom på trender i serum alkalisk fosfatase nivåer; nivået kan være i normalområdet, men kan ha doblet fra forrige lesing.
- Osteoporose følger med bein sykdom som oppstår I CKD. Bisfosfonater må ikke brukes i TRINN 3-5 CKD pasienter.