Zpět k Psaní Lewis Struktury Molekuly
kostra struktura kovalentní molekuly mohou často být stanovena s ohledem na valence jednotlivých atomů. Obvykle se atom, který tvoří největší počet vazeb, nachází ve středu kostry, kde se může připojit k maximálnímu počtu dalších atomů.
Příklad 1: kyselina chlorná má molekulární vzorec HOCl. Nakreslete
strukturální vzorec.
Řešení Existuje několik možných způsobů, jak se spojují atomy spolu
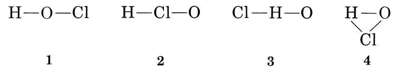
obvyklé valence H je 1, a tak struktury 3 a 4, které dvěma vazbami H, mohou být odstraněny. Obvyklá valence Cl je také 1, a tak lze vyloučit i strukturu 2. Struktura 1 znázorňuje h tvořící jednu vazbu, Cl tvořící jednu a O tvořící dvě, v souladu s obvyklými valencemi, a tak je zvolena.
celkový počet dostupných valenčních elektronů je 1 z H plus 6 Z O plus 7 z Cl nebo 14. Plnění těchto do kostry máme
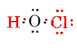
Všimněte si, že O, který měl největší valenci, je ve středu kostry.
Příklad 2:
Nakreslit strukturní vzorec pro hydroxylamin, NH3O.
Řešením je V tomto případě N má největší valence (3), následuje O (2) a H (1). Jak N, tak O mohou tvořit „mosty“ mezi jinými atomy, ale H nemůže. Proto jsme místo, N a O, ve městě skeletu dát
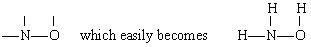
přidáním tří H atomy.
Existuje celkem 5 + 3 + 6 = 14 valenční elektrony z N, 3H a O. Ty mohou být umístěny takto:
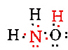
Jakmile Lewis diagramu bylo zjištěno,, molekulární vzorec je často přepsán, aby nám připomněl, co strukturní vzorec je. Například molekulární vzorec pro hydroxylamin je obvykle napsán NH2OH místo NH3O, aby nám připomněl, že dvě H jsou vázány na N a jedna na o. Předpokládá se, že osoba, která čte vzorec, si uvědomí, že N A O mají každý jeden valenční elektron, který se navzájem sdílí, spojující —NH2 s —OH. V některých případech více než jedna struktura skeletu uspokojí valenci každého atomu a také oktetové pravidlo. Například, můžete ověřit, že molekulární vzorec C2H6O odpovídá na obě tyto:
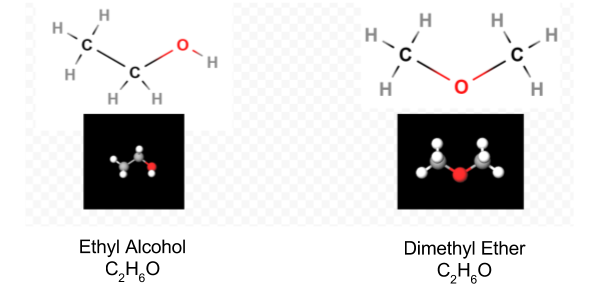
V takovém případě můžeme jen rozhodnout, který z molekulární strukturu, máme tím experimentovat. Vlastnosti ethylalkoholu, když jsou zředěny vodou a spotřebovány, jsou dobře známy. Dimethylether je plyn. Stejně jako diethylether používaný v operačních sálech je vysoce výbušný a může vás uspat. Dvě molekuly, jako je dimethylether a ethylalkohol, které mají stejný molekulární vzorec, ale různé strukturní vzorce jsou považovány za izomery.
Zpět k Psaní Lewis Struktury Molekuly
Poděkování:
C2H6O molekul a jejich kosterních struktur byly vytvořeny pomocí MolView.