Abstrakti
Lisämunuaiskasvaimet voivat olla hyvänlaatuisia löydöksiä tai merkitä niiden hormonitoiminnan tai mahdollisen pahanlaatuisen histologian aiheuttamaa korkeaa sairastuvuutta ja kuolleisuutta. Lääketieteellinen kirjallisuus osoittaa, että tämä ehto johtuu tekniikan parantumisesta ja levittämisestä monenlaisissa kuvantamismenetelmissä, mikä lisää huomattavasti lisämunuaisen kyhmyjen diagnoosia ja sen välitöntä hoitoa. Kun hoidetaan potilasta, jolla on lisämunuaiskasvaimia, ammattilaisen pääasiallisena huolenaiheena tulisi olla selvittää, onko vaurio pahanlaatuinen kasvain ja onko olemassa hormonaalista toimintaa, jotka ovat kaksi tapausta, jotka yleensä vaativat leikkausta. Sen määrittämiseksi, onko vaurio hormonaalisesti toimiva, on tarpeen suorittaa täydelliset kliiniset ja endokriiniset arvioinnit. Näin ollen sen pitäisi olla osa yleislääkärin rutiinia tunnistaa ja arvioida, onko vaurio pahanlaatuinen tai funktionantti, tilanteissa, joissa adrenalektomia on tarpeen.
Keywords
Adrenocortical tumors, Adenoma, Adrenal, Cushing’s syndrome, Aldosteronoma
List of Acronyms
ACTH: Adrenocorticotropic Hormone; DEXA: Dexamethasone; FEO: Pheochromocytoma; FEO/ PGL: Feocromocitoma/Paraganglioma; HA: Systemic Arterial Hypertension; SAGH: Autonomous Subclinical Hypersecretion of Glucocorticoids; SC: Serum Cortisol; UFC: Urine Free Cortisol; IA: Adrenal Incidentaloma; HU: Hounsfield Unit
Introduction
Adrenal gland tumors are common diseases in clinical practices. Sen mukaan, miten ne ilmenevät, ne luokitellaan funktionantteihin (jotka tuottavat hormoneja) ja toimimattomiin (tunnetaan myös vaimentimina). Biologisen käyttäytymisen osalta ne voidaan jakaa hyvän-tai pahanlaatuisiin kasvaimiin .
useimmat lisämunuaiskuoren kasvaimet ovat hyvänlaatuisia, yksipuolisia ja toimimattomia adenoomia, joiden halkaisija on alle 4 cm ja jotka on havaittu vatsan kuvantamistutkimuksissa .
tälle ”satunnaishavainnolle” annetaan nimi lisämunuaisen satunnaishavainto ja se määritellään lisämunuaisen massaksi, joka on kliinisesti havaitsematon ja jota esiintyy kuvantamistutkimuksissa muista syistä kuin lisämunuaisten arvioinnista. Lisämunuaisten adenoomien esiintyvyys on viime vuosina lisääntynyt, koska vatsalaukun kuvantaminen on lisääntynyt herkästi .
toimivat lisämunuaiskasvaimet ovat yleensä hyvänlaatuisia adenoomatyyppejä, jotka aiheuttavat esimerkiksi Cushingin oireyhtymän, primaarisen aldosteronismin tai harvemmin virilisaation . Luuytimessä feokromosytoomat, katekoliamiinien erityskasvaimet, jotka erottuvat harvinaisuudesta huolimatta ja merkitsevät suurta sairastuvuutta ja kuolleisuutta .
epidemiologia
yhdistetyssä tutkimuksessa, jossa oli erilaiset valinta-ja diagnoosikriteerit, meillä oli lisämunuaiskasvainten tärkeimmät etiologiat: adenoomat 41%, etäpesäkkeet 19%, karsinoomat 10%, Myelolipoomat 9% ja Feokromosytoomat 8%. Suurin osa jäljelle jääneistä tapauksista (13%) oli hyvänlaatuisia leesioita, kuten lisämunuaiskystia .
kliinisissä raporteissa lisämunuaisten ilmaantuvuus oli huipussaan viidennellä-seitsemännellä vuosikymmenellä. Potilaiden keski-ikä diagnoosihetkellä on 55 vuotta, eikä naisten ja miesten välillä ole merkittäviä ikäeroja .
esiintyvyys lisääntyy iän myötä; esiintyvyys on alle 1% alle 30-vuotiailla ja 7% yli 70-vuotiailla potilailla .
johtuu hormonituotannosta, vaikka suurin osa kasvaimista ei toimi, tiettyjen hormonien hieman lisääntynyt tuotanto voidaan todentaa vähintään 15%: ssa tapauksista.
hormonaalinen arviointi
kortisolia erittävät adenoomat tai lisämunuaiskarsinoomat, feokromosytoomat, aldosteronomat ja androgeenien eritysleesiot ovat sellaisia eritys-tai funktionaalisia lisämunuaiskuoren massoja, joita diagnosoidaan useammin .
kortisolia tuottavat kasvaimet
nämä kasvaimet tuottavat yleensä kortisolin määrän pienenemistä, mikä ei useimmissa tapauksissa riitä lisäämään vapaan kortisolin erittymistä virtsaan. Ne pystyvät kuitenkin aiheuttamaan hypotalamus-aivolisäke-akselin suppression. Yleensä potilailla ei ole Cushingin oireyhtymään liittyviä ilmenemismuotoja. Tästä syystä tämä tila tunnetaan subkliinisenä Cushingin oireyhtymänä tai subkliinisenä hyperkortisolismina .
on tärkeää korostaa eroa subkliinisen Cushingin oireyhtymän, jolle on ominaista kliinisesti ilmennyt biokemiallinen poikkeavuus, ja prekliinisen Cushingin oireyhtymän välillä, joka on itse oireyhtymän kehityksen alkuvaihe. Glukokortikoidien autonominen subkliininen liikaeritys (SAGH) on uusin termi, jonka tarkoituksena on määritellä lisämunuaisen adenooman aiheuttama autonominen kortisolin eritys potilailla, joilla ei ole Cushingin oireyhtymän oireita .
aikuisilla hyperkortisolismin viittaavimpia merkkejä ja oireita ovat proksimaalinen lihasheikkous, kasvojen runsaus, raajojen menetys, johon liittyy vatsan ja kasvojen lisääntynyt rasva, leveät violetit raidat, hematoomat ilman selvää traumaa ja supraklavikulaariset puristukset .
monien hyperkortisolismin oireiden vuoksi muun muassa hypertensio ja diabetes eivät ole tyypillisiä, ja niiden kliinisen ulkonäön aste on yhdenmukainen hormonaalisen ylituotannon laajuuden vaihtelun kanssa, SAGH: n tarkka esiintyvyyden osoittaminen riippuu käytetyillä testimenetelmillä saaduista tuloksista ja kriteereistä, joilla oireiset potilaat valitaan taudin vahvistamista varten .
jos epäilet Cushingin oireyhtymää, 1 mg: n deksametasonisuppressiotesti tulee tehdä yön yli. Päivä ennen seerumin kortisolin keräämistä, joka tapahtuu klo 8, potilas ottaa 1 mg deksametasonia suun kautta klo 11 pm .
sitä pidetään epänormaalina kortisolivasteena, kun se esitetään vaihteluvälillä 1, 8-5, 0 mcg / dl, tai tarkemmin:
A) Jos
B) Jos 1, 8-5 mcg / dL: epämääräiset tulokset;
C) > 5 mcg / dL: erittäin todennäköinen diagnoosi Cushingin oireyhtymästä;
epänormaali suppressio deksametasonilla vastaa epäilyttävää seulontaa, joten se on varmistettava antamalla vapaata virtsan kortisolia 24 tuntia sen jälkeen, kun deksametasonia on annettu 8 mg yön yli, ja seerumin ACTH-annos, jotta voidaan määrittää Cushingin oireyhtymän alkuperä, sillä yleensä esiintyy ei-tuettuja pitoisuuksia (ACTH-riippuvainen) .
subkliinisen Cushingin oireyhtymän diagnosoinnissa käytetään seuraavia kriteerejä:
– Plasmaattinen kortisoli > 5 mcg/dL 1 mg: n deksametasonitestissä ilman muuta stigmaa tai vähintään 2 seuraavista tuloksista .
1.Plasman ACTH
2.Vapaa virtsan kortisoli 24 tuntia kestäneessä näytteessä nousi;
3.Seerumin kortisoli > 3 mcg / dL 1 mg: n deksametasonitestissä (Kuva 1).
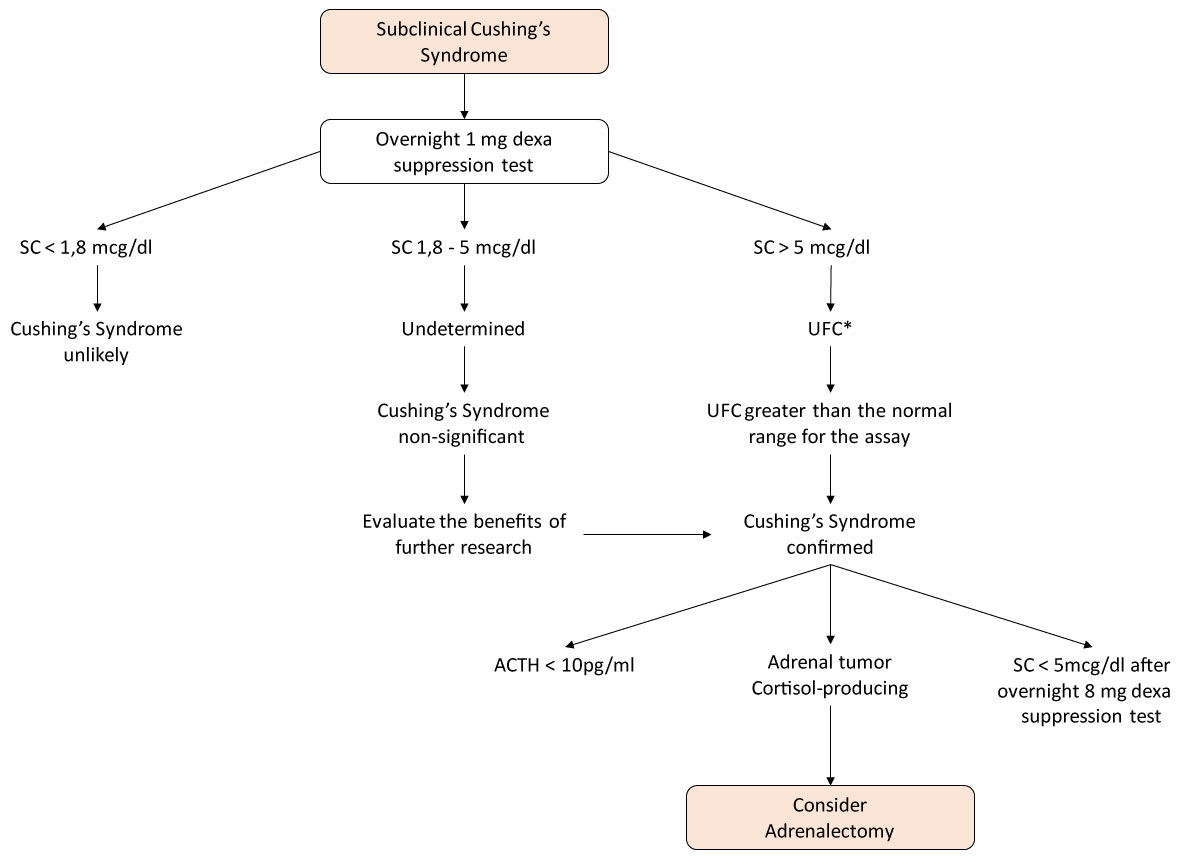 Kuva 1: algoritmi Cushingin oireyhtymän tutkimiseen lisämunuaisissa. *Vähintään kaksi mittausta. Näytä kuva 1
Kuva 1: algoritmi Cushingin oireyhtymän tutkimiseen lisämunuaisissa. *Vähintään kaksi mittausta. Näytä kuva 1
siksi subkliinisen Cushingin oireyhtymän lähestymistavasta on vaikea päästä yksimielisyyteen, sillä sitä voidaan hoitaa kliinisesti tai leikkauksella . Potilailla, joilla on monia samanaikaisia sairauksia, jotka voivat liittyä hyperkortisolismiin, adrenalektomian riski/hyöty on otettava huomioon hoitona. Suuri osa tämän leikkauksen saaneista potilaista voi kehittyä akuutti lisämunuaisen vajaatoiminta (joskus kuolemaan johtava), joten perioperatiivisen kattavuuden saavuttaminen glukokortikoidilla on erittäin tärkeää.
Katekoliamiinia tuottavat kasvaimet
Feokromosytoomat ovat lisämunuaisen ytimen kromaffiinisolujen kasvaimia, jotka tuottavat, varastoivat, metaboloituvat ja erittävät katekoliamiineja, joissakin tapauksissa muut peptidihormonit paraganglioomat (PGL) ovat samanlaisia kasvaimia, mutta ekstraperäisiä. Feo / PGL-oireyhtymä on harvinainen sairaus, jonka esiintyvyys on arviolta 0,1-0,2% hypertensiivisistä henkilöistä .
useimmat katekoliamiinia erittävät kasvaimet ovat satunnaisia. Osalla potilaista (noin 40%) tauti on kuitenkin osa perhehäiriötä; näillä potilailla katekoliamiinia erittävät kasvaimet ovat todennäköisemmin kahdenkeskisiä lisämunuaisten feokromosytoomia tai paraganglioomia.
feokromosytoomaan liittyy useita suvussa esiintyviä häiriöitä, joilla kaikilla on autosomaalinen dominanttiperimä:
* feokromosytooman likimääräinen esiintymistiheys näissä häiriöissä on 10-20% VHL-oireyhtymässä, 50% MEN2: ssa ja 3% NF1: ssä .
nämä kasvaimet ovat erityisen tärkeitä, koska vaikka harvinaiset (samoin kuin aldosteronin eritysadenoomat) aiheuttavat kirurgisesti korjattavan verenpainetaudin . Hypertensio on usein puuskittaista. Feokromosytoomaa sairastavien potilaiden klassinen oirekolmikko koostuu episodisesta päänsärystä, hikoilusta ja takykardiasta, ja on olemassa sellaisten potilaiden esiintyvyys, joilla ei ole kolmea klassista oiretta. Niiden potilaiden lisäksi, joilla on taudin tyypillisiä kliinisiä ilmenemismuotoja, tutkimus on tehtävä myös henkilöillä, joiden suvussa on FEO tai medullaarinen kilpirauhassyöpä, kun läsnä on HA nuoria, HA vaikea hallita tai anestesia-induktio.
feokromosytooma diagnosoidaan tyypillisesti mittaamalla metanefriinit ja katekoliamiinit virtsasta ja plasmasta, kuten kuvassa 2 esitetään .
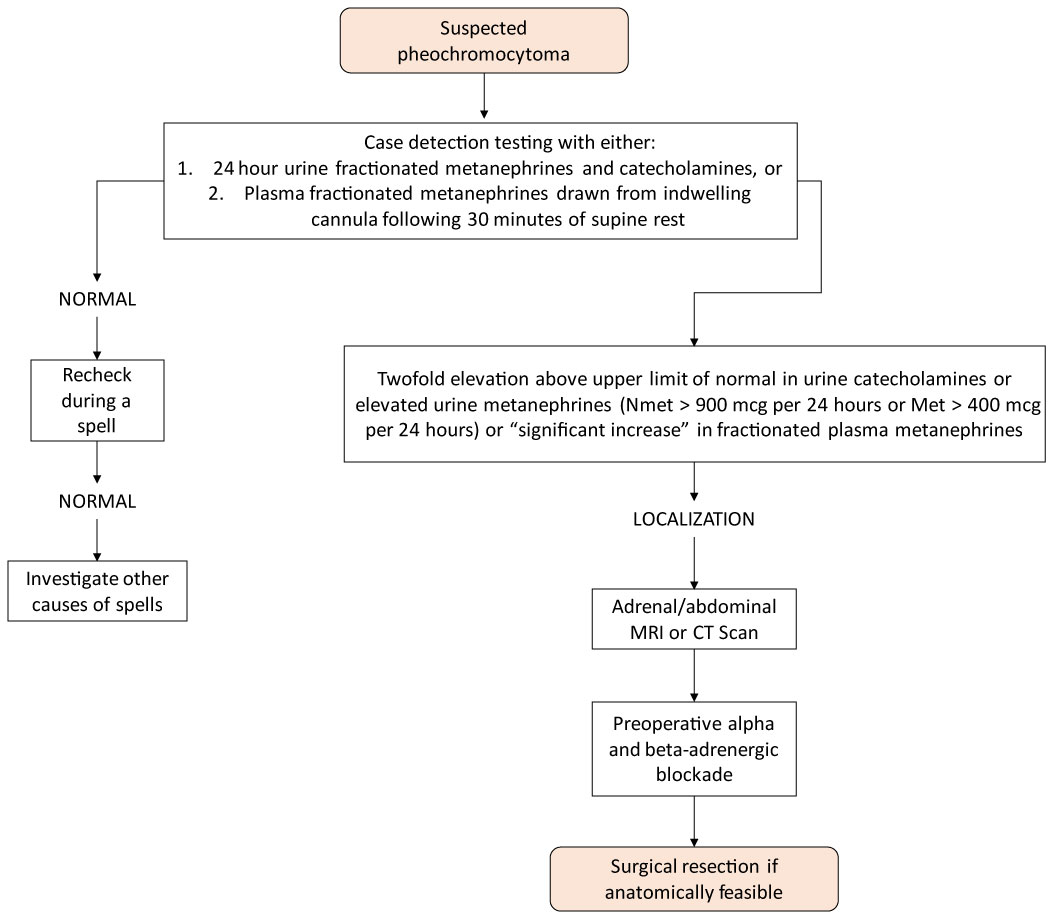 kuva 2: algoritmi lisämunuaisten Satunnaistaloomien feokromosytoomien tutkimiseksi. Näytä kuva 2
kuva 2: algoritmi lisämunuaisten Satunnaistaloomien feokromosytoomien tutkimiseksi. Näytä kuva 2
mitä tulee kuvamenetelmiin, Feokromosytoomilla on suurempi vaimennus tehostamattomassa CT: ssä (> 20 HU), lisääntynyt massan vaskularisaatio, viive varjoaineen pesussa (10 minuuttia varjoaineen antamisen jälkeen, absoluuttinen varjoaineen pesu Alle 50%), suuri signaalin voimakkuus T2-painotetussa MRI: ssä, kystinen ja hemorraginen muutos ja vaihteleva koko, ja ne voivat olla molemminpuolisia.
sen sijaan lisämunuaisen karsinoomaan tai etäpesäkkeisiin viittaavia kuvantamisominaisuuksia ovat: Epäsäännöllinen muoto, epähomogeeninen tiheys, korkeat TEHOSTAMATTOMAT CT-vaimennusarvot (> 20 HU), viivästynyt varjoaineen poistuminen elimistöstä (esim .4 cm ja kasvaimen kalkkeutuminen.
aldosteronia tuottavat kasvaimet
Aldosteronomat ovat melko harvinaisia ja vaikeasti havaittavia, ja niille on kliinisesti ominaista hypokalemiaan liittyvä systeeminen valtimon hypertensio. Koska useimmat potilaat ovat hypokalsemian suhteen oireettomia, eli he ovat normaalikaleemisia, on suositeltavaa, että kaikki potilaat, joilla on lisämunuaisen incidoosiin liittyvä hypertensio, arvioidaan mittaamalla heidän aldosteronin ja reniinin plasmapitoisuudet, ja niiden välinen suhde, joka on suurempi kuin 30, viittaa voimakkaasti autonomiseen aldosteronin tuotantoon. Suurempi syy kuin 50 erottaa selvästi primaarisen aldosteronismin muista essentiaalisen hypertension muodoista jo alle 20 kiistää diagnoosin ja johtaa välillä 20-30, osoittavat tarkemman diagnoosin.
spironolaktonia käyttäviä potilaita ei voida arvioida aldosteronisuhteen ja plasman aktiivisuuden perusteella. Muita lääkkeitä, jotka voivat vaikuttaa kyseenalaisiin tuloksiin, ovat beetasalpaajat, alfa-adrenergiset agonistit ja tulehduskipulääkkeet. Samoin joissakin lääkkeissä voi ilmetä konservatiivisen angiotensiinientsyymin inhibiittorin väheneminen, kuten aldosteronireseptorin salpaajassa, tiatsiinin estäjässä ja kalsiumkanavan kuvion 3 dihydropyridiinissä .
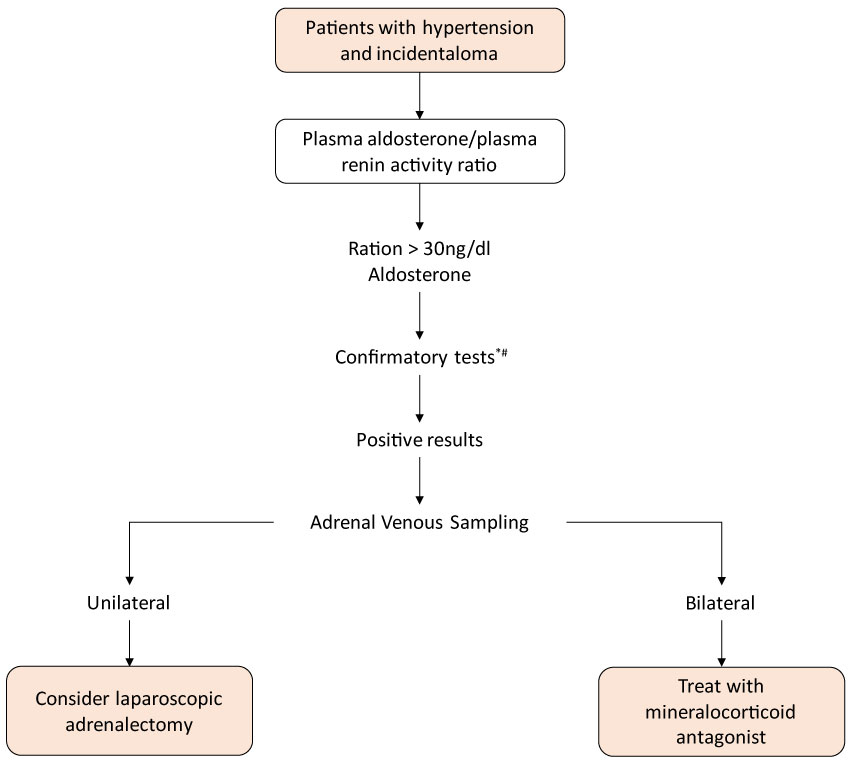 kuva 3: algoritmi hyperaldosteronismin tutkimiseksi lisämunuaisten Satunnaispotilaissa. *Yleisimmin käytetyt Varmistustestit: oraalinen natriumkuormitustesti, laskimonsisäinen keittosuolaliuoksen infuusiotesti. Näytä kuva 3
kuva 3: algoritmi hyperaldosteronismin tutkimiseksi lisämunuaisten Satunnaispotilaissa. *Yleisimmin käytetyt Varmistustestit: oraalinen natriumkuormitustesti, laskimonsisäinen keittosuolaliuoksen infuusiotesti. Näytä kuva 3
lisämunuaiskuoren katetrointi on arviointimenetelmä, joka edistää sen varmistamista, onko aldosteronituotannon lisääntyminen yli 40-vuotiailla potilailla, joilla on vahvistettu hyperaldosteronismi, todella aiheutunut satunnaisesta loomasta tai lisämunuaisen hyperplasiasta.
tällaisissa tapauksissa adrenalektomia ei ratkaisisi hormonaalista hyperproduktiota, joka tulisi pitää kurissa lääkkeillä, aldosteroniantagonisteilla kuten spironolaktonilla .
potilailla, joilla on spontaani hypokalemia, plasman reniini alle havaitsemisrajan ja plasman aldosteroni > 20 ng/dl, on esitetty, ettei lisätutkimuksia tarvita.
androgeenia ja estrogeenia tuottavat kasvaimet
21-hydroksylaasin puutoksesta johtuvassa synnynnäisessä lisämunuaisen hyperplasiassa on tavallista löytää lisämunuaisten massoja, yksi-tai kahdenvälisiä, ACTH: n aiheuttaman kroonisen liiallisen lisämunuaisten stimulaation seurauksena .
lisämunuaisten adenoomia tuottava sukupuolihormoni on hyvin harvinainen. Androgeenia tuottavat karsinoomat ovat myös harvinaisia. Androgeenien tai ylimääräisen estrogeenin tapauksia kuvataan harvoin potilailla, joilla on hyvänlaatuinen lisämunuaiskuoren adenooma, mutta yleensä ne ilmenevät oireina tai merkkeinä virilizaatiosta naisilla (akne, hirsutismi) tai feminisaatiosta miehillä (Gynekomastia). Näin ollen tällaisia vaurioita ei voida pitää todellisina IAs: nä. Siksi tarve mitata sukupuolihormoneja ja steroidien esiasteita on rajoitettu tapauksissa lisämunuaisen leesioiden kanssa määrittämättömyys tai epäily kuvantamisominaisuudet maligniteetti, jossa kohonneet tasot voivat viitata lisämunuaiskuoren alkuperä kasvaimen ja viittaa läsnäolo lisämunuaisen adenokarsinooma . Adrenalektomia on tarkoitettu hormonien hallintaan henkilöillä, joilla on virilization tai korkeat androgeenipitoisuudet .
estrogeenia tuottavat kasvaimet ovat melko harvinaisia ja useimmissa tapauksissa pahanlaatuisia. Näiden kasvainten esiintyminen miehillä ilmenee yleensä naisistumisen kautta gynecomastia, vähentynyt libido, kivesten surkastuminen; naisilla se voi ilmetä rintojen arkuuden ja verenvuodon kautta . Tällaisissa tapauksissa voidaan osoittaa myös adrenalektomia.
Keskustelu
lisämunuaisten kuvantamista koskevat tutkimukset ovat erityisen merkityksellisiä ymmärrettäessä, että tämän alueen ammattilainen on tarkkaavainen ja utelias minkä tahansa lisämunuaisten terveyttä epäilevän poikkeavan piirteen suhteen.
samanaikaisesti voidaan todeta, miten tärkeää on tuntea kunkin havaitun tapauksen kannalta olennaiset tehokkaat diagnosointimenetelmät ja hoito.
kaikista hormonitutkimuksessa käytetyistä ja ehdotetuista tutkimussuunnitelmista eniten toistuu se, joka käyttää seerumin kortisolia yöllisen suspension jälkeen, 1 mg deksametasonia (subkliiniseen hyperkortisolismiin) ja plasman metanefriinejä (FEO: hon). Aldosteronomas-valmisteen tutkimus on indisoitu vain hypertensio-ja hypokalemiatapauksissa, plasman aldosteronin ja plasman reniiniaktiivisuuden määrittämisessä.
useissa medical symposiumissa julkaistuissa ja levitetyissä tutkimuksissa mainitaan useita hormonaalisiin tutkimuksiin käytettäviä tutkimussuunnitelmia, lisämunuaisten kudossolujen poikkeavuuden havainnointia ja löytämistä, näiden rauhasten suojaamia erilaisia kasvaimia sekä sairauksien ennaltaehkäiseviä ja hoitotoimenpiteitä, jotka tarjoavat potilaille elämänlaatua.
tunnustukset/eturistiriidat
kenelläkään kirjoittajista ei ole eturistiriitaa.
Citation
do Prado BC, Schafasteck GS, Puppim AR (2019) Hormonal Evaluation of Adrenal Tumors: What the Common General Practitioner Should Know. Int Arch Urol Complic 5: 063. doi.org/10.23937/2469-5742/1510063