ez nem nyilvánvaló. A vegyérték elektronok azok, amelyek fontosak a kémiai kötésben. Az átmeneti fémek esetében a “fontos” szó a kontextustól függően változik.
könnyebb és praktikusabb leírni, hogy mely pályák valenciapályák, amikor az átmeneti fémekről van szó (bár a lantanidok és aktinidok esetében nehéz lesz).
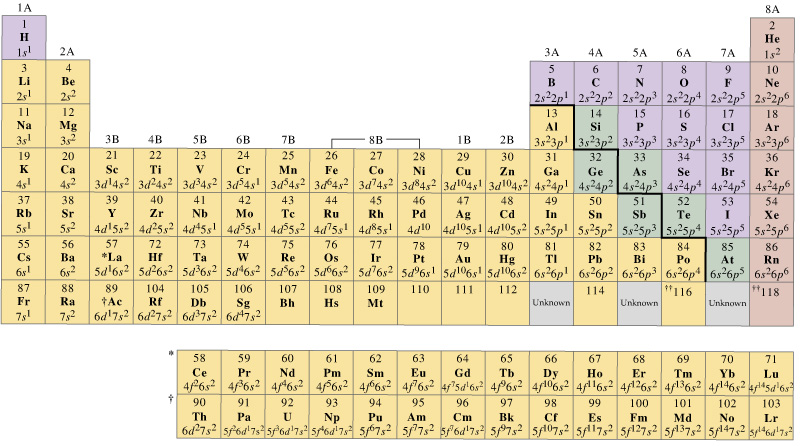
általában az első soros átmenetifémeknek van egy sor vegyértékpályájuk, amelyek tartalmazzák a #4s# és #3D#’s-t, de a vegyértékelektronok száma változó lesz.
például…

- a Szkandiumnak van értelme, ha legfeljebb három vegyértékelektron van, mivel #”Sc”^(+3)# oxidációs állapot létezik (például #”ScCl”_3#), de nem #”Sc”^(+4)# vagy magasabb. A# +3 # oxidációs állapot három vegyértékelektron átvitelét igényelte volna, ha tiszta kationt képezne.
- a krómnak legfeljebb hat vegyértékelektronja lehet, amely magában foglalja a #3d # elektronjait, mivel #+6# oxidációs állapotot képes elérni (azaz #”Cr”_2″O”_7^(2 -)#, vagy # “CrO”_4^(2-)#).
- a réz általában #+1# oxidációs állapotú (pl. #”CuCl”#), ezért van értelme, hogy az egy #4S# elektronját leggyakrabban vegyértékelektronként használja. De a# +2 # oxidációs állapot is ismert(például #”CuCl”_2#), így képes a #bb(3D)# elektronjaiból is elvenni a vegyértékelektronjait.
másrészt könnyen kijelenthetjük, hogy az első soros átmenetifémek vegyértékpályái a #4s# és #3D# pályák.
tehát általában azt mondanám, hogy az átmeneti fémek (és a lantanidok és aktinidok) vegyértékelektronjainak száma kiszámíthatatlan módon változik, de a vegyértékpályákat néha meg lehet jósolni elegendő kémiai intuícióval.
jogi nyilatkozat: a lantanidok és aktinidok számára azonban általában nehéz megjósolni, hogy mely pályák vegyértékűek.
például az aktinidák #5f# és #6D# pályái nagyon közel vannak a #7s# pályájukhoz, így az atomenergia-számítások végrehajtása során kitalálhatjuk és belefoglalhatjuk a #7s#, #6d# és #5f# valenciaterületeket (még akkor is, ha a #6D# pályák üresek).