Bevezetés
a Peyronie-kór (Pd) a pénisz lokalizált, sebgyógyító, kötőszöveti rendellenessége, amelyet a tunica albuginea hegesedése jellemez. Ez a rostos rugalmatlan heg vezet pénisz fájdalom, pénisz deformitás és merevedési zavar (ED) nehezen teljesítő coitus. Francois de la Peyronie először 1743-ban írta le az állapotot, miközben ő volt a sebész Lajos XIV Franciaország. Bár a korábbi tanulmányok 0,3–0,7% – os incidenciáról számoltak be, a legújabb publikációk 3,2–8,9% – os általános incidenciát mutattak, az esetek több mint 75% – a 45 és 65 év közötti férfiaknál fordult elő (1,2). Megjegyzendő, hogy a betegek 10% – ánál jelentkeznek a tünetek 40 éves kor előtt (2). Ezenkívül a radikális prosztatektómiát követő PD előfordulása 15,9% – ot jelent, és egy nemrégiben készült tanulmány kimutatta, hogy a pénisz görbülete gyakori megállapítás (38,6%) a felfújható péniszprotézis implantációs műtét idején ed prosztatarák kezelés után (3,4).
a PD kezelése koncentrált anamnézissel és fizikai vizsgálattal kezdődik. A részletes anamnézisnek értékelnie kell a betegség kialakulásával és időtartamával, a kapcsolódó traumás etiológiával, a pénisz görbületének mértékével, az erekció során bekövetkező hosszvesztéssel és a szexuális funkció szubjektív szintjével kapcsolatos információkat. Ami a szubjektív szexuális értékelést illeti, a standardizált kérdőívek, mint például az International Index of Erectile Function (IIEF) lehetővé teszik az objektív és szubjektív kezdeti értékeléseket, valamint a kezelés hatékonyságának mérésére szolgáló eszközt. Az urogenitális rendszer fizikai vizsgálatának tartalmaznia kell a pénisz hosszát, miközben feszített, plakk helyét és méretét. A görbület mértékét úgy lehet felmérni, hogy a beteg fényképeket készít a felálló falloszról, vagy vazoaktív injekciókkal kombinálva pénisz duplex Doppler ultrahanggal.
a PD természetes kórtörténetének és patogenezisének megértése fontos a megfelelő kezelési rend kiválasztásához. Míg a patofiziológia nem teljesen ismert, feltételezik, hogy a felbujtó esemény szubklinikai traumás szakadás a tunica albuginea felé. A szakadás proliferatív fibrotikus reakcióhoz vezet, ami rugalmatlan heget eredményez. A PD kezelését az akut fázisba, valamint a krónikus stabilizációs fázisba sorolják. Az akut fázis idejét lazán úgy határozzák meg, hogy kevesebb, mint 12 hónap a tünetek megjelenésétől számítva. Ez idő alatt a beteg heg folyamatosan változik. A krónikus fázist akkor határozzák meg, ha a beteg görbülete legalább 6 hónapig stabil maradt. Míg a műtéti kezelés továbbra is a PD aranystandardja, leginkább a betegség krónikus fázisában lévő férfiaknak kínálják. Az akut fázisban lévő betegek számára a farmakoterápia lehetőséget nyújt a funkció javítására, a deformitás csökkentésére és a heg progressziójának stabilizálására (5). Itt áttekintjük a PD orális kezelési lehetőségeivel kapcsolatos jelenlegi rendelkezésre álló ismereteket. Fontos megjegyezni, hogy míg egyes felsorolt ajánlások bizonyítékokon alapuló megállapításokon alapulnak, mások a szakértői véleményt tükrözik (1.táblázat).

teljes táblázat
kálium-para-amino-benxoát (POTABA)
a POTABA egy olyan vegyület, amely antifibrotikus és gyulladáscsökkentő tulajdonságairól ismert, amelyek elősegítik a fibrotikus rendellenességek, például dermatomyositis és scleroderma kezelését. Úgy gondolják, hogy hatékonysága a kollagénképződés csökkenésének köszönhető a szerotoninszint csökkentésével, a monoamin-oxidáz aktivitás növelésével és a fibroblaszt glikozaminoglikán szekréció gátlásával (6). A POTABA első javasolt alkalmazása a PD kezelésére 1959-ben volt Zarafonetis és Horrax (7). 2005-ben Weidner et al. többközpontú, randomizált, kettős vak placebo-kontrollos vizsgálatot végzett POTABA-val (51 beteg) szemben a placebóval (52 beteg) a nem kalcifikált plakkkal rendelkező NA-ban szenvedő PD betegek kezelésében. A kísérleti kar 3 g POTABÁT kapott orálisan, naponta 4 alkalommal 12 hónapig. 12 hónap elteltével a POTABA-val kezelt betegeknél jelentősen javult a pénisz plakk mérete a placebóval kezeltekhez képest. Ezenkívül a placebót kapó betegeknél a görbület romlását figyelték meg. A szerzők arra a következtetésre jutottak, hogy a POTABA segíthet a hegszövet stabilizálásában, ami megakadályozná a görbület előrehaladását (6). Nem végeztek további randomizált kontroll vizsgálatokat a POTABA hatékonyságának értékelésére. Ez talán annak mellékhatásprofiljának köszönhető, amely magában foglalja a gyomor-bélrendszeri szorongást, a hasmenést, az akut hepatitist és a hipoglikémiát (8).
E-Vitamin
az E-Vitamin, egy zsírban oldódó antioxidáns, inaktiválja a szabad gyököket, amelyek telítik a nitrogén-monoxidot (NO), ezáltal az aktív NO-szinteket megemelve, hogy lehetővé tegyék a megfelelő sebgyógyulást. Az oxidatív stressz korlátozásával potenciálisan gyulladáscsökkentő hatást is kínál. Először 1948-ban írták le a PD kezelésére (9), és alacsony költsége és rendelkezésre állása miatt továbbra is a PD leggyakrabban felírt orális szere (10). Annak ellenére, hogy az elmúlt hét évtizedben több placebo-kontrollos terv nem mutatott szignifikáns javulást a fájdalom, a görbület mértéke, a plakk mérete vagy a közösülés képessége. 1983-ban Pryor és Farrell befejezte az E-vitamin kettős-vak, placebo-kontrollos vizsgálatát 40 PD-s betegen, és nem talált szignifikáns javulást a plakk méretében vagy a pénisz görbületében (11). Továbbá egy újabb tanulmány 2007-ben Safarinejad et al. feltéve, hogy az eddigi legnagyobb próba értékelte az E-vitamint A PD szempontjából. A szerzők az E-vitamint önmagában és az L-karnitinnel kombinálva placebóval hasonlították össze 236 korai krónikus PD-ben szenvedő férfiban; olyan betegnek minősül, akinek erekció során fájdalma van, a pénisz görbülete nem zavarja a hüvelyi behatolást, nem fájdalmas tapintható heg, hiperechoikus elváltozás a pénisz ultrahangján, a meszesedés hiánya és a plakk teljes területe <2 cm2. Az 1. csoport (58 férfi) naponta kétszer 300 mg E-vitamint kapott orálisan. A 2. csoport (59 férfi) propionil-L-karnitint kapott, 1 g orálisan naponta kétszer. A 3. csoport (60 férfi) E-vitamint kapott 300 mg orálisan naponta kétszer, valamint propionil-L-karnitint 1 g orálisan naponta kétszer. Végül a 4. csoport hasonló placebót kapott a 6 hónapos próbaidőszak alatt. A kezelés után nem volt szignifikáns változás a pénisz görbületének csökkenésében a négy csoport között (P=0,9), sem a plakk méretének csökkenése (P=0,1) (12).
az E-vitamin hatékonyságát bizonyító bizonyítékok hiánya ellenére még mindig gyakran írják fel és gyakran adják be más kezelési módokkal egyidejűleg, szinergikus szerep reményében. Az E-vitamin használatának gyakori káros hatásai közé tartozik a hányinger, hányás, hasmenés és a prosztatarák és a cerebrovascularis események fokozott kockázata (13).
kolhicin
bár a kolhicin leginkább a köszvény kezeléséről ismert, olyan tulajdonságokkal is rendelkezik, amelyek segítik a PD kezelését. A kolhicin depolimerizálja a tubulint, ezáltal gátolja a sejt mitózist, a leukocita adhéziót és a kollagén transzportot. Ezt a tulajdonságot alkalmazva a kolhicinnek elméletileg csökkentenie kell a seb összehúzódását a kollagén lerakódás gátlásával (14). A kolhicint értékelő legtöbb tanulmány leírta a görbület némi javulását, de ezeket a vizsgálatokat nem randomizálták, és nem is nyújtottak objektív mérést a javulás meghatározásához. Safarinejad et al. azon kevés vizsgálatok egyikének bizonyult, amelyek a kolchicin terápiás hatásait értékelték egyetlen központ, randomizált, kettős-vak, placebo-kontrollos vizsgálat elvégzésével 84 PD-s betegen, meszes plakkok nélkül (15). A kolhicin karon lévő betegeket napi 0,5–2,5 mg kolhicinnel kezelték 4 hónapig. A vizsgálat végén a kolhicin csoport nem mutatott objektív javulást a pénisz görbületében vagy a plakk méretében. Más tanulmányok értékelték a kolchicin szinergikus hatásait az E-vitaminnal. a plakk méretének és a pénisz görbületének jelentős javulását jelentették a napi E-vitamint és kolchicint használó betegeknél az ibuprofenhez képest (16). Megjegyzendő, hogy ebben a vizsgálatban csak 45 beteg vett részt, és nem volt placebo kar. Azonban egy későbbi, 100 férfin végzett retrospektív vizsgálat nem mutatott statisztikailag szignifikáns különbséget a fájdalomcsillapítás, a pénisz görbülete vagy a plakk mérete között a kolhicin és az E-vitaminnal kombinált kolhicin között (17).
Tamoxifen
a Tamoxifen nem szteroid ösztrogénreceptor antagonista. A PD kezelésében kimutatták, hogy csökkenti a fibrogenezist a tunica albuginea-ban a fibroblasztból felszabaduló TGF-6db felszabadulásának modulálásával (18). Ralph et al. először 1992-ben javasolta a kezelést egy ellenőrizetlen vizsgálat eredményeként, amely 11 férfi közül 31-nél javította a pénisz deformitását. Ezek a megállapítások azonban nem voltak reprodukálhatók, amikor a tamoxifent egy prospektív, placebo-kontrollos vizsgálatban értékelték 25 meszes plakk nélküli PD-ben szenvedő betegen. Annak ellenére, hogy naponta kétszer 20 mg tamoxifent alkalmaztak, a fájdalom, a görbület vagy a plakk mérete nem javult jelentősen a placebóhoz képest (19).
karnitin
a karnitin az acetil-koenzim-A inhibitora, amely lehetővé teszi a szabad gyökök képződésének csökkentését a sejtstressz idején. 2001-ben Biagiotti et al. randomizált vizsgálatot végzett 96 PD beteg L-karnitinnal szemben a tamoxifennel szemben. Az eredmények jelentős péniszgörbület-javulást mutattak az L-karnitin csoportban (20). Mint már említettük, a Safarinejad 2007 4-karos vizsgálat (E-vitamin, karnitin, E-vitamin és karnitin, valamint placebo) nem mutatott jelentős javulást a pénisz görbületében, a plakk méretében vagy a fájdalomban (12).
Omega-3 zsírsav
más orális szerekhez hasonlóan az omega-3 zsírsavakat is értékelték a PD kezelésében ismert gyulladáscsökkentő tulajdonságai miatt. 2009-ben Safarinejad et al. publikálták eredményeiket egy prospektív, randomizált kettős-vak omega-3 zsírsavak versus placebo vizsgálatban. Összesen 224 korai krónikus stádiumú PD-ben szenvedő beteget randomizáltak 1 – re.84 g napi omega – 3 kiegészítés a placebóval szemben 6 hónapig. A betegeket IIEF-5-tel és PDDU-val értékelték a 6 hónapos gyógyszeres kezelés előtt és után. Sajnos nem volt jelentős javulás a plakk térfogata, a pénisz görbülete, az erekció során fellépő fájdalom és az erekciós funkció tekintetében (21). Jelenleg hiányoznak az adatok az omega-3 kiegészítés jótékony hatásának alátámasztására a PD korai-krónikus stádiumában.
prokarbazin
a prokarbazin egy alkilező kemoterápiás gyógyszer, amelyet gyakran használnak a központi idegrendszeri limfóma, Hodgkin limfóma és magas fokú gliómák kezelésére. 1968-ban Aron et al. megjegyezte a Dupuytren-kór regresszióját a Hodgkin-kór prokarbazinnal kezelt betegeknél, ezáltal arra utal, hogy a kötőszövet proliferációjával járó betegségben alkalmazzák (22). Ezzel az előfeltevéssel az 1970-es években a Bystr 6 javasolta a prokarbazint a PD kezelésére, de a későbbi vizsgálatok nem tártak fel objektív előnyöket. Ezenkívül a vizsgálatok a citotoxikus gyógyszer jelentős mellékhatásait mutatták be, és azt javasolták, hogy ne alkalmazzák a PD jóindulatú betegségében. A mellékhatások közé tartozik a myelosuppressio, a hepatotoxicitás, a fáradtság, a GI distress és a központi idegrendszeri zavar (23,24).
5-ös típusú foszfodiészteráz inhibitorok (PDE-5 inhibitorok)
bár a PDE-5 inhibitorokat általában az ED kezelésére gondolják, a legújabb vizsgálatok kimutatták annak lehetséges alkalmazását a PD kezelésében ED-vel vagy anélkül. A PDE-5 inhibitorok növelik a ciklikus guanozin-monofoszfátot (cGMP) azáltal, hogy gátolják a cGMP GMP-vé történő lebomlását. A cGMP és az NO növekedésével a kollagén szintézis és a lerakódás gátolt, és a fibroblaszt és a myofibroblast apoptózisa következik be (25). Ennek a tulajdonságnak köszönhetően a PDE-5 inhibitorok előnyösnek bizonyulhatnak a heg átalakításában. A PD patkánymodelljében a szildenafil szignifikánsan csökkentette a kollagén-fibroblaszt arányt a tunica albuginea-ban, valamint a plakk méretét (25). Chung és munkatársai tanulmányozzák a tadalafil alkalmazását a PD kezelésére humán alanyokban. Azt jelentették, hogy 2.Napi 5 mg tadalafil 6 hónapon át a septum heg megszűnését eredményezte a tapintható péniszplakk nélküli betegek 69% – ánál (24/35). A nem kezelt karnak csak 10% – a észlelte a heg felbontását. Fontos megemlíteni, hogy a septum heg nem volt klinikailag tapintható, és a legtöbb beteg ebben a vizsgálatban nem volt görbület (26). Újabban egy 2014-es tanulmány számolt be a PD-ben szenvedő betegek kezelési eredményeiről 50 mg szildenafil naponta vagy 400 NE E-vitamin 3 hónapig. 12 hét elteltével mindkét csoport a plakk térfogatának és a pénisz görbületének hasonló csökkenését mutatta, ami statisztikailag szignifikáns volt. A két csoport közötti különbségek azonban statisztikailag nem voltak szignifikánsak. A szildenafil kohorsz statisztikailag szignifikáns javulást mutatott az IIEF pontszámokban és a fájdalomcsökkenésben az E-vitaminhoz képest (27). Nagy léptékű kettős vak placebo vizsgálatot kell végezni, és validálni kell a PDE-5 inhibitor klinikai előnyeit, de a jelenlegi kutatások ígéretesek (2.táblázat).
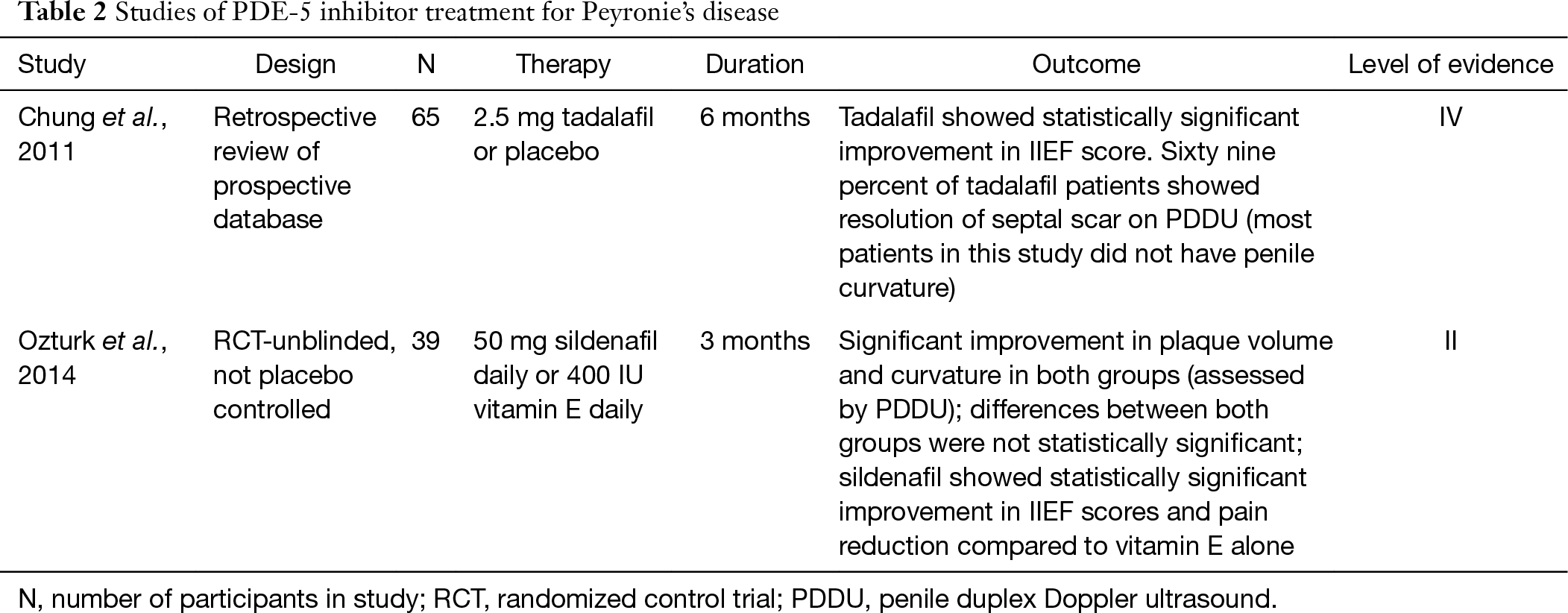
teljes táblázat
L-arginin
az L-arginin egy NO-prekurzor, amely stimulálja a NO-szintázt. Ez a NO növekedését, valamint az apoptózis miatti fibroblaszt csökkenését okozza. Úgy gondolják, hogy ez a két tulajdonság az L-arginin, mint antifibrotikus szer mögött álló mechanizmus (25). Mint már említettük, Valente et al. PDE-5 inhibitorokkal kezelt patkánymodellekben, De l-argininnel is értékelték a péniszplakkokat. Hasonlóan a PDE-5 inhibitorokhoz, az L-arginin szignifikánsan csökkentette a plakk méretét, valamint a kollagén-fibroblaszt arányt (25). Egy későbbi tanulmány szerint Medeiros et al. kimutatták, hogy az arginin védő hatással is rendelkezik a hegszövet kialakulása ellen, amikor a patkányok péniszét kismedencei sugárzásnak vetik alá (28). 2012-ben Abern et al. megfigyelték a görbület javulásának tendenciáját a PD-ben szenvedő betegeknél, akiket intralesionális verapamillal, orális L-argininnel és orális pentoxifillinnel (PTX) együtt kezeltek penis traction terápiával (29). Míg ez a tanulmány számos változóval rendelkezik, amelyek hozzájárulhatnak a görbület javulásához, ez egyike azon kevés emberi kísérleteknek, amelyekben az L-arginint alkalmazták a PD kezelésére. Tekintettel ezekre az eredményekre, az L-arginin értékes kezelési lehetőségnek bizonyulhat a PD számára, de további humán vizsgálatokra van szükség.
pentoxifillin (PTX)
bár a PD kezelésére vizsgált orális gyógyszerek többsége gyenge vagy meghatározatlan eredményeket mutatott kontrollált vizsgálatokban, a PTX sokkal jobban teljesített. A PTX egy xantinszármazék, amely nem specifikus foszfodiészteráz inhibitorként működik, ismert gyulladáscsökkentő és anti-fibrogén tulajdonságokkal (30). A PD kezelésére egy in vitro vizsgálat alapján javasolták, amely kimutatta, hogy megakadályozza a tunica albuginea fibroblaszt proliferációját, csökkenti a TGF-B által közvetített kollagén lerakódást, csökkenti az elasztin lerakódását és növeli a fibrinolitikus aktivitást (31-33). Ezeket a tulajdonságokat figyelembe véve egy 2010-es kettős vak, placebo-kontrollos vizsgálat igyekezett meghatározni a PTX hatását korai krónikus PD-ben szenvedő betegeknél (30). Kétszáz huszonnyolc beteget randomizáltak, hogy 400 mg ptx tartós felszabadulást kapjanak a placebóval szemben 6 hónapig. A legtöbb résztvevő legalább egy korábbi PD-kezelés sikertelen volt. A placebo csoportban 4-szer nagyobb volt a betegség progressziójának valószínűsége (42%) a kezelési karhoz képest (11%). Továbbá, a PTX csoport szignifikáns javulást mutatott mind az objektív, mind a szubjektív mérésekben; (I) a pénisz görbületének javulása duplex ultrahanggal mérve a prosztaglandin E1 tizedes injekció előtt és után; (II) plakktérfogat és (III) IIEF pontszámok (30). Újabb vizsgálatok értékelték orális PTX együtt orális antioxidánsok, intralesional PTX és intralesional verapamil változó eredmények (34,35). Míg a PTX továbbra is erős versenytársa a PD-kezelésnek, további nagy, többközpontú kísérleteket kell lezárni annak biztosítása érdekében, hogy az eredmények reprodukálhatók legyenek (3.táblázat).

teljes táblázat
következtetések
a több évtizedes PD-kutatás ellenére a végleges etiológiát és patofiziológiát nem sikerült teljesen tisztázni. Míg a műtéti terápia továbbra is a krónikus súlyos PD arany standardja, számtalan más kevésbé invazív kezelési lehetőség létezik, nevezetesen orális és intralesionális gyógyszerek. Itt áttekintettük a PD kezelésére leggyakrabban felírt vagy megvitatott orális szereket. Bár számos jól megtervezett tanulmány pozitív válaszokat fedezett fel orális gyógyszerekkel, kis mintaméretük korlátozza a vizsgálat erejét és reprodukálhatóságát. Jelenleg az Amerikai Urológiai Szövetség irányelvei az állami klinikusok nem ajánlhatnak orális terápiát E-vitaminnal, tamoxifennel, omega-3 zsírsavval vagy E-vitamin L-karnitinnel történő kombinációjával. Hasonlóképpen, a Szexuális orvoslásról szóló 2010. évi nemzetközi konzultáció nem támogatta az orális szerek rutinszerű klinikai alkalmazását a PD számára (5). Két orális gyógyszer, amelyet az irányelvek nem korlátoznak, a PDE-5 inhibitorok és a PTX. További kutatásokra van szükség a PDE-5 és a PTX területén, beleértve a nagy multi center kettős vak, randomizált kontroll vizsgálatokat is, hogy meghatározzák hatékonyságukat. Mindkét gyógyszerosztály reményt ad a PD kezelésére engedélyezett orális gyógyszerek hiányára.
Köszönetnyilvánítás
Nincs.
lábjegyzet
összeférhetetlenség: a szerzőknek nincs összeférhetetlenségük.
- Mulhall JP, Creech SD, Boorjian SA, et al. A Peyronie-kór prevalenciájának szubjektív és objektív elemzése a prosztatarák szűrésére jelentkező férfiak populációjában. J Urol 2004;171: 2350-3.
- Mulhall JP, Schiff J, Guhring P. a Peyronie-kór természetes történetének elemzése. J Urol 2006;175: 2115-8; vita 2118.
- Tal R, Heck M, Teloken P, et al. Peyronie-betegség radikális prostatectomia után: incidencia és prediktorok. J Szex Med 2010; 7: 1254-61.
- Lin H, Alba F, Romero C, et al. 1815 a pénisz görbülete gyakori megállapítás a péniszprotézis beültetésénél a merevedési zavarban szenvedő betegeknél radikális prosztatektómia után. J Urol 2011;185:e728-e729.
- Ralph D, Gonzalez-Cadavid N, Mirone V, et al. A Peyronie-kór kezelése: bizonyítékokon alapuló 2010-es Irányelvek. J Szex Med 2010; 7: 2359-74.
- Weidner W, Hauck EW, Schnitker J, et al. Kálium-paraaminobenzoát (POTABA) Peyronie-kór kezelésében: prospektív, placebo-kontrollos, randomizált vizsgálat. Eur Urol 2005;47: 530-5; vita 535-6.
- Zarafonetis CJ, Horrax TM. Peyronie-betegség kezelése kálium-para-amino-benzoáttal (potaba). J Urol 1959; 81: 770-2.
- Roy J, Carrier S. akut hepatitis, amely a Peyronie-betegség kálium-para-amino-benzoáttal (Potaba) történő kezelésével jár. J Szex Med 2008; 5:2967-9.
- Scott WW, Scardino pl. Új koncepció a Peyronie-kór kezelésében. Dél-Med J 1948;41: 173-7.
- Levine LA, Burnett AL. A Peyronie-kór szokásos működési eljárásai. J Szex Med 2013; 10:230-44.
- Pryor JP, Farrell vö. Az E-vitamin kontrollált klinikai vizsgálata Peyronie-kórban. Prog Reprod Biol 1983; 9: 41-5.
- Safarinejad MR, Hosseini SY, KOLAHI AA. Az E-vitamin és a propionil-L-karnitin összehasonlítása külön-külön vagy kombinációban korai krónikus Peyronie-betegségben szenvedő betegeknél: kettős-vak, placebo-kontrollos, randomizált vizsgálat. J Urol 2007;178:1398-403; vita 1403.
- Klein EA, Thompson IM Jr, Tangen CM, et al. E-Vitamin és a prosztatarák kockázata: a szelén és az E-Vitamin Rákmegelőzési vizsgálata (SELECT). JAMA 2011; 306: 1549-56.
- el-Sakka AI, Bakircioglu ME, Bhatnagar RS, et al. A kolchicin hatása Peyronie-szerű állapotra egy állatmodellben. J Urol 1999;161: 1980-3.
- Safarinejad Mr.a kolchicin terápiás hatásai a Peyronie-kór kezelésében: randomizált kettős-vak, placebo-kontrollos vizsgálat. Int J Impot Res 2004;16:238-43.
- Prieto Castro RM, Leva Vallejo ME, Regueiro Lopez JC, et al. Kombinált kezelés E-vitaminnal és kolchicinnel a Peyronie-betegség korai szakaszában. BJU Int 2003; 91: 522-4.
- Cortex Xhams-Gonz Xhamsterlez JR, Glina S. Peyronie-betegség konzervatív kezelése: kolchicin vs.kolchicin plusz E-vitamin Actas Urol Esp 2010;34:444-9.
- Ralph DJ, Brooks MD, Bottazzo GF, et al. A Peyronie-betegség kezelése tamoxifennel. Br J Urol 1992; 70: 648-51.
- Teloken C, Rhoden EL, Grazziotin TM, et al. Tamoxifen versus placebo a Peyronie-kór kezelésében. J Urol 1999;162: 2003-5.
- Biagiotti G, Cavallini G. acetil-L-karnitin vs tamoxifen a Peyronie-betegség orális terápiájában: előzetes jelentés. BJU Int 2001; 88: 63-7.
- Safarinejad Mr.az omega-3 hatásossága és biztonságossága a korai stádiumú Peyronie-kór kezelésében: prospektív, randomizált, kettős-vak placebo-kontrollos vizsgálat. J Szex Med 2009; 6: 1743-54.
- Aron E. a Dupuytren-kór citosztatikus szerrel (metilhidrazin) történő orvosi kezelése. Presse Med 1968; 76: 1956.
- Bystr D. O., Johansson B., Edsmyr F., et al. Induratio pénisz plastica (Peyronie-betegség). A kezelés különböző formáinak eredményei. Scand J Urol Nephrol 1972; 6: 1-5.
- Oosterlinck W, teszi G. Peyronie-betegség kezelése prokarbazinnal. Br J Urol 1975;47: 219-20.
- Valente EG, Vernet D, Ferrini MG, et al. Az L-arginin és a foszfodiészteráz (PDE) gátlók ellensúlyozzák a fibrózist a Peyronie fibrotikus plakkjában és a kapcsolódó fibroblaszt tenyészetekben. Nitrogén-Oxid 2003; 9: 229-44.
- Chung E, Deyoung L, Brock GB. A PDE5 inhibitorok szerepe a pénisz septum heg átalakításában: a klinikai és radiológiai eredmények értékelése. J Szex Med 2011;8: 1472-7.
- Ozturk U, Yesil S, Goktug HN, et al. A szildenafil kezelés hatása Peyronie-betegségben szenvedő és merevedési zavarban szenvedő betegekre. Ir J Med Sci 2014;183: 449-53.
- Medeiros Jl Jr, Costa WS, Felix-Patricio B, et al. Az argininnel és glutaminnal történő táplálékkiegészítés védő hatása a kismedencei sugárzásnak kitett patkányok péniszére. Andrológia 2014;2: 943-50.
- Abern MR, Larsen S, Levine LA. A pénisz vontatásának, az intralesionális verapamilnak és a Peyronie-betegség orális terápiáinak kombinációja. J Szex Med 2012; 9:288-95.
- Safarinejad MR, Asgari MA, Hosseini sy, et al. Kettős-vak, placebo-kontrollos vizsgálat a pentoxifillin hatásosságáról és biztonságosságáról korai krónikus Peyronie-betegségben. BJU Int 2010;106:240-8.
- Raetsch C, Jia JD, Boigk G, et al. A pentoxifillin csökkenti a profibrogén citokinek és a procollagen I expresszióját patkány másodlagos epefibrózisában. Gut 2002; 50: 241-7.
- l, Vandenbussche P, Crusiaux A, Et al. A pentoxifillin differenciális hatása a tumor nekrózis faktor-alfa (TNF-alfa) és az interleukin-6 (IL-6) monociták és T-sejtek általi termelésére. Immunológia 1992; 76: 30-4.
- Shindel AW, Lin G, Ning H, et al. A pentoxifillin csillapítja a transzformáló növekedési faktort-61-stimulált kollagén lerakódást és elasztogenezist humán tunica albuginea eredetű fibroblasztokban 1. rész: hatás az extracelluláris mátrixra. J Szex Med 2010; 7: 2077-85.
- Paulis G, Barletta D, Turchi P, et al. A pentoxifillin hatásosságának és biztonságosságának értékelése más antioxidánsokkal összefüggésben a Peyronie-kór orvosi kezelésében: esettanulmány. Res Rep Urol 2015; 8: 1-10.
- Alizadeh M, Karimi F, Fallah Mr.a verapamil hatékonyságának értékelése Peyronie-betegségben, összehasonlítva a pentoxifillinnel. Glob J Egészségügyi Sci 2014; 6: 23-30.
- Smith JF, Shindel AW, Huang YC, et al. Pentoxifillin kezelés és a pénisz meszesedése Peyronie-betegségben szenvedő férfiaknál. Ázsiai J Androl 2011;13: 322-5.