a bizonyíték mögött természetes beavatkozások alkoholmentes zsírmáj betegség: növényekkel, tápanyagokkal és probiotikumok kezelésére ez a közös betegség
mivel a nő az alkoholmentes zsírmáj betegség (NAFLD) mind a felnőttek és a gyermekgyógyászat és a hiányzó jelzett gyógyszerészeti kezelés,, természetes stratégiák kezelésére ez a feltétel állni jól lebeg, mint a “következő legjobb dolog.”Számos táplálékkiegészítőt és növényi anyagot tanulmányoztak klinikailag, és ígéretet mutatnak a NAFLD és gyulladásos megfelelője, az alkoholmentes steatohepatitis (NASH) kezelésére. Tekintettel arra, hogy ezek közül a terápiák közül hány foglalkozik a NAFLD kialakulásához hozzájáruló tényezőkkel, nem kell sok érvelés ahhoz, hogy megértsük, hogyan lehet hatékonyan kezelni a betegség néhány kiváltó okát, ahelyett, hogy csak egy tünetet kezelnének.
öt kiegészítő beavatkozás, amelyek klinikai vagy epidemiológiai bizonyítékokkal szolgálnak a NAFLD beállítására, a foszfatidil-kolin, amely foszfolipideket és kolint, E-vitamint biztosít, mind alfa-tokoferolként, mind delta-és gamma-tokotrienolok keverékeként, bogáncsmag-kivonat, berberin és probiotikumok.
- zsíros májváltozások: korrelál a foszfatidil-kolin hiányával?
- E-Vitamin
- máriatövis
- berberin
- probiotikumok
- következtetés
- Dr. Carrie Decker, ND kitüntetéssel diplomázott a National College of Natural Medicine (ma a National University of Natural Medicine) Portland, Oregon. Dr. Decker távolról látja a betegeket, különös tekintettel a gyomor-bélrendszeri betegségekre, a hangulati egyensúlyhiányra, az étkezési rendellenességekre, az autoimmun betegségekre és a krónikus fáradtságra. Mielőtt naturopátiás orvos lett volna, Dr. Decker mérnök volt, és biomedicinális és gépészmérnöki diplomát szerzett a Wisconsin-Madison Egyetemen és az Illinois Egyetemen az Urbana-Champaign-ban. Dr. Decker továbbra is élvezi a tudományos kutatást és az írást, és ezeket a készségeket használja az integratív Orvostudományi oktatás támogatására íróként és különböző források közreműködőjeként. Dr. A Decker támogatja az allergia kutatócsoportot oktatási és termékfejlesztő csapatuk tagjaként.
- források:
- Spengler EK, Loomba R. ajánlások a nem alkoholos zsírmájbetegség és az alkoholmentes steatohepatitis diagnosztizálására, májbiopsziára történő áttételre és kezelésére. Mayo Klinika Eljárás. 2015;90(9):1233–1246.
- Berardis S, Sokal E. gyermek alkoholmentes zsírmájbetegség: növekvő közegészségügyi kérdés. Eur J Pediatr. 2014 február;173(2): 131-9.
- Jadeja R, et al. Növényi gyógyszerek alkoholmentes steatohepatitis kezelésére: jelenlegi forgatókönyv és jövőbeli kilátások. Evid Alapú KOMPLEMENT Alternat Med. 2014:648308.
- Pomorski T, et al. Lipid Eloszlás és transzport a sejtmembránokon keresztül. Semin Sejt Dev Biol. 2001 ápr.; 12(2): 139-48.
- Yamaji-Hasegawa A, et al. A foszfolipidek aszimmetrikus eloszlása a biomembránokban. Biol Pharm Bika. 2006. augusztus;29(8): 1547-53.
- Helló, M. A., et al. Epeúti lipid szekréció. Turk J Gastroenterol. 2007. június;18(2): 65-70.
- Fischer LM, et al. A szex és a menopauzális állapot befolyásolja az emberi táplálkozási igényeket a tápanyag kolin számára. Én J Clin Nutr Vagyok. 2007 május; 85(5): 1275-85.
- Wallace TC, et al. A szokásos Kolinbevitel az Egyesült Államokban a tojás-és Fehérjefogyasztáshoz kapcsolódik. Tápanyagok. 2017 augusztus 5; 9(8).
- Zeisel SH. A génválasz elemek, a genetikai polimorfizmusok és az epigenetika befolyásolják a kolin emberi étrendi igényét. IUBMB élet. 2007. június;59(6): 380-7.
- Zeisel SH. A génválasz elemek, a genetikai polimorfizmusok és az epigenetika befolyásolják a kolin emberi étrendi igényét. IUBMB élet. 2007. június;59(6): 380-7.
- Guerrerio AL, et al. Kolinbevitel nem alkoholos zsírmájbetegségben szenvedő betegek nagy csoportjában. Én J Clin Nutr Vagyok. 2012 ápr.; 95(4): 892-900.
- Ma X, et al. A polienil-foszfatidilkolin csillapítja az alkoholmentes májfibrózist és felgyorsítja annak regresszióját. J Hepatol. 1996 május;24(5): 604-13.
- Lieber CS, et al. A foszfatidilkolin védi a pávián fibrózisát és cirrhosisát. Gasztroenterológia. 1994 január;106(1): 152-9.
- Chanussot F, et al. A ciklosporin A által kiváltott intrahepatikus kolesztázis étrendi (n-6) többszörösen telítetlen foszfatidil-kolinokkal történő megelőzése állatokban. Élet Sci. 2003 június 13;73(4): 381-92.
- Karaman a, et al. A többszörösen telítetlen foszfatidilkolin védő hatása patkányokban az epeelzáródás által kiváltott májkárosodásra. J Pediatr Surg. 2003 Szeptember;38(9): 1341-7.
- Karaman a, et al. A többszörösen telítetlen foszfatidilkolin védő hatása patkányokban az epeelzáródás által kiváltott májkárosodásra. J Pediatr Surg. 2003 Szeptember;38(9): 1341-7.
- Stremmel W, et al. A nyálkahártya védelme foszfatidilkolin által. Dig Dis. 2012; 30 Suppl 3: 85-91.
- Parlesak a, et al. A konjugált primer epesók csökkentik az endotoxin permeabilitását a bélhámsejteken keresztül, és szinergizálnak a foszfatidilkolinnal a gyulladásos citokin termelés elnyomásában. Crit Care Med. 2007. október;35(10): 2367-74.
- Mitzscherling K, et al. A foszfatidilkolin visszafordítja a transzepithelialis endotoxin permeabilitás etanol által kiváltott növekedését, és megszünteti a transzepithelialis leukocyta aktivációt. Alkohol Clin Exp Res. 2009 Márc; 33(3): 557-62.
- Buzzetti E, et al. Az alkoholmentes zsírmájbetegség (NAFLD) többszörös patogenezise. Anyagcsere. 2016 augusztus;65(8):1038-48.
- El Hadi h, et al. E-Vitamin, mint alkoholmentes zsírmájbetegség kezelése: valóság vagy mítosz? Antioxidánsok (Bázel). 2018 január 16; 7(1).
- Bugianesi E, et al. A metformin randomizált, kontrollált vizsgálata az E-vitaminnal vagy az előíró étrenddel szemben alkoholmentes zsírmájbetegségben. Am J Gastroenterol. 2005 május;100(5): 1082-90.
- Sanyal AJ, et al. Pioglitazon, E-vitamin vagy placebo alkoholmentes steatohepatitis esetén. N Engl J Med. 2010 május 6; 362(18): 1675-85.
- Lavine JE. E-Vitamin nem alkoholos steatohepatitis kezelése gyermekeknél: kísérleti tanulmány. J Pediatric. 2000 június;136(6): 734-8.
- Peh HY, et al. E-Vitamin terápia a rákon túl: tokoferol versus tokotrienol. Pharmacol Ther. 2016. június;162: 152-69.
- Qureshi AA, et al. A lipidparaméterek, a citokinek és az RNS dózisfüggő modulációja delta-tokotrienol által hiperkoleszterinémiás alanyokban, akik az AHA 1. lépéses étrendre korlátozódtak. Brit J Med & Med res. 2015; 6(4): 351-66.
- Qureshi AA, et al. A delta-tokotrienol hatása a gyulladásos biomarkerekre és az oxidatív stresszre hiperkoleszterinémiás betegeknél. Clin Exp Kardiológia. 2015;6(4):1000367.
- Zaiden N, et al. A Gamma-delta tokotrienolok csökkentik a máj trigliceridszintézisét és VLDL szekrécióját. J Atheroscler Thromb. 2010 ott 27;17(10): 1019-32.
- Magosso E, et al. Tokotrienolok a máj echogén válaszának normalizálására alkoholmentes zsírmájban: randomizált, placebo-kontrollos klinikai vizsgálat. Nutr J. 2013 Dec 27;12(1): 166.
- Pervez MA, et al. A Delta-tokotrienol kiegészítés hatása májenzimekre, gyulladásra, oxidatív stresszre és máj steatosisra alkoholmentes zsírmájbetegségben szenvedő betegeknél. Turk J Gastroenterol. 2018 márc;29(2):170-176.
- Abenavoli L, et al. Tejes bogáncs májbetegségekben: múlt, jelen, jövő. Phytother Res. 2010 Október;24(10): 1423-32.
- Valenzuela a, et al. A szilimarin szelektivitása a patkány különböző szöveteiben a GSH-tartalom növekedésére. Planta Med. 1989. október;55(5): 420-2.
- Rui YC. A szilimarin farmakológiai vizsgálatainak előrehaladása. Mem Inst Oswaldo Cruz. 1991; 86 Suppl 2:79-85.
- Gu M, et al. A szilimarin a Farnesil X Receptor aktiválásával enyhíti az étrend által kiváltott elhízással járó metabolikus diszfunkciót. Első Pharmacol. 2016 szeptember 28; 7: 345.
- Ali AH, et al. A farnesoid X receptor agonisták fejlődésének legújabb fejleményei. Ann Transl Med. 2015 január;3(1): 5.
- Traussnigg S, et al. A nem szteroid farnesoid x receptor agonista px-104 hatásossága és biztonságossága alkoholmentes zsírmájbetegségben (NAFLD) szenvedő betegeknél. Zeitschrift F .. Gastroenterologie. 2017 Május;55(05): A71.
- Zhong S, et al. A szilimarin terápiás hatása nem alkoholos zsírbetegség kezelésében: randomizált kontroll vizsgálatok metaanalízise (PRISMA). Orvostudomány (Baltimore). 2017 Dec;96(49): e9061.
- Hajiaghamohammadi AA, et al. A metformin, a pioglitazon és a szilimarin kezelés hatása az alkoholmentes Zsírmájbetegségre: randomizált, kontrollált kísérleti vizsgálat. Hepat Mon. 2012 augusztus;12(8): e6099.
- Birdsall TC, et al. Berberin: számos gyógynövényben található alkaloid terápiás potenciálja. Altern Med Rev. 1997; 2:94-103.
- Imanshahidi M, et al. A Berberis vulgaris és aktív alkotóeleme, a berberin farmakológiai és terápiás hatásai. Phytother Res. 2008 Augusztus;22(8): 999-1012.
- Zhu X, et al. A berberin lehetséges mechanizmusai az alkoholmentes zsírmájbetegség kezelésében. Molekulák. 2016 ott 14; 21(10).
- Lan J, et al. A berberin hatásának és biztonságosságának metaanalízise 2-es típusú diabetes mellitus, hiperlipémia és magas vérnyomás kezelésében. J Ethnopharmacol. 2015 február 23;161: 69-81.
- Sun R, et al. Az orálisan alkalmazott berberin a mikrobiális epesav metabolizmus és a bél FXR jelátviteli útvonalának megváltoztatásával modulálja a máj Lipid metabolizmusát. Mol Pharmacol. 2017 február;91(2): 110-122.
- Guo T és munkatársai. A berberin enyhíti a máj steatosisát és elnyomja a máj és a zsírszövet gyulladását az étrend által kiváltott elhízásban szenvedő egerekben. Sci Rep. 2016 Elront 3; 6: 22612.
- Schattenberg JM, et al. A JNK1, de nem a JNK2 elősegíti a steatohepatitis kialakulását egerekben. Hepatológia. 2006 január;43(1): 163-72.
- Han J, et al. A bél mikrobiotájának modulálása, mint a berberin antidiabetikus mechanizmusa. Med Sci Monit. 2011;17: RA164-7.
- Gu L, et al. Az endotoxinémia egérmodelljében a berberin enyhíti a bél epithelialis szűk csomópont károsodását és lefelé szabályozza a miozin könnyű lánc kináz útvonalait. J Infect Dis. 2011. június 1.; 203(11): 1602-12.
- Li n, et al. A berberin gyengíti a gyulladásgátló citokin által kiváltott szoros kapcsolódási zavarokat a bélhámsejtek in vitro modelljében. Eur J Pharm Sci. 2010 ápr 16;40(1):1-8.
- Ma X, et al. A Diabetes mellitus patogenezise oxidatív stressz és gyulladás révén: berberin általi gátlása. Első Pharmacol. 2018 július 27; 9: 782.
- Yan HM, et al. A berberin hatékonysága alkoholmentes zsírmájbetegségben szenvedő betegeknél. PLoS Egy. 2015 augusztus 7;10 (8): e0134172.
- Ma YY, et al. A probiotikumok hatása az alkoholmentes zsírmájbetegségre: metaanalízis. Világ J Gastroenterol. 2013 ott 28;19(40): 6911-8.
- Vajro P, et al. A Lactobacillus rhamnosus törzs GG hatása gyermekkori elhízással összefüggő májbetegségben. J Pediatr Gastroenterol Nutr. 2011. június;52(6): 740-3.
- Alisi a, et al. Randomizált klinikai vizsgálat: a VSL # 3 jótékony hatásai elhízott, alkoholmentes steatohepatitisben szenvedő gyermekeknél. Aliment Pharmacol Ther. 2014. június; 39(11): 1276-85.
- P Enterprez-Rubio KG, et al. A berberin alkalmazásának hatása a metabolikus szindrómára, az inzulinérzékenységre és az inzulinszekrécióra. Metabolit Syndr Relat Disord. 2013 ott;11(5): 366-9.
- Iacono a, et al. A probiotikumok, mint a NAFLD kezelésének feltörekvő terápiás stratégiája: a molekuláris és biokémiai mechanizmusokra összpontosít. J Nutr Biochem. 2011 augusztus;22(8): 699-711.
- Honda Y, et al. A glutation hatékonysága alkoholmentes zsírmájbetegség kezelésében: nyílt, egykarú, multicentrikus, kísérleti vizsgálat. BMC Gastroenterol. 2017 augusztus 8;17(1): 96.
- Dentico P, et al. . Recenti Prog Med. 1995. Július-Augusztus; 86(7-8): 290-3.
- Khoshbaten M, et al. Az N-acetil-cisztein javítja a májfunkciót alkoholmentes zsírmájbetegségben szenvedő betegeknél. Hepatitis Mon. 2010;10(1):12-16.
- Muto C, et al. A Gamma-tokotrienol csökkenti a triacil-glicerin szintet patkány primer hepatocitákban a zsírsav-metabolizmus szabályozása révén. J Clin Biochem Nutr. 2013;52(1):32-37.
- Parker HM, et al. Omega-3 kiegészítés és alkoholmentes zsírmájbetegség: szisztematikus áttekintés és metaanalízis. J Hepatol. 2012;56(4):944-51.
zsíros májváltozások: korrelál a foszfatidil-kolin hiányával?
a foszfatidil-kolin (PC) elengedhetetlen a test összes sejtjének egészségéhez, és az egyik legfontosabb foszfolipid, amelyből a sejtmembránok állnak. A PC az epe teljes foszfolipid tartalmának több mint 90% – át teszi ki, és elősegíti a zsír emulgeálódását, felszívódását és szállítását. Tanulmányok kimutatták, hogy a kolin ajánlott megfelelő bevitele (AI) (lásd az 1.táblázatot) nem elegendő a hiány tüneteinek, például a zsírmáj változásainak vagy az izomkárosodásnak a megelőzéséhez. Ezenkívül egy nemrégiben készült tanulmány megállapította, hogy az amerikai felnőtteknek csak 8% – A felel meg a kolin ajánlott AI-jának, a vegetáriánusok, a posztmenopauzás nők és a férfiak esetében a legnagyobb az elégtelenség kockázata., A genetikai polimorfizmusok szintén növelhetik a kolin iránti igényt, amely szintén a metilcsoportok forrása a szervezetben.
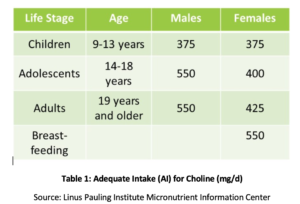
NAFLD-ben szenvedő posztmenopauzás nőknél a csökkent kolinbevitel szignifikánsan összefügg a fibrózis fokozott kockázatával. Állatokban kimutatták, hogy a PC véd a májgyulladással járó fibrózis ellen., Kimutatták, hogy a PC fokozott bevitele fokozza az epe lipid szekrécióját, ezáltal megakadályozza a kolesztázist és az azt követő májkárosodást számos mechanizmus révén, beleértve a nukleáris faktor elnyomását kappa B (NF-kB), a gyulladás jól ismert molekuláris kiváltója., Az epeutak elzáródásának állatmodelljében kimutatták, hogy a kiegészítő PC csökkenti a májkárosodást, a ductalis proliferációt és a fibrózist.
a PC a bél egészségének szempontjából is nélkülözhetetlen, és a védő bélnyálkahártya elsődleges összetevője. Sejttenyészetekben kimutatták, hogy a PC-vel végzett kezelés csökkenti az endotoxin migrációját a bél hámsejtjein keresztül, tovább elnyomva a kapcsolódó gyulladásos citokinválaszt. A PC csökkenti az endotoxin transzlokációt az alkohol által kiváltott béláteresztő képesség növekedésének hátterében is. Ezt a jótékony hatást javasolták az egyik mechanizmusként, amellyel a PC terápiásnak tekinthető alkoholos májbetegségben.
E-Vitamin
mivel az oxidatív stressz hatása és a csökkent antioxidáns védelem a NAFLD kialakulását vezető tényezőként javasolt, nem meglepő, hogy az antioxidánsokat az állapot lehetséges kezelésére vizsgálták.
 az E-vitamint számos klinikai vizsgálatban tanulmányozták a NAFLD kezelésére, mind önálló, mind kiegészítő terápiaként. E vizsgálatok áttekintése során az E-vitamin dózisa 400 és 1200 NE/nap között volt, a vizsgálat időtartama pedig 24 hét és több mint két év között volt. Az eredmények általában pozitívak voltak, ami azt mutatja, hogy amikor az E-vitamint bevonták, javultak a szövettan, a steatosis és/vagy a transzamináz szintek., A NAFLD-vel végzett gyermekgyógyászatban az E-vitamint terápiaként is tanulmányozták. Egy nyílt elrendezésű kísérleti vizsgálatban, amelyben 11 NAFLD-ben szenvedő gyermek vett részt, 400-1200 NE E-vitamin pótlása négy-tíz hónapon keresztül normalizálta a transzamináz és az alkalikus foszfatáz szintjét a kezelés alatt, azonban a kezelés abbahagyása után visszatértek abnormális állapotba. A máj echogenitása a kezelés során nem változott.
az E-vitamint számos klinikai vizsgálatban tanulmányozták a NAFLD kezelésére, mind önálló, mind kiegészítő terápiaként. E vizsgálatok áttekintése során az E-vitamin dózisa 400 és 1200 NE/nap között volt, a vizsgálat időtartama pedig 24 hét és több mint két év között volt. Az eredmények általában pozitívak voltak, ami azt mutatja, hogy amikor az E-vitamint bevonták, javultak a szövettan, a steatosis és/vagy a transzamináz szintek., A NAFLD-vel végzett gyermekgyógyászatban az E-vitamint terápiaként is tanulmányozták. Egy nyílt elrendezésű kísérleti vizsgálatban, amelyben 11 NAFLD-ben szenvedő gyermek vett részt, 400-1200 NE E-vitamin pótlása négy-tíz hónapon keresztül normalizálta a transzamináz és az alkalikus foszfatáz szintjét a kezelés alatt, azonban a kezelés abbahagyása után visszatértek abnormális állapotba. A máj echogenitása a kezelés során nem változott.
a tokotrienolok az E-vitamin természetben előforduló formáinak kevésbé tanulmányozott családja, a tokoferolok, amelyek gyakrabban találhatók a természetben, uralják a tudományos kutatást. A tokotrienolok azonban erős antioxidánsok,egyes kutatások szerint a tokoferolok antioxidáns potenciáljának 40-60-szorosa. A tokotrienolokról kimutatták, hogy javítják az összkoleszterint és frakcióit, csökkentve az ÖSSZKOLESZTERINT és az LDL-koleszterint 15-20% – kal, a triglicerideket pedig csaknem 30% – kal. A tokotrienolokról kimutatták, hogy in vivo gyulladáscsökkentő és antioxidáns hatásúak, csökkentik a nagy érzékenységű C-reaktív fehérje (hs-CRP) szintjét és csökkentik az LDL oxidációját.
a Tokotrienolokat a NAFLD kezelésére is tanulmányozták. Ultrahanggal diagnosztizált NAFLD-ben szenvedő betegeknél 200 mg kevert tokotrienol (pálmaolajból származik, magas gamma-frakcióval és további 61 mg alfa-tokoferollal) naponta kétszer, egy éven keresztül, szignifikánsan normalizálta a hepatikus echogén választ és a remisszió arányát a placebóhoz képest. Egy második vizsgálatban, amelyben ultrahanggal diagnosztizált NAFLD-vel és transzaminázszint emelkedéssel rendelkező betegek vettek részt, 300 mg tokotrienol (90:10 delta:gamma keverék) naponta kétszer 12 héten keresztül, szignifikánsan csökkentette az aszpartát-aminotranszferáz (AST), az alanin-aminotranszferáz (ALT), a hs-CRP és a malondialdehid (az oxidatív stressz markere) szintjét, valamint a zsírmáj index pontszámát a placebóhoz képest.
máriatövis
máriatövis (Silybum marianum) talán a legismertebb májvédő botanikai. A szilimarin, a tejcsíra aktív összetevőinek keveréke, és a szilibinin, a benne található legaktívabb vegyület, állatkísérletekben kimutatták, hogy csökkenti az acetaminofen, az alkohol, a vas túlterhelés és a sugárzás által okozott májkárosodást más ismert máj mérgező anyagok között. Kimutatták, hogy a szilimarin növeli a glutation, egy erős antioxidáns szintjét mind a májban, mind a belekben. Csökkenti a lipidperoxidációt is, amely károsítja a sejtmembránokat, megváltoztatja azok működését, és esetleg sejthalált okoz.
szilibinin és szilimarin kimutatták, hogy aktiválja a nukleáris epesav receptor ismert farnesoid X receptor (FXR) a májban, lefelé szabályozó gyulladásos utak és korrigáló inzulinrezisztencia és diszlipidémia által kiváltott magas zsírtartalmú étrend (HFD) etetés. Az FXR az epesav, a glükóz és a lipid egyensúly kulcsfontosságú szabályozója a szervezetben. Az FXR-rel hasonló módon kölcsönhatásba lépő gyógyszereket is vizsgálják a NAFLD kezelésére és a kapcsolódó metabolikus kihívásokra.
klinikai vizsgálatok azt is kimutatták, hogy a bogáncs javítja a NAFLD-vel kapcsolatos különböző paramétereket. Egy 2017-es metaanalízis megállapította, hogy a máriatövis-kezelés szignifikánsan csökkenti az ALT-ot és az AST-t -5,08 NE/L-rel, illetve -5,44 NE/L-rel a NAFLD-ben szenvedő betegeknél. Az adagok a napi egyszeri 140 mg-tól a napi háromszor 200 mg-ig terjedtek, 8-24 hétig. A legalacsonyabb napi 140 mg-os adag mellett, 8 hét elteltével az éhomi vércukorszint (FBG), a lipidprofil és a szérum inzulinszintek jelentős javulását figyelték meg az AST és az ALT 56-ról 37-re történő csökkentése mellett.77 NE/L, illetve 78, 73-53, 05 NE/L.
berberin
a berberin, az Orangis-sárga alkaloid, amely megtalálható a botanikai növényekben, mint például az Oregoni szőlőgyökér és kéreg, a goldenseal és a borbolya, egy másik botanikai eredetű anyag, amely számos mechanizmussal rendelkezik, amelyek segíthetnek a NAFLD elleni védelemben és a felbontás támogatásában.,,
a berberin antidiabetikus és lipidegyensúlyozó hatását számos klinikai vizsgálatban igazolták, és  lehet olyan eszköz, amelyen keresztül a berberin pozitívan befolyásolja a májfunkciót. Kimutatták, hogy a berberin megváltoztatja az anyagcserével kapcsolatos génexpressziót és az epesav metabolizmusát az FXR-t is magában foglaló utakon keresztül. Állatkísérletekben kimutatták, hogy a berberin megakadályozza a HFD-vel összefüggő elhízást és a máj triglicerid felhalmozódását vad típusú (normál) egerekben, de nem azokban, amelyekben az intestinalis FxR expresszió genetikai eliminációja volt. A berberinről azt is kimutatták, hogy elnyomja az elhízással összefüggő gyulladást és a máj steatosisát egerekben azáltal, hogy csökkenti a jnk1 néven ismert gyulladásos komplex foszforilációját, amely a steatohepatitis kialakulásában szerepet játszó protein kináz. A JNK1-et erősen aktiválják a környezeti stresszorok és a gyulladásgátló citokinek.
lehet olyan eszköz, amelyen keresztül a berberin pozitívan befolyásolja a májfunkciót. Kimutatták, hogy a berberin megváltoztatja az anyagcserével kapcsolatos génexpressziót és az epesav metabolizmusát az FXR-t is magában foglaló utakon keresztül. Állatkísérletekben kimutatták, hogy a berberin megakadályozza a HFD-vel összefüggő elhízást és a máj triglicerid felhalmozódását vad típusú (normál) egerekben, de nem azokban, amelyekben az intestinalis FxR expresszió genetikai eliminációja volt. A berberinről azt is kimutatták, hogy elnyomja az elhízással összefüggő gyulladást és a máj steatosisát egerekben azáltal, hogy csökkenti a jnk1 néven ismert gyulladásos komplex foszforilációját, amely a steatohepatitis kialakulásában szerepet játszó protein kináz. A JNK1-et erősen aktiválják a környezeti stresszorok és a gyulladásgátló citokinek.
a berberin a bélben is hat. Nemcsak a bél mikrobiális egyensúlyát érinti, hanem közvetlenül befolyásolja a bél permeabilitását is, javítva az endotoxémiának kitett állatok szoros csomópont-integritását vagy a gyulladásgátló citokinekkel kezelt sejttenyészeteket., Közvetlen gyulladáscsökkentő hatásokat is kimutattak.
a berberin előnyeit a NAFLD-ben klinikailag is bizonyították egy randomizált, párhuzamos kontrollos, nyílt klinikai vizsgálatban. NAFLD-ben szenvedő betegeknél kimutatták, hogy a berberin helyreállítja a normális májszerkezetet, a lipideket és a vércukorszint-anyagcserét, jelentős javulást tapasztalva azon populációhoz képest, akik csak életmódbeli változásokat hajtottak végre.
probiotikumok
tekintettel a sok emésztőrendszeri zavar és a májenzim-emelkedés közötti kapcsolatra, nem meglepő, hogy a probiotikumokat a NAFLD kezelésére is tanulmányozták. Egy közelmúltbeli metaanalízis jól összefoglalja a kollektív eredményeket.
százharmincnégy, májbiopsziával Nafl/Nash-t diagnosztizált beteget vontak be ebbe az elemzésbe, és az erre a metaanalízisre alkalmas négy randomizált, kontrollos vizsgálatban alkalmazott minden beavatkozás egyedi volt (Lactobacillus bulgaricus és Streptococcus thermophilus három hónapig; Lactobacillus GG nyolc hétig; Bifidobacterium longum és fruktooligoszacharidok (FOS) 24 hétig; és a Lactobacillus plantarum, L. delbrueckii, L. acidophilus, L. rhamnosus és Bifidobacterium bifidum hat hónapig). A probiotikumok adagja napi 500 millió és 12 milliárd kolóniaképző egység (CFU) között mozgott. A probiotikus kezelések szignifikánsan csökkentették az ALT és az AST szintet -23,71 UI/L és -19,77 UI/L-rel. Jelentős javulást figyeltek meg az összkoleszterinszintben, a tumor nekrózis faktor (TNF)-a) és az inzulinrezisztenciában is.
két további klinikai vizsgálat vizsgálta a probiotikumokat a gyermekgyógyászati NAFLD kezelésére. Egy kettős-vak, placebo-kontrollos, kísérleti vizsgálatban tizenkét gyermek, akiknek átlagos életkora 10 év.7 éves, ultrahanggal diagnosztizált zsírmájváltozásokkal és tartós transzamináz emelkedéssel 12 milliárd CFU L. rhamnosus GG-t vagy placebót kaptak naponta 8 héten keresztül. A probiotikummal végzett kezelés szignifikánsan csökkentette az ALT-szintet a placebóhoz képest, azonban a máj echogenitása és az AST-szintje nem változott. Ezenkívül az anti-peptidoglikán-poliszacharid antitestek, amelyek a baktériumok vagy a bakteriális membrán transzlokációjának indikátorai a bélgáton keresztül, szignifikánsan csökkentek a probiotikumot kapó gyermekeknél a placebóhoz képest. A második tanulmány biopsziával bizonyított NAFLD-vel rendelkező gyermekek kezelését vizsgálta VSL #3-mal, 8 probiotikus törzs nagy hatékonyságú keverékével (beleértve Streptococcus thermophilus, 3 Bifidobacteria spp., és 4 Lactobacillus spp.), a placebóhoz képest. A probiotikumot kapó gyermekeknél a zsírmáj pontszámok szignifikánsan javultak, a vizsgálat végén a none, könnyű, közepes vagy súlyos zsírmáj valószínűsége 21%, 70%, 9% és 0% volt, szemben a placebo csoport 0% – ával, 7% – ával, 76% – ával és 17% – ával.
következtetés
a biztonságos és hatékony lehetőségek széles skálája áll rendelkezésre, amelyek támogatják a NAFLD-ben szenvedők egészségének helyreállítását. Bár minden egyénnek különböző mögöttes mechanizmusai lehetnek, amelyek hozzájárulnak a májműködési zavarhoz és a gyulladásos változásokhoz, ezek a támogató természetes szerek—és sok más (lásd 2.táblázat)—támogathatják a normális májfunkciót az ilyen kihívásokkal küzdő egyéneknél.
2.táblázat: táplálkozási és botanikai beavatkozások a NAFLD számára. Az ilyen tápanyagokat szakképzett és engedéllyel rendelkező egészségügyi szakember irányítása alatt kell használni.
| tápanyag | adagolás | mechanizmus |
| foszfatidilkolin (PC), étrendi kolin forrása | 1, 5 g naponta kétszer étkezés közben (PC) vagy 200 mg naponta kétszer (kolin) | a kolin gyakori étrendi hiány. PC előállításához szükséges epe és védő gasztrointesztinális nyálkahártya gáton. |
| bogáncsmag | 140-200 mg naponta egyszer-háromszor | hepatoprotektív. Támogatja a máj glutation szintjét, stabilizálja az epesó exportpumpát (BSEP), és aktiválja az FXR útvonalakat. |
| a berberin HCl | 500 mg naponta kétszer-háromszor | javítja a szérum glükóz-és lipidprofilt, csökkenti a máj zsírtartalmát is. |
| probiotikumok, beleértve a B. longum, B. bifidum, S. thermophilus, L. rhamnosus, L. acidophilus és L. plantarum | 12 milliárd kolóniaképző egység (CFU) naponta | javította a bél epithelialis gátfunkcióját és csökkentette a bél és a szisztémás gyulladást. |
| acetil-glutation | 300 mg naponta | javítja a májsejtek méregtelenítő képességét. |
| N-acetilcisztein (NAC) | 500-600 mg naponta kétszer, legjobb éhgyomorra bevenni | a NAC gátolja a lipidperoxidáció terjedését és támogatja a máj glutationszintjét. |
| E-Vitamin (tokoferolok)
vagy tokotrienolok |
400 napi 1200 ne étkezés közben
200-300 mg étkezés közben |
védő antioxidáns.
a tokotrienolok a zsírsav-szintáz és a karnitin-palmitoil-transzferáz enzimek szabályozásával csökkentik a triglicerid felhalmozódást, ami a májgyulladás és az endoplazmatikus retikulum stressz csökkenéséhez vezet. |
| az Omega-3 esszenciális zsírsavak | 2 – 4 g naponta, étkezés közben | az Omega-3 többszörösen telítetlen zsírsavakról ismert, hogy csökkentik a szterin szabályozó elem-kötő fehérje-1C-t és a peroxiszóma proliferátor által aktivált alfa receptor szabályozását, ezáltal elősegítve a zsírsav oxidációját és csökkentve a steatosist. |