はじめに
ペイロニー病(PD)は、白癬の瘢痕化を特徴とする陰茎の局所的な創傷治癒の結合組織障害である。 この繊維状の非弾性瘢痕は、陰茎の痛み、陰茎の変形および勃起不全(ED)を引き起こし、性交を行うことが困難である。 フランソワ-ド-ラ-ペイロニーは、フランスのルイ14世の外科医であった1743年に最初にこの状態を説明した。 以前の研究では0.3〜0.7%の発生率が報告されていましたが、最近の出版物では3.2〜8.9%の全体的な発生率が示されており、症例の75%以上が45〜65歳(1,2)の 注目すべきは、患者の10%が40歳(前に症状の発症を経験する2)。 さらに、根治的前立腺切除後のPDの発生率は15.9%と高いことが報告されており、最近の研究では、前立腺癌治療後のEDのためのインフレータブルペニールプロテーゼ移植手術の際に陰茎湾曲が一般的な所見(38.6%)であることが示されている(3,4)。
PDの治療は、集中した履歴と身体検査から始まります。 詳細な歴史は、疾患の発症および期間、関連する外傷性病因、陰茎湾曲の程度、勃起時の長さの喪失、および性機能の主観的レベルに関する情報を評価す 主観的な性的評価に関しては、勃起機能の国際指数(IIEF)などの標準化されたアンケートは、客観的および主観的な初期評価と治療中の有効性を測定するためのツールを可能にする。 泌尿生殖器系の身体検査には、伸びている間の陰茎の長さ、プラークの位置、およびサイズが含まれるべきである。 曲率の程度は、患者が直立したファルスの写真を撮ることによって、または陰茎二重ドップラー超音波と組み合わせて血管活性注射によって評価するこ
PDの自然史と病因を理解することは、適切な治療レジメンを選択する上で重要である。 病態生理学は完全には理解されていないが、扇動事象は白癬菌に対する無症状の外傷性涙であると仮定されている。 涙は増殖性線維性反応をもたらし、その結果、非弾性瘢痕が生じる。 PDの治療は急性期と慢性安定期に分けられる。 急性期の時間は、症状の発症から12ヶ月未満と大まかに定義されています。 この時間の間に、患者の傷は変更し、変わり続けています。 慢性期は、患者の湾曲が少なくとも6ヶ月間安定したままであれば決定される。 外科的治療はPDの金本位のままですが、それは主に疾患の慢性期に男性に提供されています。 急性期のそれらの患者のために、薬物療法は、機能を改善し、変形を減少させ、瘢痕の進行を安定させる可能性を提供する(5)。 本明細書では、PDの経口治療の選択肢に関する現在入手可能な知識をレビューする。 リストされている特定の勧告は証拠に基づく所見に基づいているが、他の勧告は専門家の意見を反映していることに注意することが重要である(表1)。

全表
パラアミノベンキソ酸カリウム(POTABA)
POTABAは、その抗線維性および抗炎症性特性で知られている化合物で、皮膚筋炎強皮症 その有効性は、セロトニンレベルの低下、モノアミン酸化酵素活性の増加、線維芽細胞グリコサミノグリカン分泌の阻害によるコラーゲン形成の減少に起因すると考えられている(6)。 PDを治療するためのPOTABAの最初の提案された使用は、1959年にZarafonetisとHorrax(7)によって行われました。 2005年、Weidner et al. 非石灰化プラークを有するナイーブPD患者の治療におけるPOTABA(51患者)対プラセボ(52患者)のマルチセンター、無作為化、二重盲検プラセボ対照試験を実施した。 試験アームは3gのポタバを経口投与し、4ヶ月間12回経口投与した。 12ヶ月後、POTABAの患者は、プラセボの患者と比較して陰茎プラークのサイズが有意に改善していた。 さらに、偽薬を受け取っている患者は彼らの湾曲の悪化があるために注意されました。 著者らは、POTABAは、湾曲の進行を防ぐ瘢痕組織の安定化を助けるかもしれないと結論付けた(6)。 POTABAの有効性を評価するためのこれ以上の無作為化対照試験はなかった。 これはおそらく、胃腸の苦痛、下痢、急性肝炎、および低血糖(含む、その副作用プロファイルに起因する8)。
ビタミンE
脂溶性酸化防止剤であるビタミンEは、一酸化窒素(NO)を飽和させるフリーラジカルを不活性化し、活性なNOレベルを上昇させて適切な創傷治癒を可能にする。 酸化圧力の制限によって、それは可能性としてはまた炎症抑制の効果を提供します。 それは1948年(9)にPDの処置のために最初に記述され、安価および供給が原因で、PDのための最も頻繁に規定された口頭代理店に残ります(10)。 過去70年間の使用にもかかわらず、複数のプラセボ対照デザインは、痛み、曲率の程度、プラークサイズ、または性交を有する能力において有意な改善を示 1983年、PryorとFarrellは、40人のPD患者を対象としたビタミンEの二重盲検プラセボ対照試験を完了し、プラークの大きさや陰茎の湾曲に有意な改善は見られませんでした(11)。 さらに、Safarinejad et alによる2007年のより最近の研究。 PDのためのビタミンEを評価するこれまでの最大の試験を提供しました。 著者らは、早期慢性PDを有する236人の男性において、ビタミンE単独およびL-カルニチンとの組み合わせをプラセボと比較した; 勃起時の痛み、膣の浸透を妨げない陰茎湾曲、非痛みを伴う触知可能な瘢痕、陰茎超音波上の高エコー病変、石灰化の欠如、および総プラーク面積<2cm2に分類さ グループ1(58人の人)はビタミンE300mgを一日二回口頭で受け取りました。 グループ2(59人の男性)は、プロピオニル-L-カルニチン、一日二回経口1gを受けました。 グループ3(60人の男性)は、ビタミンE300mgを一日二回経口投与し、プロピオニル-L-カルニチン1gを一日二回経口投与した。 最後にグループ4は6か月の試験期間の間に偽薬の同じような養生法を受け取りました。 治療後、四つのグループ(P=0.9)、またプラークサイズ(P=0.1)(12)のいずれかの減少の間に陰茎湾曲の減少に有意な変化はなかった。
ビタミンEの有効性を証明する証拠がないにもかかわらず、ビタミンEは依然として頻繁に処方され、相乗的な役割を期待して他の治療法と同時 ビタミンEの使用による一般的な副作用には、吐き気、嘔吐、下痢、および前立腺癌および脳血管イベントのリスク増加が含まれます(13)。
コルヒチン
コルヒチンは痛風の治療で主に知られていますが、PDの治療に役立つ特性も示しています。 コルヒチンはそれにより細胞の有糸分裂、白血球の付着およびコラーゲンの輸送を禁じるtubulinを、解重合させます。 この特性を適用すると、コルヒチンは理論的にはコラーゲン沈着を阻害することによって創傷収縮を減少させるべきである(14)。 コルヒチンを評価するほとんどの研究は、曲率のいくつかの改善を説明しているが、これらの研究は無作為化されておらず、改善の定義のための客観的な測定を提供していない。 Safarinejad et al. 石灰化プラークのない84人のPD患者を対象とした単一のセンター、無作為化、二重盲検、プラセボ対照試験を完了することにより、コルヒチンの治療効果を評価した数少ない試験の1つであることが証明されました(15)。 コルヒチン群の患者は、毎日0.5–2.5mgのコルヒチンで4ヶ月間治療された。 試験の終わりに、コルヒチン群は陰茎の湾曲またはプラークのサイズの客観的な改善を示さなかった。 他の研究では、ビタミンEとのコルヒチンの相乗効果を評価しています。Prieto Castro et al. イブプロフェン単独と比較して、毎日のビタミンEとコルヒチンを使用している患者のプラークサイズと陰茎湾曲の有意な改善を報告した(16)。 注目すべきは、この試験には45人の患者しかおらず、プラセボ群はなかったことである。 しかし、100人の男性を対象としたその後のレトロスペクティブ研究では、コルヒチンとビタミンEと組み合わせたコルヒチンとの間の痛みの軽減、陰茎の湾曲、またはプラークサイズの有効性に統計的に有意な差はなかった(17)。
タモキシフェン
タモキシフェンは非ステロイド性エストロゲン受容体拮抗薬である。 PDの治療では、線維芽細胞から放出されるTGF-βの放出を調節することによって、白斑膜における線維形成を減少させることが示されている(18)。 ラルフ他 最初に31人の人のうち11のためのpenile醜状の改善を示した制御されていない調査の結果として1992年に処置を提案しました。 しかし、これらの所見は、石灰化プラークのないPD患者25人を対象とした前向きプラセボ対照試験でタモキシフェンを評価した場合、再現性がなかった。 1日2回20mgのタモキシフェンを使用したにもかかわらず、プラセボと比較して痛み、湾曲、またはプラークの大きさに有意な改善はなかった(19)。
カルニチン
カルニチンは、細胞ストレス時のフリーラジカル形成の減少を可能にするアセチル補酵素-Aの阻害剤です。 2001年、Biagiotti et al. L-カルニチン対タモキシフェンに対する96人のPD患者の無作為化試験を実施した。 結果は、Lカルニチン群(20)で有意な陰茎曲率の改善を示した。 前述のように、Safarinejad2007 4腕試験(ビタミンE、カルニチン、ビタミンEとカルニチン、およびプラセボ)は、陰茎の湾曲、プラークの大きさ、または痛み(の有意な改善を
オメガ3脂肪酸
他の経口剤と同様に、オメガ3脂肪酸は、その既知の抗炎症特性のためにPDの治療において評価されています。 2009年には、Safarinejad et al. プラセボ試験と比較して、前向きで無作為化された二重盲検オメガ-3脂肪酸の結果を発表しました。 初期慢性期PDを有する224人の患者の合計は1に無作為化された。毎日のオメガ3の補足の84g対偽薬6か月間。 患者は、6ヶ月の投薬の前後にIIEF-5およびPDDUで評価された。 残念なことに、プラーク容積、陰茎湾曲、勃起時の痛み、および勃起機能に関して有意な改善はなかった(21)。 現在、PDの早期慢性期におけるオメガ3補充の有益な効果を支持するデータが不足している。
プロカルバジン
プロカルバジンは、CNSリンパ腫、ホジキンリンパ腫、高悪性度神経膠腫の治療によく使用されるアルキル化化学療法薬です。 1968年、Aron et al. ホジキン病のプロカルバジンによる治療を受けている患者のデュピュイトレン病の退行を指摘し、それによって結合組織の増殖を伴う疾患におけるその使用を示唆している(22)。 この前提で、1970年代に、ByströmはPDの治療のためにプロカルバジンを提案したが、その後の研究では客観的な利益は明らかにされなかった。 さらに、研究は細胞傷害性薬物の重大な副作用を明らかにし、PDの良性疾患には使用しないことが推奨された。 副作用には、骨髄抑制、肝毒性、疲労、GI苦痛、およびCNS障害が含まれる(23,24)。
ホスホジエステラーゼ5型阻害剤(PDE-5阻害剤)
PDE-5阻害剤はEDの治療薬として一般的に考えられていますが、最近の研究では、EDの有無にかかわらず、PD PDE-5阻害剤は、gmpへのcGMPの分解を阻害することにより、環状グアノシン一リン酸(cGMP)を増加させる。 CGMPおよびNOの増加に伴い、コラーゲン合成および沈着が阻害され、線維芽細胞および筋線維芽細胞のアポトーシスが起こる(25)。 この特性のために、PDE-5阻害剤は瘢痕リモデリングに有利であることが判明する可能性がある。 PDのラットモデルではプラークのサイズ(25)と同様、albuginea tunicaのコラーゲンに繊維芽細胞の比率で重要な減少を引き起こすために、sildenafilにより示されていました。 Chungたちは、ヒト被験者におけるPDの治療にタダラフィルを使用することを研究している。 その2人が報告している。6か月間毎日5mgのtadalafilは触診可能なpenileプラークなしで患者の69%(24/35)の隔壁の傷の決断で起因しました。 非処置の腕の10%だけ傷の決断を指摘しました。 中隔瘢痕は臨床的に触知可能ではなく、この研究のほとんどの患者は湾曲を有していなかったことに言及することが重要である(26)。 最近では、2014年の研究では、毎日50mgのシルデナフィルまたは400iuビタミンEを3ヶ月間使用したPD患者の治療結果が報告されています。 12週間後、両方のグループは、プラーク体積と統計的に有意であった陰茎湾曲の同様の減少を示した。 しかし,両群間の差は統計的に有意ではなかった。 Sildenafilのコホートは単独でビタミンEと比較されるIIEFのスコアおよび苦痛の減少で統計的に有意な改善を示しました(27)。 大規模な二重盲検プラセボ試験を実施し、PDE-5阻害剤の臨床的利益を検証する必要があるが、現在の研究は有望である(表2)。
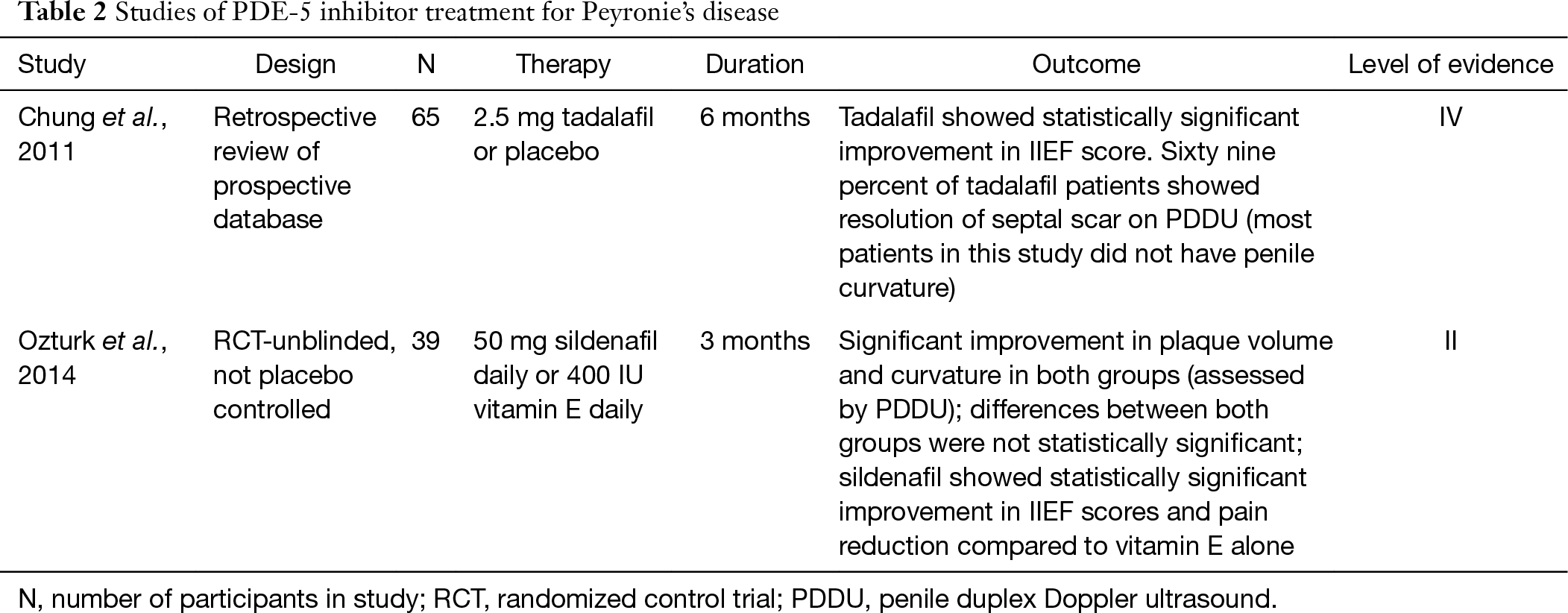
フル表
L-アルギニン
L-アルギニンはNO合成酵素を刺激するNO前駆体である。 これは、アポトーシスによる線維芽細胞の減少と同様に、NOの増加を引き起こす。 これら二つの特性は、抗線維化剤としてのL-アルギニンの背後にあるメカニズムであると考えられている(25)。 前述のように、Valente e t a l. PDE-5阻害剤だけでなく、l-アルギニンで治療したラットモデルにおける陰茎プラークを評価した。 PDE-5阻害剤と同様に、L-アルギニンは、プラークサイズだけでなく、線維芽細胞比(25)にコラーゲンの有意な減少を示した。 Medeiros et al.による後の研究。 骨盤放射線にラットの陰茎を提出するときにアルギニンはまた、瘢痕組織形成に対する保護効果を有することを実証した(28)。 2012年、Abern et al. 病変内ベラパミル、経口L-アルギニンおよび経口ペントキシフィリン(PTX)と組み合わせて陰茎牽引療法で治療されたPD患者の曲率改善の傾向を指摘した(29)。 この研究には、曲率の改善に寄与する可能性のある多数の変数がありますが、PDの治療にL-アルギニンを使用した数少ないヒト試験の1つであることが証明されています。 これらの知見を考えると、L-アルギニンはPDのための貴重な治療選択肢であることが証明されるかもしれないが、さらなるヒト試験が必要である。
ペントキシフィリン(PTX)
PDの治療のために調査された経口薬のほとんどは、対照研究で悪いまたは不確定な結果を示していますが、PTXははるかに良 PTXは、既知の抗炎症および抗線維化特性を有する非特異的ホスホジエステラーゼ阻害剤として機能するキサンチン誘導体である(30)。 それはtunicaのalbugineaの繊維芽細胞拡散を防ぎ、コラーゲンのtgf-Bによって仲介される沈殿を減衰させ、エラスチンの沈殿を減らし、そしてfibrinolytic活動を高めることを示 これらの特性を考慮すると、2010年の二重盲検、プラセボ対照研究は、早期慢性PD患者におけるPTXの効果を決定しようとした(30)。 二百二十から八患者は、400mgのPTX持続放出対プラセボを6ヶ月間受けるために無作為化された。 ほとんどの参加者は、少なくとも一つの以前のPD治療に失敗していました。 プラセボ群は、治療群(11%)と比較して、疾患の進行を有する可能性が4倍高かった(42%)。 さらに、PTXグループは、客観的および主観的尺度の両方で有意な改善を示した;(I)プロスタグランジンE1と体形注射前後の二重超音波によって測定されたpenile曲率の改善;(II)プラーク体積および(III)IIEFスコア(30)。 より最近の研究では、経口抗酸化物質、病巣内PTXおよび病巣内ベラパミルと組み合わせて経口PTXを評価しており、様々な結果が得られている(34,35)。 PTXは依然としてPD治療の強力な競争相手であるが、結果が再現可能であることを確実にするためには、さらなる大規模な多施設試験を締結する必要がある(表3)。

完全な表
結論
何十年ものPD研究にもかかわらず、決定的な病因および病態生理は完全には解明されていない。 外科療法が慢性の厳しいPDのための金本位のままである間、他のより少なく侵略的な処置の選択、即ち口頭およびintralesional薬物の無数があります。 本明細書では、我々は、PDの治療のための主に一般的に処方されるか、または議論される経口剤をレビューした。 多くのうまく設計された研究では、経口薬で肯定的な反応が発見されていますが、サンプルサイズが小さいため、研究のパワーと再現性が制限されます。 現在、米国泌尿器科協会のガイドラインでは、臨床医はビタミンE、タモキシフェン、オメガ3脂肪酸、またはビタミンEとL-カルニチンとの組み合わせによる経口療法を提供すべきではないとしている。 同様に、性的医学に関する2010年の国際相談は、PDに対する経口剤の日常的な臨床使用を支持しなかった(5)。 ガイドラインによって制限されない2つの経口薬は、PDE-5阻害剤およびPTXである。 PDE-5およびPTXに関するさらなる研究は、大規模な多施設二重盲検無作為化対照試験を含むために、その有効性を決定するために必要とされている。 両方の投薬クラスは、PDの治療のための許可された経口薬がないことに希望を与える。
脚注
利益相反:著者は宣言する利益相反を持っていません。
- Mulhall JP,Creech SD,Boorjian SA,et al. 前立腺癌のスクリーニングのために示す人の人口のPeyronieの病気の流行の主観的で、客観的な分析。 J Urol2004;171:2350-3.
- Mulhall JP,Schiff J,Guhring P.ペイロニー病の自然史の分析。 Jウロール2006;175:2115-8;議論2118.
- Tal R,Heck M,Teloken P,et al. 根治的前立腺切除後のペイロニー病:発生率および予測因子。 JセックスMed2010;7:1254-61.
- Lin H,Alba F,Romero C,et al. 1815penile湾曲は根治的なprostatectomyの後で勃起不全の患者のためのpenile語頭音添加の注入に共通の所見です。 J Urol2011;185:e728-e729.
- Ralph D,Gonzalez-Cadavid N,Mirone V,et al. ペイロニー病の管理:エビデンスに基づく2010年のガイドライン。 JセックスMed2010;7:2359-74.
- Weidner W,Hauck EW,Schnitker J,et al. Peyronieの病気の処置のカリウムのparaaminobenzoate(POTABA):前向きの、偽薬制御された、無作為化された調査。 Eur Urol2005;47:530-5;ディスカッション535-6.
- Zarafonetis CJ,Horrax TM. パラアミノ安息香酸カリウム(potaba)によるペイロニー病の治療。 J Urol1959;81:770-2.
- Roy J、キャリアS.パラアミノ安息香酸カリウム(Potaba)によるペイロニー病の治療に関連する急性肝炎。 JセックスMed2008;5:2967-9.
- Scott WW,Scardino PL. ペイロニー病の治療における新しい概念。 南メドJ1948;41:173-7.
- レヴァイン-ラ、バーネット-アル。 ペイロニー病のための標準的な操作手順。 JセックスMed2013;10:230-44.
- Pryor JP,Farrell CF. ペイロニー病におけるビタミンEの制御された臨床試験。 Prog Reprod Biol1983;9:41-5.
- Safarinejad氏、ホセイニSY、Kolahi AA。 早期慢性ペイロニー病患者におけるビタミンEとプロピオニル-L-カルニチンの別々または組み合わせの比較:二重盲検、プラセボ対照、無作為化試験。 J Urol2007;178:1398-403; 1403.
- Klein EA,Thompson IM Jr,Tangen CM,et al. ビタミンEと前立腺がんのリスク:セレンとビタミンEがん予防試験(選択)。 JAMA2011;306:1549-56.
- El-Sakka AI,Bakircioglu ME,Bhatnagar RS,et al. 動物モデルにおけるPeyronieのような状態に対するコルヒチンの効果。 J Urol1999;161:1980-3.
- Safarinejad氏ペイロニー病の管理におけるコルヒチンの治療効果:無作為化二重盲検、プラセボ対照試験。 Int J Impot Res2004;16:238-43.
- Prieto Castro RM,Leva Vallejo ME,Regueiro Lopez JC,et al. ペイロニー病の初期段階におけるビタミンEおよびコルヒチンとの併用治療。 BJU Int2003;91:522-4.
- Cortés-González JR,Glina S.ペイロニー病の保存的治療:コルヒチン対コルヒチン+ビタミンE.Actas Urol Esp2010;34:444-9.
- ラルフDJ,ブルックスMD,Bottazzo GF,et al. タモキシフェンによるペイロニー病の治療。 Br J Urol1992;70:648-51.
- Teloken C,Rhoden EL,Grazziotin TM,et al. Peyronieの病気の処置の偽薬対Tamoxifen。 J Urol1999;162:2003年5月。
- Biagiotti G,Cavallini G.ペイロニー病の経口療法におけるアセチル-L-カルニチン対タモキシフェン:予備報告。 BJU Int2001;88:63-7.
- Safarinejad氏早期ペイロニー病の治療に対するオメガ-3の有効性と安全性:前向き、無作為化、二重盲検プラセボ対照試験。 JセックスMed2009;6:1743-54.
- Aron E.細胞増殖抑制剤(メチルヒドラジン)によるデュピュイトレン病の治療。 1968;76:1956.
- Byström J,Johansson B,Edsmyr F,et al. 陰茎形成不全症(ペイロニー病)。 治療の様々な形態の結果。 Scand J Urol Nephrol1972;6:1-5.
- オーステリンクW、プロカルバジンによるペイロニー病の治療を行う。 Br J Urol1975;47:219-20.
- Valente EG,Vernet D,Ferrini MG,et al. L-アルギニンおよびホスホジエステラーゼ(PDE)阻害剤は、ペイロニーの線維性プラークおよび関連する線維芽細胞培養における線維症を打ち消す。 2003年9月、229-44歳でプロデビュー。
- Chung E,Deyoung L,Brock GB. 陰茎中隔瘢痕リモデリングにおけるPDE5阻害剤の役割:臨床および放射線学的転帰の評価。 JセックスMed2011;8:1472-7.
- Ozturk U,Yesil S,Goktug HN,et al. Peyronieの病気および勃起不全の患者に対するsildenafilの処置の効果。 Ir J Med Sci2 0 1 4;1 8 3:4 4 9−5 3.
- Medeiros Jl Jr,Costa WS,Felix-Patricio B,et al. 骨盤放射線に提出されたラットの陰茎に対するアルギニンおよびグルタミンによる栄養補給の保護効果。 Andrology2014;2:943-50。
- Abern MR,Larsen S,Levine LA. Peyronieの病気のためのpenile牽引、intralesional verapamilおよび口頭療法の組合せ。 JセックスMed2012;9:288-95.
- Safarinejad MR,Asgari MA,Hosseini SY,et al. 早期慢性ペイロニー病におけるペントキシフィリンの有効性および安全性に関する二重盲検プラセボ対照研究。 BJU Int2010;106:240-8.
- Raetsch C,Jia JD,Boigk G,et al. ペントキシフィリンは、ラット二次胆道線維症におけるプロフィブロゲン性サイトカインおよびプロコラーゲンI発現をダウンレギュレートする。 Gut2002;50:241-7。
- Schandené L,Vandenbussche P,Crusiaux A,et al. 単球およびT細胞による腫瘍壊死因子-α(TNF-α)およびインターロイキン-6(IL-6)の産生に対するペントキシフィリンの差動効果。 Immunology1 9 9 2;7 6:3 0−4.
- Shindel AW,Lin G,Ning H,et al. ペントキシフィリンは、ヒト白膜由来線維芽細胞における成長因子-β1刺激コラーゲン沈着と弾性形成を変換減衰パート1:細胞外マトリックスへの影響。 JセックスMed2010;7:2077-85.
- Paulis G,Barletta D,Turchi P,et al. ペイロニー病の治療における他の抗酸化物質に関連するペントキシフィリンの有効性および安全性評価:症例対照研究。 2015年8月1日から10日にかけて放送された。
- Alizadeh M,Karimi F,Fallah氏ペイロニー病におけるベラパミル有効性の評価ペントキシフィリンとの比較。 Glob J健康Sci2014;6:23-30.
- Smith JF,Shindel AW,Huang YC,et al. ペイロニー病の男性におけるペントキシフィリン治療および陰茎石灰化。 アジアJ Androl2011;13:322-5.