非アルコール性脂肪肝疾患に対する自然介入の背後にある証拠:この一般的な病気を治療するためのボタニカルズ、栄養素、およびプロバイオティクス
成人および小児科の両方における非アルコール性脂肪肝疾患(NAFLD)の上昇および示された医薬品治療の欠如を考えると、この状態の治療のための自然戦略は”次善のもの”として十分に態勢を整えている。”いくつかの栄養補助食品や植物は臨床的に研究されており、NAFLDとその炎症性の対応物である非アルコール性脂肪性肝炎(NASH)の治療のための約束を示して これらの治療法のどれがNAFLDの開発に寄与する要因に対処しているかを考えると、単に症状に対処するのではなく、病気の根本原因のいくつかに効果的に対処する方法を理解するのにはあまり推論が必要ではありません。
NAFLDの設定での使用のための臨床的または疫学的証拠を伴う五つの補足的介入は、ホスファチジルコリンであり、リン脂質およびコリン、ビタミンEをαトコフェロールおよびデルタおよびガンマトコトリエノール、ミルクシスル種子抽出物、ベルベリン、およびプロバイオティクスの両方として提供する。
- 脂肪肝の変化:ホスファチジルコリン欠乏症と相関するか?
- ビタミンE
- ミルクシスル
- ベルベリン
- プロバイオティクス
- 結論
- キャリー-デッカー博士は、オレゴン州ポートランドの国立自然医学大学(現在の国立自然医学大学)を優等で卒業しました。 ドクター-オブ-ザ-イヤー デッカーは、胃腸疾患、気分の不均衡、摂食障害、自己免疫疾患、および慢性疲労に焦点を当てて、遠隔で患者を見ています。 自然療法医になる前はエンジニアであり、ウィスコンシン大学マディソン校とイリノイ大学アーバナ-シャンペーン校で生物医学と機械工学の大学院の学位を取得していた。 デッカー博士は、学術研究と執筆を楽しみ続け、これらのスキルを使用して、ライターとして統合医学教育を支援し、様々なリソースに貢献しています。 ドクター-オブ-ザ-イヤー Deckerは、教育および製品開発チームの一員として、アレルギー研究グループをサポートしています。
- 出典:
- Spengler EK、Loomba R.診断、肝生検の紹介、および非アルコール性脂肪肝疾患および非アルコール性脂肪性肝炎の治療に関する推奨事項。 メイヨークリニック 2015;90(9):1233–1246.
- Berardis S,Sokal E.小児非アルコール性脂肪肝疾患:公衆衛生上の問題が増加している。 ユール-ジュリエット()とも。 2014Feb;173(2):131-9.
- Jadeja R,et al. 非アルコール性脂肪性肝炎の治療のための漢方薬: 現在のシナリオと将来の見通し。 Evidベースの補数Alternat Med. 2014:648308.
- Pomorski T,et al. 細胞膜を渡る脂質の配分そして輸送。 セミン-セル-デヴ-バイオル… 2001Apr;12(2):139-48.
- 山路-長谷川A,et al. 生体膜中のリン脂質の非対称分布。 バイオルファームブル… 2006Aug;29(8):1547-53.
- Hišmiošullari AA,et al. 胆道脂質の分泌。 トゥルク-ジャイルズ所属。 2007Jun;18(2):65-70.
- Fischer LM,et al. 性およびmenopausal状態は栄養コリンのための人間の食餌療法の条件に影響を与えます。 Am J Clin Nutr. 2007May;85(5):1275-85.
- Wallace TC,et al. 通常のコリンの取入口は米国の卵および蛋白質の食糧消費と関連付けられます。 栄養素。 2017年5月9日(8日)に発売された。
- 遺伝子応答要素、遺伝的多型およびエピジェネティクスは、コリンのための人間の食事要件に影響を与えます。 IUBMBの生活。 2007Jun;59(6):380-7.
- 遺伝子応答要素、遺伝的多型およびエピジェネティクスは、コリンのための人間の食事要件に影響を与えます。 IUBMBの生活。 2007Jun;59(6):380-7.
- Guerrerio AL,et al. 非アルコール性脂肪肝疾患を有する患者の大規模なコホートにおけるコリン摂取。 Am J Clin Nutr. 2012Apr;95(4):892-900.
- Ma X,et al. ポリエニルホスファチジルコリンは非アルコール性肝線維症を減衰させ,その退行を促進する。 J-Hepatol. 1 9 9 6年5月;2 4(5):6 0 4−1 3.
- ホスファチジルコリンはヒヒの線維症および肝硬変から保護する。 消化器科. 1994Jan;106(1):152-9.
- Chanussot F,et al. 動物におけるシクロスポリンAによって誘導される肝内胆汁うっ滞の食事(n-6)多価不飽和ホスファチジルコリンによる予防。 ライフサイエンス 2003Jun13;73(4):381-92.
- Karaman A,et al. ラットの胆道閉塞によって誘発される肝障害に対する多価不飽和ホスファチジルコリンの保護効果。 J Pediatr Surg.2003Sep;38(9):1341-7.
- Karaman A,et al. ラットの胆道閉塞によって誘発される肝障害に対する多価不飽和ホスファチジルコリンの保護効果。 J Pediatr Surg.2003Sep;38(9):1341-7.
- Stremmel W,et al. ホスファチジルコリンによる粘膜保護。 ディグ-ディズ 2012;30Suppl3:85-91.
- Parlesak A,et al. 共役一次胆汁酸塩は、腸上皮細胞を介してエンドトキシンの透過性を低下させ、炎症性サイトカイン産生の抑制にホスファチジルコリンと相乗作用 クリティカルケアMed. 2007Oct;35(10):2367-74.
- Mitzscherling K,et al. ホスファチジルコリンは経上皮内毒素透過性のエタノール誘発性の増加を逆転させ、経上皮白血球活性化を廃止する。 アルコールClin Exp Res.2009Mar;33(3):557-62.
- Buzzetti E,et al. 非アルコール性脂肪肝疾患(NAFLD)のマルチヒット病因。 メタボリックシンドロームとは? 2016年6月(8):1038-48.
- El Hadi H,et al. 非アルコール性脂肪肝疾患の治療としてのビタミンE:現実または神話? (バーゼル)。 2018年(平成16年)7月1日現在の世帯数と人口は以下の通りである。
- Bugianesi E,et al. 非アルコール性脂肪肝疾患におけるメトホルミン対ビタミンEまたは処方食の無作為化比較試験。 アム-ジョイ-ジョイ-ジョイ 2005May;100(5):1082-90.
- Sanyal AJ,et al. 非アルコール性脂肪性肝炎のためのピオグリタゾン、ビタミンE、またはプラセボ。 N Engl J Med. 2010May6;362(18):1675-85.
- 小児における非アルコール性脂肪性肝炎のビタミンE治療: パイロット研究。 J-Pediatr. 2000Jun;136(6):734-8.
- Peh HY,et al. 癌を越えてビタミンE療法:トコフェロール対トコトリエノール。 ファーマコール-サー 2016Jun;162:152-69.
- 高コレステロール血症被験者におけるデルタ-トコトリエノールによる脂質パラメータ、サイトカイン、およびRNAの用量依存的変調は、AHAステップ-1食に制限さ MedのブリットJ&Med Res.2015;6(4):351-66.
- 高コレステロール血症の被験者における炎症性バイオマーカーおよび酸化ストレスに対するデルタ-トコトリエノールの影響。 クリン-エクスパンション-ジャパン所属。 2015;6(4):1000367.
- Zaiden N,et al. ガンマのデルタのトコトリエノールは肝臓のトリグリセリドの統合およびVLDLの分泌を減らします。 Jリーグ-横浜Fc所属。 2010Oct27;17(10):1019-32.
- Magosso E,et al. 非アルコール性脂肪肝における肝エコー原性応答の正常化のためのトコトリエノール:無作為化プラセボ対照臨床試験。 Nutr J.2013Dec27;12(1):166.
- Pervez MA,et al. 非アルコール性脂肪肝疾患患者における肝酵素、炎症、酸化ストレスおよび肝脂肪症に対するデルタ-トコトリエノール補充の効果。 トゥルク-ジャイルズ所属。 2011年03月29日(2):170-176.
- Abenavoli L,et al. 肝疾患におけるミルクシスル:過去、現在、未来。 Phytother Res.2010Oct;24(10):1423-32.
- Valenzuela A,et al. ラットの異なる組織におけるGSH含量の増加に対するシリマリンの選択性。 プランタ-メド… 1 9 8 9Oct;5 5(5):4 2 0−2.
- シリマリンの薬理学的研究の進歩。 メム-インスト-オズワルド-クルス 1991;86Suppl2:79-85.
- Gu M,et al. シリマリンは、ファルネシルX受容体の活性化を介して食事誘発性肥満に関連する代謝機能障害を改善する。 フロントファーマコール… 2016年(平成28年)7月34日現在の世帯数と人口は以下の通りである。
- Ali AH,et al. ファルネソイドX受容体作動薬の開発における最近の進歩。 アン-トランシルヴァニア 2015年3月1日、5度目の防衛に成功した。
- Traussnigg S,et al. 非アルコール性脂肪肝疾患(NAFLD)患者における非ステロイド性ファルネソイドX受容体アゴニストPX-104の有効性および安全性。 Zeitschrift für Gastroentologie. 2017年5月;55(05):A71.
- Zhong S,et al. 非アルコール性脂肪疾患の治療におけるシリマリンの治療効果:ランダム化対照試験のメタ分析(PRISMA)。 医学(ボルチモア)。 2017Dec;96(49):e9061.
- 非アルコール性脂肪肝疾患に対するメトホルミン、ピオグリタゾン、およびシリマリン治療の効果:無作為化対照パイロット研究。 ヘパト-モン 2012Aug;12(8):e6099.
- ベルベリン:いくつかの薬用植物に見られるアルカロイドの治療可能性。 Altern Med Rev.1997;2:94-103.
- Imanshahidi M,et al. 尋常性ベルベリスおよびその活性成分、ベルベリンの薬理学的および治療的効果。 Phytother Res.2008Aug;22(8):999-1012.
- 非アルコール性脂肪肝疾患の治療におけるベルベリンの潜在的なメカニズム。 分子だ 2016年(平成14年)21月10日現在の世帯数と人口は以下の通りである。
- 2型糖尿病、高脂血症および高血圧の治療におけるベルベリンの効果および安全性のメタ分析。 Jエスノファーマコール… 2015Feb23;161:69-81.
- Sun R,et al. 経口投与されたベルベリンは、微生物胆汁酸代謝および腸のFXRシグナル伝達経路を変化させることによって肝脂質代謝を調節する。 モル-ファーマコール 2017Feb;91(2):110-122.
- ベルベリンは肝臓の脂肪症を改善し、食事療法誘発の肥満のマウスのレバーおよび脂肪組織の発火を抑制します。 Sci Rep.2016Mar3;6:22612.
- Schattenberg JM,et al. JNK1ではなく、JNK2は、マウスにおける脂肪性肝炎の発症を促進する。 肝臓学だ 2006Jan;43(1):163-72.
- Han J,et al. ベルベリンの抗糖尿病メカニズムとしての腸内微生物叢の調節。 メド-サイ-モニット 2011年(平成17年)4月7日現在の世帯数と人口は以下の通りである。
- Gu Lら。 ベルベリンは、腸上皮タイトジャンクション損傷を改善し、エンドトキシン血症のマウスモデルでミオシン軽鎖キナーゼ経路をダウン調節します。 Jリーグ-ディビジョン所属。 2011Jun1;203(11):1602-12.
- Li N,et al. ベルベリンは、腸上皮細胞のin vitroモデルでプロ炎症性サイトカイン誘発タイトジャンクション破壊を減衰させます。 ユーロ-J-ファルム-サイ. 2010Apr16;40(1):1-8.
- Ma X,et al. 酸化ストレスおよび炎症による真性糖尿病の病因:ベルベリンによるその阻害。 フロントファーマコール… 2018Jul27;9:782.
- 非アルコール性脂肪肝疾患患者におけるベルベリンの有効性。 プロスワン 2015Aug7;10(8):e0134172.
- Ma YY,et al. 非アルコール性脂肪肝疾患に対するプロバイオティクスの影響:メタ分析。 ワールドJリーグ所属。 2013Oct28;19(40):6911-8.
- Vajro P,et al. 小児肥満関連肝疾患におけるLactobacillus rhamnosus株GGの影響。 J-PediatrのGastroenterol Nutr. 2011Jun;52(6):740-3.
- Alisi A,et al. 無作為化臨床試験:非アルコール性脂肪性肝炎を有する肥満小児におけるVSL#3の有益な効果。 Aliment Pharmacol Ther. 2014Jun;39(11):1276-85.
- Pérez-Rubio KG,et al. メタボリックシンドローム,インスリン感受性,インスリン分泌に対するベルベリン投与の効果。 メタボリックシンドロームとは? 2013Oct;11(5):366-9.
- Iacono A,et al. NAFLDを治療するための新たな治療戦略としてのプロバイオティクス:分子および生化学的メカニズムに焦点を当てる。 J Nutr Biochem. 2011Aug;22(8):699-711.
- 本田Yら。 非アルコール性脂肪肝疾患の治療のためのグルタチオンの有効性:オープンラベル、シングルアーム、多施設、パイロット研究。 BMC消化器病… 2017年8月17日(1):96。
- Dentico P,et al. . 最近のプログMed. 1995Jul-Aug;86(7-8):290-3.
- Khoshbaten M,et al. N-アセチルシステインは、非アルコール性脂肪肝疾患の患者の肝機能を改善する。 型肝炎モン… 2010;10(1):12-16.
- 武藤Cほか Γ-トコトリエノールは、脂肪酸代謝の調節を通じてラット一次肝細胞におけるトリアシルグリセロールレベルを減少させる。 J Clin Biochem Nutr. 2013;52(1):32-37.
- オメガ3補充と非アルコール性脂肪肝疾患:体系的なレビューとメタ分析。 J-Hepatol. 2012;56(4):944-51.
脂肪肝の変化:ホスファチジルコリン欠乏症と相関するか?
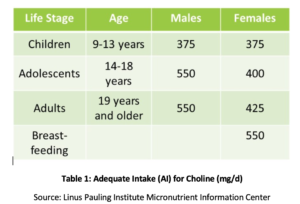
ホスファチジルコリン(PC)は、体内のすべての細胞の健康に不可欠であり、細胞膜が構成されている主要なリン脂質の一つです。、PCは総胆汁リン脂質の内容の90%に構成し、脂肪質の乳化、吸収および輸送を促進します。 調査はコリンの推薦された十分な取入口(AI)が(表1を見なさい)脂肪肝の変更または筋肉損傷のような不足の徴候の防止のために十分ではないかも さらに、最近の研究では、米国の成人の8%のみが推奨されるコリンのAIを満たしており、菜食主義者、閉経後の女性、および男性は不十分なリスクが最、遺伝の多型はまたまたボディのメチル基のもとであるコリンのための必要性を高めるかもしれません。
NAFLDのpostmenopausal女性では、減らされたコリンの取入口は線維症の高められた危険とかなり関連付けられるために示されていました。 動物では、PCは肝臓の発火と関連付けられる線維症から保護するために示されていました。、PCの増加された取入口はそれにより核要因κ B(NF-κ b)の抑制を含む多数のメカニズムによって胆汁うっ滞およびそれに続く肝臓損傷を、発火のよく理 胆道閉塞の動物モデルでは、補足的なPCは、肝臓の損傷、管の増殖、および線維症を減少させることが示されている。
PCは腸の健康にも不可欠であり、保護腸粘液層の主要成分である。 細胞培養では、PCとの処置は更に準の炎症性cytokineの応答を抑制する腸の上皮細胞を通した内毒素の移動を減らすために示されていました。 PCはまた腸の透磁率のアルコール誘発の増加の設定の内毒素の転座を減らします。 この有益な効果は、PCがアルコール性肝疾患における治療と考えられるメカニズムの一つとして提案されている。
ビタミンE
酸化ストレスのヒットと抗酸化防御の減少がNAFLDの開発をリードする要因として提案されているように、抗酸化物質が状態の潜在的な治療法として調査されていることは驚くべきことではありません。
 ビタミンEは、独立療法と補助療法の両方として、NAFLDの治療のためのいくつかの臨床試験で研究されています。 これらの研究のレビューでは、ビタミンEの投与量は400から1200IU/日の範囲であり、研究期間は24週間から2年以上であった。 所見は一般的に陽性であり、ビタミンEが含まれていた場合、組織学、脂肪症、および/またはトランスアミナーゼレベルの改善が見られたことを示してい、NAFLDの小児科では、ビタミンEはまた療法として調査されました。 NAFLDを持つ11人の子供を含むオープンラベルパイロット研究では、4-10ヶ月間のビタミンEの400-1200IUの補充は、治療中にトランスアミナーゼとアルカリホスファターゼレベルを正常化することが判明したが、治療が中止されると異常に戻った。 肝エコー原性は治療中に変化しなかった。
ビタミンEは、独立療法と補助療法の両方として、NAFLDの治療のためのいくつかの臨床試験で研究されています。 これらの研究のレビューでは、ビタミンEの投与量は400から1200IU/日の範囲であり、研究期間は24週間から2年以上であった。 所見は一般的に陽性であり、ビタミンEが含まれていた場合、組織学、脂肪症、および/またはトランスアミナーゼレベルの改善が見られたことを示してい、NAFLDの小児科では、ビタミンEはまた療法として調査されました。 NAFLDを持つ11人の子供を含むオープンラベルパイロット研究では、4-10ヶ月間のビタミンEの400-1200IUの補充は、治療中にトランスアミナーゼとアルカリホスファターゼレベルを正常化することが判明したが、治療が中止されると異常に戻った。 肝エコー原性は治療中に変化しなかった。
トコトリエノールは、天然に存在するビタミンEのあまり研究されていないファミリーであり、自然界でより頻繁に見られるトコフェロールが科学的研究を支配している。 但し、トコトリエノールはトコフェロールの40から60倍の酸化防止潜在性を持っているように研究で引用される有効な酸化防止剤です。 トコトリエノールは、総コレステロールとその画分を改善し、総コレステロールとLDLコレステロールを15-20%、トリグリセリドをほぼ30%まで減少させることが示されている。 トコトリエノールはまた、in vivoでの抗炎症および抗酸化作用を有し、高感度C反応性タンパク質(hs-CRP)レベルを低下させ、LDL酸化を減少させることが示さ
トコトリエノールはNAFLDの治療薬としても研究されている。 超音波診断されたNAFLDの患者では、混合されたトコトリエノールの200mg(高いガンマの一部分およびアルファのトコフェロールの付加的な61mgが付いているパーム油から、供給された)がかなり偽薬と比較される肝臓のエコー原性の応答そして寛解の率を正常化するために1年間取られました。 超音波診断されたNAFLDとトランスアミナーゼ上昇を有する患者を含む第二の研究では、トコトリエノールの300mg(90:10デルタ:ガンマブレンド)は、プラセボと比較してアスパラギン酸アミノトランスフェラーゼ(AST)、アラニンアミノトランスフェラーゼ(ALT)、hs-CRP、およびマロンジアルデヒド(酸化ストレスのマーカー)レベルだけでなく、脂肪肝指数スコアを有意に減少させた。
ミルクシスル
ミルクシスル(Silybum marianum)は、おそらく最もよく知られている肝臓保護植物です。 Silymarinのミルクシスルの活動的な要素の混合物、およびsilibininのその中で見つけられる最も活動的な混合物は動物実験で他の知られていたレバー有毒物質間のacetaminophen、アル シリマリンは、肝臓と腸の両方で強力な抗酸化物質であるグルタチオンのレベルを上昇させることが示されています。 それはまた、脂質過酸化を減少させ、細胞膜に損傷を与え、その機能を変化させ、そしておそらく細胞死を引き起こす。
シリビニンとシリマリンは、肝臓のファルネソイドX受容体(FXR)として知られる核胆汁酸受容体を活性化し、炎症経路を下方調節し、高脂肪食(HFD)摂食によ FXRは、体内の胆汁酸、グルコース、および脂質バランスの重要な調節因子です。 これらのミルクシスル由来化合物と同様の方法でFXRと相互作用する薬物も、NAFLDおよび関連する代謝課題の治療のために研究されている。
臨床研究では、ミルクシスルがNAFLDに関連する様々なパラメータを改善することも示されています。 2017年のメタアナリシスでは、NAFLD患者では、ミルクシスルによる治療でALTとASTがそれぞれ-5.08IU/Lと-5.44IU/Lで有意に減少することがわかりました。 投与量は、140mgから1日1回、200mgまで、8〜24週間の期間にわたって、1日3回の範囲であった。 毎日140mgの最も低い適量で、8週後に、重要な改善は56からの37へのASTおよびALTの減少に加えて絶食の血ブドウ糖(FBG)、脂質のプロフィールおよび血清のイン77IU/Lおよび78.73から53.05IU/L。
ベルベリン
オレゴン州のブドウの根や樹皮、ゴールデンシール、メギなどの植物に見られるオレンジがかった黄色のアルカロイドであるベルベリンは、NAFLDから保護し、その解決をサポートするのに役立つ多数のメカニズムを有する植物由来の物質である。,
ベルベリンの抗糖尿病および脂質バランス効果はいくつかの臨床試験で実証されており、 はベルベリンが肝機能に正の影響を与 ベルベリンは、fxrを含む経路を介して代謝関連遺伝子発現および胆汁酸代謝を変化させることが示されている。 動物実験では、ベルベリンは、野生型(正常)マウスにおけるHFD関連肥満および肝臓トリグリセリド蓄積を予防する効果を有するが、腸FXR発現の遺伝的排除 ベルベリンはまた、脂肪性肝炎の発症に関与するプロテインキナーゼであるJNK1として知られている炎症性複合体のリン酸化を減少させることに JNK1は環境ストレス因子と炎症促進性サイトカインによって強く活性化される。
はベルベリンが肝機能に正の影響を与 ベルベリンは、fxrを含む経路を介して代謝関連遺伝子発現および胆汁酸代謝を変化させることが示されている。 動物実験では、ベルベリンは、野生型(正常)マウスにおけるHFD関連肥満および肝臓トリグリセリド蓄積を予防する効果を有するが、腸FXR発現の遺伝的排除 ベルベリンはまた、脂肪性肝炎の発症に関与するプロテインキナーゼであるJNK1として知られている炎症性複合体のリン酸化を減少させることに JNK1は環境ストレス因子と炎症促進性サイトカインによって強く活性化される。
ベルベリンは腸内でも作用します。 それは腸の微生物バランスにだけでなく、影響を与えますが、また直接腸の透磁率に影響を与え、内毒素血症に応じて動物または炎症促進cytokinesと扱われ、直接的な抗炎症効果も実証されている。
NAFLDにおけるベルベリンの利点は、無作為化並列制御オープンラベル臨床試験でも臨床的に実証されています。 NAFLD患者では、ベルベリンは正常な肝構造、脂質、および血糖代謝を回復させることが示され、生活習慣の変化のみを実施した人口に有意な改善が見られ
プロバイオティクス
多くの消化器系障害と肝酵素上昇との関係を考えると、プロバイオティクスもNAFLDの治療薬として研究されていることは驚く 最近のメタ分析は、集合的な調査結果をよく要約しています。
肝生検によりNAFL/NASHと診断された患者をこの分析に含め、このメタ分析の対象となる無作為化比較試験で使用された各介入はユニークであった(Lactobacillus bulgaricusおよびStreptococcus thermophilus、Lactobacillus GG、24週間、Bifidobacterium longumおよびfructooligosaccharides(FOS)、およびLactobacillus plantarumの独自の組み合わせであるLactobacillus plantarumの独自の組み合わせであった。delbrueckii,l.acidophilus,l.rhamnosus,およびbifidobacterium bifidumを6ヶ月間投与した。 プロバイオティクスの投与量は、毎日500万から12億コロニー形成単位(Cfu)の範囲であった。 プロバイオティクス治療は、それぞれ-23.71UI/Lおよび-19.77UI/LによってALTおよびASTレベルを有意に減少させることが示された。 総コレステロール,腫よう壊死因子(TNF)-αレベル,およびインスリン抵抗性の有意な改善も認められた。
小児NAFLDの治療としてプロバイオティクスを調査した二つの追加の臨床試験。 二重盲検、プラセボ対照、パイロット研究では、12人の子供、10の平均年齢を持っています。超音波診断された脂肪肝の変化と持続的なトランスアミナーゼ上昇を伴う7歳は、L.rhamnosus GGまたはプラセボの12億Cfuを毎日8週間与えられた。 プロバイオティクスによる治療はプラセボと比較してALTレベルを有意に減少させたが、肝臓エコー原性およびASTレベルは変化しなかった。 さらに、抗ペプチドグリカン-多糖類抗体、細菌または腸の障壁を通る細菌の膜の転座の表示器は偽薬と比較されるprobioticを受け取っている子供でかなり減 第二の研究では、VSL#3、8プロバイオティクス株(Streptococcus thermophilus、3Bifidobacteria sppを含む)の高効力ブレンドで生検で証明されたNAFLDを有する子供の治療を検討した。 および4種のLactobacillus spp.)、プラセボと比較した。 プロバイオティクスを受けている小児では、脂肪肝スコアは、プラセボ群の0%、7%、76%および17%と比較して、研究終了時になし、軽さ、中等度、または重度の脂肪肝の確率が21%、70%、9%および0%であることで有意に改善された。
結論
NAFLDを持つ人々の健康回復を支援する幅広い安全で効果的な選択肢があります。 各個体は、肝機能障害および炎症性変化に寄与する異なる根底にあるメカニズムを有するかもしれないが、これらの支持天然薬剤および他の多くの(表2参照)のそれぞれは、これらの課題を有する個体における正常な肝機能を支持する可能性がある。
表2:NAFLDのための栄養および植物学的介入。 これらのような栄養素は修飾され、認可されたヘルスケアの従業者の指導の下で使用されるべきです。
| 栄養素 | 投与量 | メカニズム |
| ホスファチジルコリン(PC)、食事コリンの供給源 | 1.5gを食事とともに一日二回(PC)または200mgを一日二回(コリン) | コリンは一般的な食事欠乏症です。 PCは胆汁および保護胃腸粘膜の障壁の生産に必要です。 |
| ミルクシスルシード | 140-200mg一日一回-三回 | 肝保護。 肝臓のグルタチオンのレベルを支え、胆汁の塩の輸出ポンプ(BSEP)を安定させ、そしてFXRの細道を活動化させます。 |
| ベルベリンHCl | 500mg毎日二から三回 | 血清グルコースおよび脂質プロファイルを改善し、肝臓脂肪含有量を減少させる。 |
| 例えば、B.longum、B.bifidum、S.thermophilus、L.rhamnosus、L.acidophilus、およびLなどの菌株を含むプロバイオティクス。 plantarum | 毎日12億コロニー形成単位(Cfu) | 腸上皮バリア機能を改善し、腸および全身性炎症を減少させた。 |
| アセチルグルタチオン | 毎日300mg | 肝細胞の解毒能力を向上させます。 |
| N-アセチルシステイン(NAC) | 500-600mg一日二回、空腹時に最もよく摂取 | NACは脂質過酸化の伝播をブロックし、肝臓のグルタチオンレベルをサポートします。 |
| ビタミンE(トコフェロール)
または トコトリエノール |
400 食品と一緒に毎日1200IUに
200〜300mg食品と一緒に毎日二回 |
保護抗酸化物質。
トコトリエノールは、脂肪酸シンターゼおよびカルニチンパルミトイルトランスフェラーゼ酵素を調節することによってトリグリセリド蓄積を減衰させ、肝炎症および小胞体ストレスを減少させる。 |
| オメガ–3必須脂肪酸 | 毎日2-4g、食事付き | オメガ-3多価不飽和脂肪酸は、ステロール調節要素結合タンパク質-1cをダウンレギュレートし、ペルオキシソーム増殖因子活性化受容体αをアップレギュレートすることが知られており、脂肪酸の酸化を促進し、脂肪症を減少させる。 |