分子のルイス構造の執筆に戻る
共有結合分子の骨格構造は、構成原子の価数を考慮することによ 通常、結合の最大数を形成する原子は、骨格の中心に見出され、そこでは他の原子の最大数に接続することができる。
例1:次亜塩素酸は分子式HOClを有する。
構造式を描画します。
溶液原子をリンクするにはいくつかの可能な方法があります
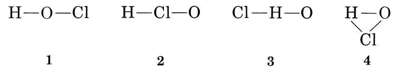
Hの通常の原子価は1であり、したがって、Hに2つの結合を有する構造3および4は、除去され得る。 Clの通常の原子価も1であるため、構造2も除外することができます。 構造1は、通常の原子価と一致して、Hが一つの結合を形成し、Clが一つを形成し、Oが二つを形成することを示しているので、それが選択される。
利用可能な価電子の総数は、Hから1プラス6からOプラス7からCl、または14です。 私たちが持っている骨格にこれらを埋める
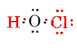
最大の原子価を持っていたOは、骨格の中心にあることに注意してください。
例2:
ヒドロキシルアミン、NH3Oの構造式を描きます。
この場合の溶液は、Nが最大の原子価(3)を持ち、その後にO(2)とH(1)が続きます。 NとOの両方が他の原子の間に「橋」を形成することができますが、Hはできません。 したがって、我々は与えるために骨格の中心にNとOを配置します
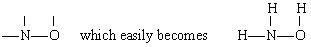
3つのH原子の付加によって。
の合計があります5 + 3 + 6 =14N、3HのとOからの価電子.これらは、次のように配置することができます:
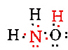
ルイス図が決定されると、構造式が何であるかを思い出させるために分子式が書き直されることがよくあります。 例えば、ヒドロキシルアミンの分子式は、通常、2つのHがNに結合し、1つがOに結合していることを思い出させるために、NH3Oの代わりにNH2OHと書かれています。 式を読んでいる人は、NとOがそれぞれ互いに共有するために残された1つの価電子を持ち、—NH2と—OHを接続していることを認識すると仮定されま いくつかのケースでは、複数の骨格構造は、同様に各原子とオクテット則の価数を満たすことになります。 たとえば、分子式C2H6Oが次の両方に対応していることを確認できます:
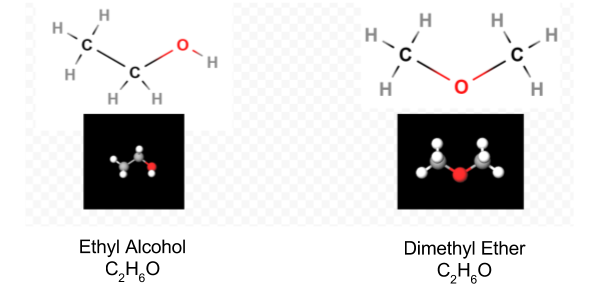
そのような場合、私たちは実験によってどの分子構造を持っているかを決定することができます。 水で希釈して消費したときのエチルアルコールの特性はよく知られている。 ジメチルエーテルは気体である。 手術室で使用されるジエチルエーテルのように、それは非常に爆発性であり、あなたを眠らせることができます。 ジメチルエーテルやエチルアルコールなど、同じ分子式を持つが構造式が異なる二つの分子は異性体であると言われています。
分子のルイス構造の執筆に戻る
謝辞:
C2H6O分子とその骨格構造はMolViewを使用して作成されました。