학습 목표
이 섹션이 끝날 때까지 다음을 수행 할 수 있습니다:
- 중성 원자와 이온에 대한 루이스 기호 쓰기
- 간단한 분자에서의 결합을 묘사하는 루이스 구조를 그립니다.
우리는 원자 및/또는 이온 사이에 형성되는 다양한 유형의 결합을 논의했습니다. 모든 경우에 이러한 결합은 원자 사이의 원자가 껍질 전자의 공유 또는 전달을 포함합니다. 이 섹션에서는 원자가 껍질 전자와 화학 결합,즉 루이스 기호와 루이스 구조를 묘사하는 전형적인 방법을 모색 할 것입니다.
루이스 기호
우리는 원자와 단 원자 이온의 원자가 전자 구성을 설명하기 위해 루이스 기호를 사용합니다. 루이스 기호는 원자가 전자 각각에 대해 하나의 점으로 둘러싸인 원소 기호로 구성됩니다:
그림 1 은 주기율표의 세 번째 기간의 요소에 대한 루이스 기호를 보여줍니다.

그림 1 을 읽습니다. 주기율표의 세 번째 기간에 각 원소에 대한 원자가 전자의 수를 보여주는 루이스 기호.
루이스 기호는 또한 나트륨과 칼슘에 대해 여기에 표시된 것처럼 원자에서 양이온의 형성을 설명하기 위해 사용될 수 있습니다:

마찬가지로 염소 및 황에 대해 아래 그림과 같이 원자에서 음이온 형성을 표시하는 데 사용할 수 있습니다.:

문자를 보여줍니다 그림 2 는 루이스 기호를 사용하여 이온 화합물을 형성하는 동안 전자의 전달을 보여줍니다.

그림 2 를 읽습니다. 양이온은 원자가 전자를 잃을 때 형성되는 반면,음이온은 전자를 얻는 원자에 의해 형성됩니다. 전자의 총 수는 변하지 않습니다.
루이스 구조
우리는 또한 루이스 구조,분자 및 다 원자 이온의 결합을 설명하는 도면에 표시된 공유 결합의 형성을 나타 내기 위해 루이스 기호를 사용합니다. 예를 들어,두 개의 염소 원자가 염소 분자를 형성 할 때 한 쌍의 전자를 공유합니다:

루이스 구조는 각 씨엘 원자가 결합에 사용되지 않는 3 쌍의 전자(고독한 쌍이라고 함)와 하나의 공유 전자 쌍(원자 사이에 쓰여짐)을 가지고 있음을 나타냅니다. 대시(또는 선)는 때때로 공유 된 전자 쌍을 나타내는 데 사용됩니다:

단일 공유 전자 쌍을 단일 결합이라고합니다. 각 씨엘 원자는 8 개의 원자가 전자와 상호 작용합니다:6 개는 고독한 쌍이고 2 개는 단일 결합입니다.
옥텟 규칙
다른 할로겐 분자(에프 2,브롬 2,난 2,및 엣 2)는 염소 분자의 결합과 같은 결합을 형성합니다:원자 사이에 하나의 단일 결합과 원자 당 3 개의 고독한 전자 쌍. 이를 통해 각 할로겐 원자는 고귀한 가스 전자 구성을 가질 수 있습니다. 8 개의 원자가 전자를 얻기에 충분한 결합을 형성하는 주요 그룹 원자의 경향은 옥텟 규칙으로 알려져 있습니다.
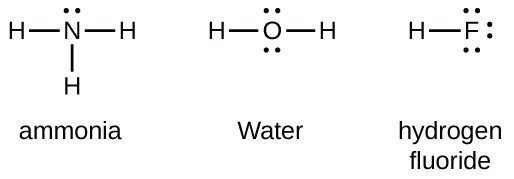
원자가 형성 할 수있는 결합의 수는 종종 옥텟(8 개의 원자가 전자)에 도달하는 데 필요한 전자의 수로부터 예측할 수 있습니다. 예를 들어,그룹 14 원소의 각 원자는 가장 바깥 쪽 껍질에 4 개의 전자를 가지고 있으므로 옥텟에 도달하기 위해 4 개의 전자가 더 필요합니다. 이 4 개의 전자는 4 개의 공유 결합을 형성함으로써 얻을 수 있습니다. 수소는 원자가 껍질을 채우기 위해 두 개의 전자 만 필요하기 때문에 옥텟 규칙의 예외입니다. 전환 요소와 내부 전환 요소도 옥텟 규칙을 따르지 않습니다:
이중 및 삼중 결합
앞에서 언급했듯이 한 쌍의 원자가 한 쌍의 전자를 공유 할 때이를 단일 결합이라고 부릅니다. 그러나 한 쌍의 원자는 필요한 옥텟을 달성하기 위해 한 쌍 이상의 전자를 공유해야 할 수도 있습니다. 이중 결합은 두 쌍의 전자가 한 쌍의 원자 사이에서 공유 될 때 형성되며,탄소(포름 알데히드)의 탄소와 산소 원자 사이와 탄소(에틸렌)의 두 탄소 원자 사이:
삼중 결합은 질소 가스(엔 2)에서와 같이 한 쌍의 원자에 의해 3 개의 전자쌍이 공유 될 때 형성됩니다):
옥텟 규칙
로 루이스 구조를 쓰는 것은 매우 단순한 분자와 분자 이온에 대해 구성 원자에 짝이없는 전자를 페어링함으로써 루이스 구조를 쓸 수 있습니다. 다음 예를 참조하십시오:

보다 복잡한 분자 및 분자 이온의 경우 여기에 설명 된 단계별 절차를 따르는 것이 도움이됩니다:
- 원자가(외피)전자의 총 수를 결정합니다.
- 분자의 골격 구조를 그려 중심 원자 주위에 원자를 배열합니다. (일반적으로,가장 작은 전기 음성도 성분은 센터에서 두어야 합니다.)각 원자를 단일 결합(하나의 전자쌍)으로 중앙 원자에 연결하십시오.
- 나머지 전자를 말단 원자(수소 제외)에 고독한 쌍으로 분배하여 각 원자 주위에 옥텟을 완성합니다.
- 나머지 모든 전자를 중심 원자에 놓습니다.
- 외부 원자의 전자를 재 배열하여 가능한 옥텟을 얻기 위해 중심 원자와 다중 결합을 만든다.
위의 단계를 사용하여 루이스의 구조를 결정합시다:
- 1 단계:원자가(외피)전자의 총 수를 결정합니다.
\큰\을 시작{array}{l}\\\팬텀{\규칙{0.8em}{0ex}}{\text{PBr}}_{3}\\\팬텀{\규칙{0.8em}{0ex}}\text{P:5 원자의 전자/atom}\번\text{1 원자}=5\\\밑줄{+\text{Br:7 원자가 전자/atom}\번\text{3 원자}=21}\\\\\팬텀{\규칙{15.이 경우 원자가 전자를 배열로 변환 할 수 있습니다.}
- 2 단계:분자의 골격 구조를 그려 중심 원자 주위에 원자를 배열합니다. (일반적으로,가장 작은 전기 음성도 성분은 센터에서 두어야 합니다.)각 원자를 단일 결합(하나의 전자쌍)으로 중앙 원자에 연결하십시오.

- 3 단계:나머지 전자를 말단 원자(수소 제외)에 고독한 쌍으로 분배하여 각 원자 주위에 옥텟을 완성합니다.
 4 단계:나머지 모든 전자를 중심 원자에 놓습니다.
4 단계:나머지 모든 전자를 중심 원자에 놓습니다.

참고:5 단계:모든 원자가 옥텟을 가지고 있기 때문에 필요하지 않습니다.
.
- 1 단계: 원자가(외피)전자의 총 수를 결정하십시오.
\원자가전자/원자 1 개,원자 2 개,원자 2 개,밑줄 4 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자/원자 1 개,원자가전자 이 경우,원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성 할 때 원자가 전자를 생성한다.}
- 2 단계:분자의 골격 구조를 그려 중심 원자 주위에 원자를 배열합니다. (일반적으로,가장 작은 전기 음성도 성분은 센터에서 두어야 합니다.)각 원자를 단일 결합(하나의 전자쌍)으로 중앙 원자에 연결하십시오.

- 3 단계:나머지 전자를 말단 원자(수소 제외)에 고독한 쌍으로 분배하여 각 원자 주위에 옥텟을 완성합니다.

- 4 단계:모든 전자가 배치 되었기 때문에 필요하지 않습니다. 그러나,탄소는 옥텟을 가지지 않는다,
- 5 단계: 가능한 옥텟을 얻기 위해 중심 원자와 여러 결합을 만들기 위해 외부 원자의 전자를 재 배열.

예 1:루이스 구조 작성
나사의 카시니-호이겐스 임무는 토성의 위성 중 하나 인 타이탄에서 독성 시안화 수소의 큰 구름을 발견했습니다. 이 분자의 루이스 구조는 무엇입니까?
학습 확인
이산화탄소,이산화탄소는 화석 연료의 연소의 산물입니다. 이산화탄소는 지구 기후 변화에 연루되어 있습니다. 이산화탄소의 루이스 구조는 무엇입니까?
주요 개념 및 요약
원자가 전자 구조는 루이스 기호(원자 및 단원자 이온의 경우)와 루이스 구조(분자 및 다원자 이온의 경우)를 그려서 시각화 할 수 있습니다. 고독한 쌍,짝이없는 전자 및 단일,이중 또는 삼중 결합은 원자가 전자가 루이스 구조의 각 원자 주위에 위치하는 위치를 나타내는 데 사용됩니다. 대부분의 구조—특히 두 번째 행 요소를 포함하는 구조-는 모든 원자(시간 제외)가 8 개의 전자로 둘러싸인 옥텟 규칙을 따릅니다. 홀수 전자 분자(자유 라디칼),전자 결핍 분자 및 다가 분자에 대해서는 옥텟 규칙의 예외가 발생합니다.
연습
- 다음 이온 각각에 대해 루이스 기호를 씁니다.:
- –
- Cl
- 나
- Mg
- 캘리포니아
- K
- Br
- Sr
- F
- MgS
- Al2O3
- GaCl3
- K2O
- Li3N
- KF
용어집
이중 결합:두 쌍의 전자가 두 원자 사이에서 공유되는 공유 결합
자유 라디칼:홀수의 전자를 포함하는 분자
가 분자:원자가 껍질에 8 개 이상의 전자를 가진 적어도 하나의 주요 그룹 요소를 포함하는 분자
루이스 구조:분자 또는 이온 내의 전자의 고독한 쌍과 결합 쌍을 보여주는 다이어그램
루이스 기호: 요소 또는 이온의 각 원자가 전자를 나타 내기 위해 점을 사용하는 요소 또는 단원 자 이온에 대한 기호
고독한 쌍:공유 결합을 형성하는 데 사용되지 않는 두 개의(한 쌍의)원자가 전자
옥텟 규칙:주요 그룹 원자가 8 개의 원자가 전자가 각 핵과 상호 작용하는 구조를 형성하고 결합 전자가 결합에 의해 연결된 두 원자와 상호 작용하는 것을 계산한다는 지침
단일 결합:전자 쌍은 두 원자 사이에서 공유
삼중 결합: 두 원자 사이에 세 쌍의 전자가 공유되는 결합


 전자가 남아 있지 않습니다.
전자가 남아 있지 않습니다.


















