Orbitalfyllingsdiagrammer
et orbitalfyllingsdiagram er den mer visuelle måten å representere arrangementet av alle elektronene i et bestemt atom. I et orbitalfyllingsdiagram vises de enkelte orbitaler som sirkler (eller firkanter), og orbitaler i et undernivå trekkes ved siden av hverandre horisontalt. Hvert undernivå er merket av sitt viktigste energinivå og undernivå. Elektroner er angitt med piler inne i sirklene. En pil som peker oppover indikerer en spinnretning, mens en pil som peker nedover indikerer den andre retningen. Orbitalfyllingsdiagrammer for hydrogen, helium og litium er vist i figuren nedenfor.
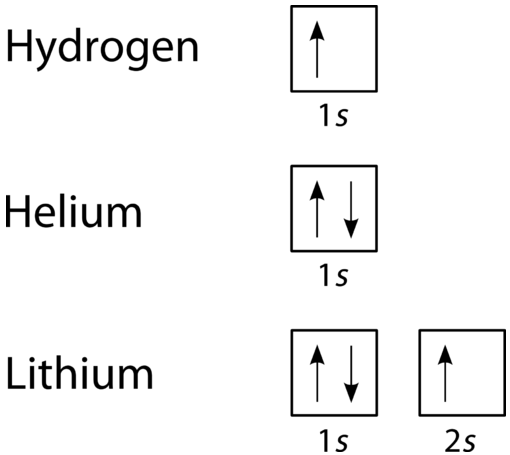
ifølge aufbau-prosessen er undernivåer og orbitaler fylt med elektroner i rekkefølge av økende energi. Siden\ (s\) sublevel består av bare en orbital, parrer den andre elektronen bare opp med den første elektronen som i helium. Det neste elementet er litium og krever bruk av neste tilgjengelige undernivå, \(2s\).
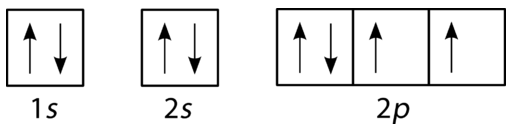
fyllingsdiagrammet for karbon er vist i figuren nedenfor. Det er to \(2p\) elektroner for karbon og hver har sin egen \(2p\) orbital.
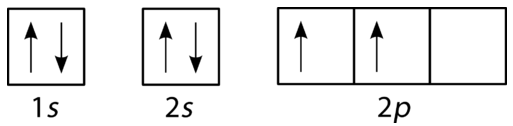
Oksygen har fire \(2p\) elektroner. Etter at hver \(2p\) orbital har en elektron i den, kan den fjerde elektronen plasseres i den første \ (2p\) orbitalen med et spinn motsatt det av den andre elektronen i den orbitalen.