Det er ikke åpenbart. Valenselektroner er de som er viktige i kjemisk binding. For overgangsmetaller vil ordet «viktig» variere avhengig av konteksten.
det er lettere og mer praktisk å beskrive hvilke orbitaler som er valensorbitaler når det gjelder overgangsmetaller (selv om det blir vanskelig med lantanider og aktinider).
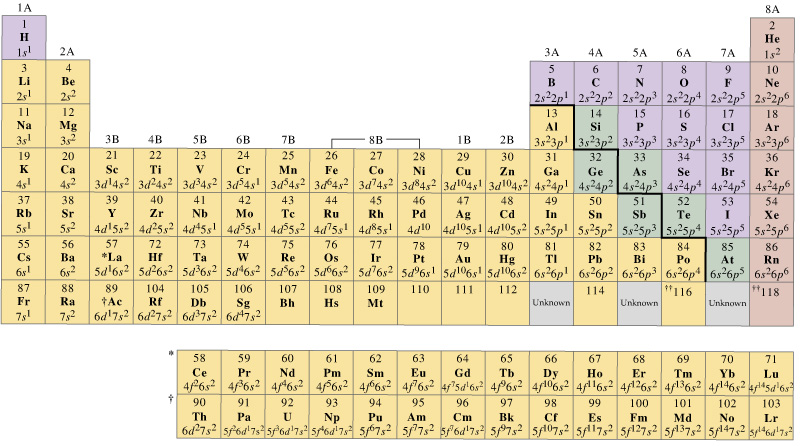
generelt har første rads overgangsmetaller et sett med valensorbitaler som inkluderer deres #4s # og # 3d#, men antall valenselektroner vil variere.
For eksempel…

- Scandium er fornuftig å ha opptil tre valenselektroner, siden en #»Sc»^(+3)# oksidasjonstilstand eksisterer (f. eks. #»ScCl»_3#), men ikke #» Sc » ^(+4)# eller høyere. En# + 3 # oksidasjonstilstand ville ha krevd overføring av tre valenselektroner hvis den skulle danne en ren kation.
- Krom kan ha opptil seks valenselektroner, som vil inkludere sine #3d# elektroner, siden det kan oppnå en# + 6 # oksidasjonstilstand (dvs. i # » Cr » _2 » O «_7^(2 -)#, eller i # «CrO»_4^(2-)#).
- Kobber har en tendens til å ha en #+1# oksidasjonstilstand (f. eks. #»CuCl»#), så det er fornuftig at Den bruker sin en # 4s # elektron oftest som sin valenselektron (er). Men en# + 2 #oksidasjonstilstand er også kjent (f.eks.# «CuCl»_2#), og så er den i stand til å ta fra sin# bb(3d) # elektroner også for sin valenselektron(er).
På den annen side kan vi lett si at valensorbitaler i første rads overgangsmetaller er #4s# og #3d# orbitaler.
så generelt vil jeg si at antall valenselektroner for overgangsmetaller (og lantanid og aktinider) varierer på en uforutsigbar måte, men valensorbitalene kan noen ganger forutsies med nok kjemisk intuisjon.
ANSVARSFRASKRIVELSE: det er imidlertid generelt vanskelig for lantanidene og aktinidene å forutsi hvilke orbitaler som er valens.
for eksempel har aktinidene #5f# og #6d# orbitaler veldig nært i energi til deres #7s # orbital, så vi KAN GJETTE og inkludere # 7s#, #6d # og # 5f # i valensrommet (selv om #6d# orbitaler er tomme) når vi utfører atomenergiberegninger.