diagramy wypełniania orbitali
diagram wypełniania orbitali jest bardziej wizualnym sposobem reprezentowania układu wszystkich elektronów w danym atomie. Na diagramie wypełniania orbitali poszczególne orbitale są pokazane jako okręgi (lub kwadraty), a orbitale w podpoziomie są rysowane obok siebie poziomo. Każdy podpoziom jest oznaczony przez jego główny poziom energii i podpoziom. Elektrony są wskazywane przez strzałki wewnątrz okręgów. Strzałka skierowana w górę wskazuje jeden kierunek obrotu, podczas gdy strzałka skierowana w dół wskazuje drugi kierunek. Orbitalne diagramy napełniania wodoru, helu i litu przedstawiono na rysunku poniżej.
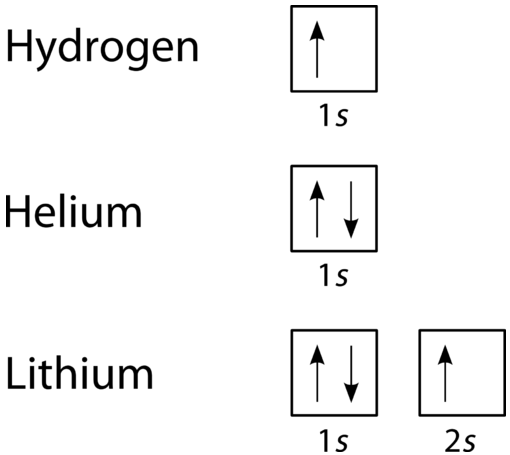
zgodnie z procesem Aufbau, podpoziomy i orbitale są wypełnione elektronami w kolejności zwiększania energii. Ponieważ podpoziom \(s\) składa się tylko z jednego orbitalu, drugi elektron po prostu paruje się z pierwszym elektronem, jak w Helu. Kolejnym elementem jest LIT i wymaga użycia następnego dostępnego podpoziomu, \(2s\).
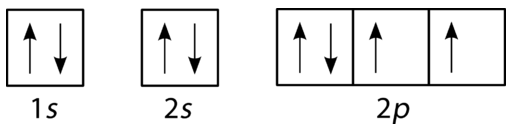
schemat napełniania węgla przedstawiono na rysunku poniżej. Istnieją dwa elektrony \(2P\) dla węgla i każdy zajmuje swój własny orbital \(2P\).
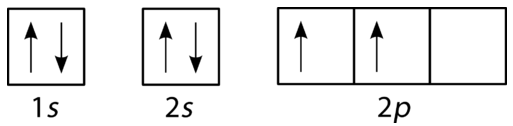
tlen ma cztery elektrony \(2P\). Po każdym\ (2P\) orbitalu ma jeden elektron w nim, czwarty elektron może być umieszczony w pierwszym \(2P\) orbitalu ze spinem przeciwnym do drugiego elektronu w tym orbitalu.