Velocità di reazione
Variazione di velocità quando si cambia l’alogeno
Velocità di reazione aumento nell’ordine HF – HCl – HBr – HI. Fluoruro di idrogeno reagisce molto più lentamente rispetto agli altri tre, ed è normalmente ignorato nel parlare di queste reazioni.
Quando gli alogenuri di idrogeno reagiscono con gli alcheni, il legame idrogeno-alogeno deve essere rotto. La forza di legame cade come si va da HF a HI, e il legame idrogeno-fluoro è particolarmente forte. Poiché è difficile rompere il legame tra l’idrogeno e il fluoro, l’aggiunta di HF è destinata ad essere lenta.
Variazione dei tassi quando si cambia l’alchene
Questo vale per alcheni asimmetrici e simmetrici. Per semplicità, gli esempi riportati di seguito sono tutti simmetrici, ma non devono esserlo.
I tassi di reazione aumentano man mano che l’alchene diventa più complicato, nel senso del numero di gruppi alchilici (come i gruppi metilici) attaccati agli atomi di carbonio alle due estremità del doppio legame. Ad esempio:
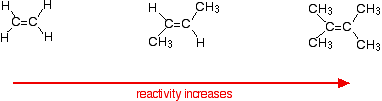
Ci sono due modi di guardare le ragioni di questo – entrambi i quali hanno bisogno di conoscere il meccanismo per le reazioni.
Gli alcheni reagiscono perché gli elettroni nel legame pi attraggono le cose con qualsiasi grado di carica positiva. Tutto ciò che aumenta la densità elettronica attorno al doppio legame aiuterà questo.
I gruppi alchilici hanno la tendenza a” spingere ” gli elettroni lontano da se stessi verso il doppio legame. Più gruppi alchilici hai, più negativa diventa l’area intorno ai doppi legami.
Più la regione diventa carica negativamente, più attirerà molecole come l’acido cloridrico.
La ragione più importante, tuttavia, risiede nella stabilità dello ion intermedio formato durante la reazione. I tre esempi sopra riportati producono queste carbocazioni (ioni di carbonio) nella fase a metà della reazione:
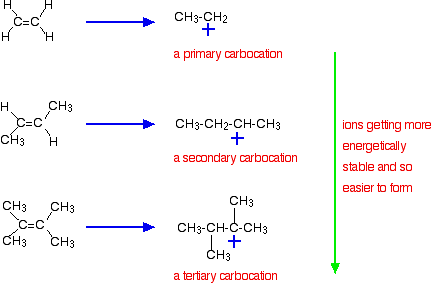
La stabilità degli ioni intermedi governa l’energia di attivazione per la reazione. Mentre vai verso gli alcheni più complicati, l’energia di attivazione per la reazione cade. Ciò significa che le reazioni diventano più veloci.