Orbital Fyldningsdiagrammer
et orbital fyldningsdiagram er den mere visuelle måde at repræsentere arrangementet af alle elektroner i et bestemt atom. I et kredsløbsfyldningsdiagram vises de enkelte orbitaler som cirkler (eller firkanter), og orbitaler inden for et underniveau tegnes ved siden af hinanden vandret. Hvert underniveau er mærket med dets primære energiniveau og underniveau. Elektroner er angivet med pile inde i cirklerne. En pil, der peger opad, angiver en spinretning, mens en pil nedad angiver den anden retning. Kredsløbsfyldningsdiagrammerne for hydrogen, helium og lithium er vist i nedenstående figur.
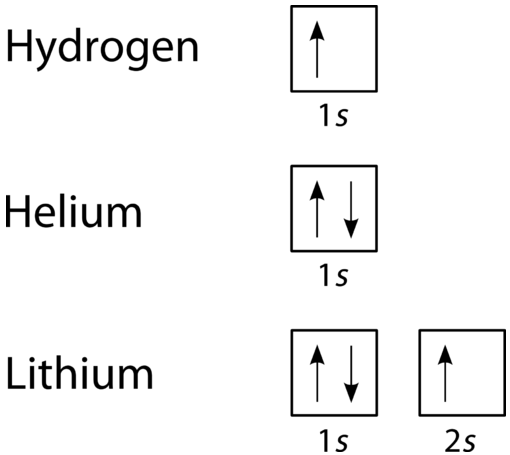
ifølge Aufbau-processen er underniveauer og orbitaler fyldt med elektroner i rækkefølge af stigende energi. Da\ (s\) underniveauet består af kun en orbital, parrer den anden elektron simpelthen op med den første elektron som i helium. Det næste element er lithium og nødvendiggør brugen af det næste tilgængelige underniveau, \(2s\).
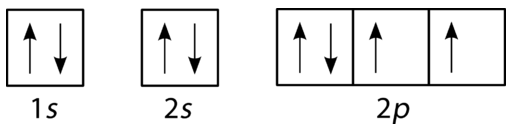
påfyldningsdiagrammet for kulstof er vist i nedenstående figur. Der er to \(2P\) elektroner til kulstof og hver optager sin egen \(2p\) orbital.
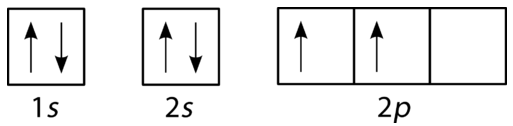
ilt har fire \(2p\) elektroner. Efter hver \(2p\) orbital har en elektron i sig, kan den fjerde elektron placeres i den første \(2p\) orbital med et spin modsat det for den anden elektron i den orbital.