tilbage til skrivning af Levis-strukturer for molekyler
skeletstrukturen i et kovalent molekyle kan ofte bestemmes ved at overveje valenserne af de bestanddele, der indgår. Normalt findes atomet, der danner det største antal bindinger, i midten af skeletet, hvor det kan forbinde til det maksimale antal andre atomer.
eksempel 1: Hypochlorsyre har molekylformlen HOCl. Tegn en
strukturformel.
løsning der er flere mulige måder at forbinde atomerne sammen
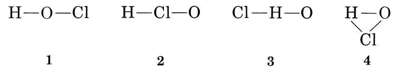
den sædvanlige valens af H er 1, og så strukturer 3 og 4, som har to bindinger til H, kan elimineres. Den sædvanlige valens af Cl er også 1, og så kan struktur 2 også udelukkes. Struktur 1 viser h danner en binding, Cl danner en, og O danner to, i overensstemmelse med de sædvanlige valenser, og så er det valgt.
det samlede antal tilgængelige valenselektroner er 1 fra H plus 6 fra O plus 7 fra Cl eller 14. Udfyldning af disse i det skelet, vi har
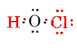
Bemærk, at O, som havde den største valens, er i midten af skeletet.
eksempel 2:
Tegn en strukturformel for hydroksylamin, NH3O.
opløsning i dette tilfælde n har den største Valens (3) efterfulgt af O (2) og H (1). Både N og O kan danne “broer” mellem andre atomer, men H kan ikke. Derfor placerer vi N og O i midten af skeletet for at give
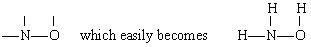
ved tilsætning af de tre H-atomer.
der er i alt 5 + 3 + 6 = 14 valenselektroner fra N, 3H og O. disse kan placeres som følger:
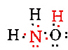
når først diagrammet er bestemt, omskrives molekylformlen ofte for at minde os om, hvad strukturformlen er. For eksempel skrives molekylformlen for hydroksylamin normalt NH2OH i stedet for NH3O for at minde os om, at to H ‘ er er bundet til N og en til O. Det antages, at den person, der læser formlen, vil indse, at N og O hver har en valenselektron tilbage til at dele med hinanden og forbinde —NH2 med —OH. I nogle tilfælde vil mere end en skeletstruktur også tilfredsstille valensen af hvert atom og oktetreglen. For eksempel kan du kontrollere, at molekylformlen C2H6O svarer til begge følgende:
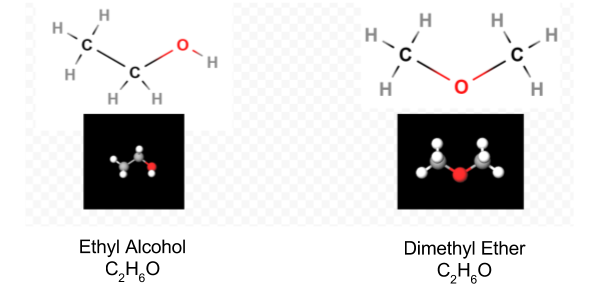
i et sådant tilfælde kan vi kun bestemme, hvilken molekylær struktur vi har ved eksperiment. Egenskaberne af ethylalkohol, når de fortyndes med vand og forbruges, er velkendte. Dimethylether er en gas. Ligesom den diethylether, der bruges i operationsstuer, er den meget eksplosiv og kan få dig til at sove. To molekyler, såsom dimethylether og ethylalkohol, som har den samme molekylformel, men forskellige strukturelle formler siges at være isomerer.
tilbage til skrivning af strukturer for molekyler
anerkendelser:
c2h6o-molekylerne og deres skeletstrukturer blev oprettet ved hjælp af Molvisning.