Generischer Name: Diphenhydraminhydrochlorid, Lidocainhydrochlorid, Aluminiumhydroxid, Magnesiumhydroxid
Darreichungsform: Oral Compoundierung Kit
Medizinisch überprüft von Drugs.com . Zuletzt aktualisiert am September 21, 2020.
- Professional
- Wechselwirkungen
- Bewertungen
- Mehr
Haftungsausschluss: Dieses Medikament wurde von der FDA nicht als sicher und wirksam befunden, und diese Kennzeichnung wurde von der FDA nicht genehmigt. Weitere Informationen zu nicht zugelassenen Medikamenten finden Sie hier.
FIRST ® – Mundwasser BLM Rx
Diphenhydramin HCl, Lidocain HCl, Aluminiumhydroxid, Magnesiumhydroxid und Simethicon Compoundierung Kit
NUR FÜR VERSCHREIBUNGSPFLICHTIGE COMPOUNDIERUNG
Auf dieser Seite
First Mouthwash BLM Beschreibung
Jedes FIRST®— Mouthwash BLM Compoundierkit besteht aus 0,2 Gramm Diphenhydraminhydrochlorid-Pulver USP und 1,6 Gramm Lidocainhydrochlorid-Pulver USP zur oralen Anwendung.* FIRST®— Mouthwash BLM Compounding Kit enthält außerdem eine 236 ml Suspension mit 3,15 g Aluminiumhydroxid USP (entspricht getrocknetem Gel USP), 3,15 g Magnesiumhydroxid USP und 0,315 g Simethicon USP mit Benzylalkohol, Butylparaben, Aroma, Hydroxyethylcellulose, Propylparaben, gereinigtem Wasser, Saccharin-Natrium, Sorbitollösung, D & C red # 28 und FD & C rot #40.* Wenn das Endprodukt compoundiert wird, ergibt es eine homogene Suspension, die Diphenhydraminhydrochlorid, Lidocainhydrochlorid und Aluminiumhydroxid, Magnesiumhydroxid und Simethicon enthält, vergleichbar mit den Wirkstoffen (Benadryl®, Lidocain HCl 2% viskos, Maalox® 1:1:1), die in Magic Mouthwash enthalten sind.**
Wie Geliefert und Compoundierung Richtungen
| Größe | 8 FL OZ (237 ml) |
| NDC# | 65628-050-01 |
| Diphenhydramin HCl | 0.2g |
| Lidocain HCl | 1,6 g |
| FIRST®-Mundwassersuspension | 236 ml |
AN DEN APOTHEKER
Alles, was Sie dazu brauchen, ist enthalten…
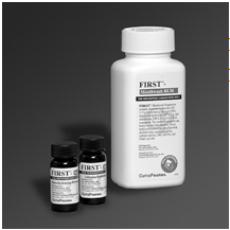
1. FIRST®- Mouthwash BLM Compounding Kit enthält vorgemessenes Diphenhydraminhydrochlorid-Pulver, Lidocainhydrochlorid-Pulver und Mundwassersuspension (Aluminiumhydroxid, Magnesiumhydroxid, Simethicon plus inaktive Inhaltsstoffe)

2. Wichtig – Klopfen Sie vor der Abgabe auf die Ober- und Unterseite der Flasche mit Diphenhydraminhydrochlorid, um das Pulver zu lösen und die Kappe zu entfernen. Leeren Sie das Diphenhydraminhydrochlorid-Pulver in die Flasche mit der flüssigen Mundwassersuspension. Ebenso klopfen Sie die Oberseite und die Unterseite der Flasche, die Lidocainhydrochlorid enthält, um das Pulver zu lösen und die Kappe zu entfernen. Leeren Sie das Lidocainhydrochlorid-Pulver in die Flasche mit der flüssigen Mundwassersuspension.
Die entsprechenden Mengen an Diphenhydraminhydrochlorid-Pulver und Lidocainhydrochlorid-Pulver wurden in jeder Flasche verpackt, um die erforderliche Dosierung jedes Arzneimittels zu liefern. Restmengen, die nach dem Entleeren in den Flaschen verbleiben, müssen nicht ausgespült werden.

3. Schließen Sie die Flasche und schütteln Sie sie 20 bis 30 Sekunden lang. Weisen Sie den Patienten an, die Flasche vor jedem Gebrauch gut zu schütteln.
Lagern Sie FIRST®- Mouthwash BLM Compounding Kit vor dem Compoundieren bei Raumtemperatur zwischen 15°-30°C (59°-86°F). Lagern Sie die endgültige Formulierung auch bei Raumtemperatur, 15 ° -30 ° C (59 ° -86 ° F).
FIRST®- Mouthwash BLM Compounding Kit Komponenten haben ein Verfallsdatum von drei Jahren.*** Basierend auf echtzeitgesteuerten Raumtemperatur— und Feuchtigkeitstests ist compounded FIRST®- Mouthwash BLM Compounding Kit für mindestens sechs Monate stabil.***
FIRST®- Mouthwash suspension erfüllt die Anforderungen für die aerobe Gesamtmikrobenzahl von nicht mehr als 100 KBE/ml sowie für das Fehlen der angegebenen Mikroorganismen Escherichia coli, Pseudomonas aeruginosa, Staphylococcus aureus und Salmonella spp. wenn getestet, wie in der aktuellen USP unter <61> Microbial Enumeration Tests und <62> Tests für spezifizierte Mikroorganismen beschrieben. FIRST®- Mouthwash Suspension erfüllt auch die Anforderungen, wie sie in der aktuellen USP unter <51> Antimikrobielle Wirksamkeitsprüfung für Produkte der Kategorie 4 beschrieben sind.
Nur zum Einnehmen. Kontakt mit den Augen vermeiden. Behälter dicht verschlossen halten. Darf nicht in die Hände von Kindern gelangen. Vor Licht schützen. Vor dem Einfrieren schützen. Compoundiertes Produkt, wie es dosiert wird, ist mindestens 180 Tage bei Raumtemperatur stabil.
* Analysenzertifikat auf Datei
** Dieses Produkt wird nicht von Pfizer, Inc. hergestellt., Hersteller von Benadryl® oder von Novartis Consumer Health, Inc. hersteller von Maalox®
*** Daten und Dokumentation auf Datei
RX ONLY
Revised: February 2010
U.S. Patent No. 6,708,822 B1
Zusätzliches US-Patent angemeldet
Vertrieben von:
CutisPharma, Inc.
INTELLIGENTE PRODUKTE FÜR INTELLIGENTE MENSCHEN®
Woburn, MA 01801, USA www.cutispharma.com
PRINCIPAL DISPLAY PANEL
NDC 65628-050-01
FIRST® Mouthwash BLM
Jedes Kit enthält:
Wirkstoffe:
Diphenhydraminhydrochlorid 0,2 g
Lidocainhydrochlorid 1,6 g
Aluminiumhydroxid 3,15 g in 236 ml Suspension (entspricht getrocknetem Gel USP)
Magnesiumhydroxid 3,15 g in 236 ml Suspension
Simethicon 0.315g in 236mL suspension
8 FL OZ (237 mL) as dispensed

| First Mouthwash BLM diphenhydramine hydrochloride and lidocaine hydrochloride and aluminum hydroxide and magnesium hydro kit |
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
Teil 1 von 3 LIDOCAINHYDROCHLORID
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
Teil 2 von 3 ERSTE MUNDWASSERSUSPENSION
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
Teil 3 von 3 DIPHENHYDRAMINE HYDROCHLORIDE
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
|
||||||||||||||||||||||
Labeler – CutisPharma, Inc. (090598256)
More about FIRST Mouthwash BLM (aluminum hydroxide / diphenhydramine / lidocaine / magnesium hydroxide / simethicone topical)
- Drug Interactions
- 2 Reviews
- Drug class: mund- und Rachen-Produkte
Zugehörige Behandlungsanleitungen
- Aphthengeschwür
Medizinischer Haftungsausschluss