Tasas de reacción
Variación de tasas cuando se cambia el halógeno
Las tasas de reacción aumentan en el orden HF-HCl – HBr-HI. El fluoruro de hidrógeno reacciona mucho más lentamente que los otros tres, y normalmente se ignora al hablar de estas reacciones.
Cuando los haluros de hidrógeno reaccionan con alquenos, el enlace hidrógeno-halógeno tiene que romperse. La fuerza de enlace disminuye a medida que se pasa de HF a HI, y el enlace hidrógeno-flúor es particularmente fuerte. Debido a que es difícil romper el enlace entre el hidrógeno y el flúor, la adición de HF está destinada a ser lenta.
Variación de las tasas cuando se cambia el alqueno
Esto se aplica a alquenos asimétricos, así como a alquenos simétricos. Para simplificar, los ejemplos que se dan a continuación son todos simétricos, pero no tienen que serlo.
Las tasas de reacción aumentan a medida que el alqueno se complica, en el sentido del número de grupos alquilos (como grupos metilo) unidos a los átomos de carbono en cada extremo del doble enlace. Por ejemplo:
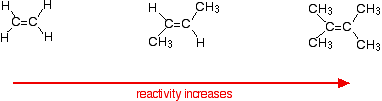
Hay dos maneras de ver las razones de esto, las cuales necesitan que conozca el mecanismo de las reacciones.
Los alquenos reaccionan porque los electrones en el enlace pi atraen cosas con cualquier grado de carga positiva. Cualquier cosa que aumente la densidad electrónica alrededor del doble enlace ayudará a esto.
Los grupos alquilos tienen una tendencia a» empujar » electrones lejos de sí mismos hacia el doble enlace. Cuantos más grupos alquilos tenga, más negativa se volverá el área alrededor de los dobles enlaces.
Cuanto más cargada negativamente se vuelva esa región, más atraerá moléculas como el cloruro de hidrógeno.
La razón más importante, sin embargo, radica en la estabilidad del ion intermedio formado durante la reacción. Los tres ejemplos anteriores producen estas carbocaciones (iones de carbonio) en la etapa intermedia de la reacción:
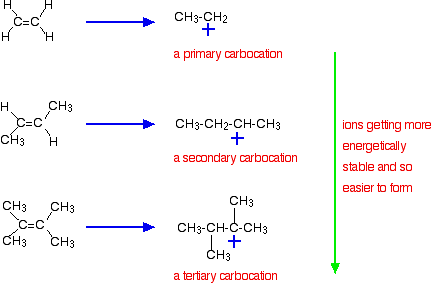
La estabilidad de los iones intermedios gobierna la energía de activación de la reacción. A medida que avanzas hacia los alquenos más complicados, la energía de activación para la reacción disminuye. Eso significa que las reacciones se vuelven más rápidas.