no es obvio. Los electrones de valencia son los que son importantes en la unión química. Para los metales de transición, la palabra «importante» variará según el contexto.
Es más fácil y práctico describir qué orbitales son orbitales de valencia cuando se trata de metales de transición (aunque se vuelve difícil con lantánidos y actínidos).
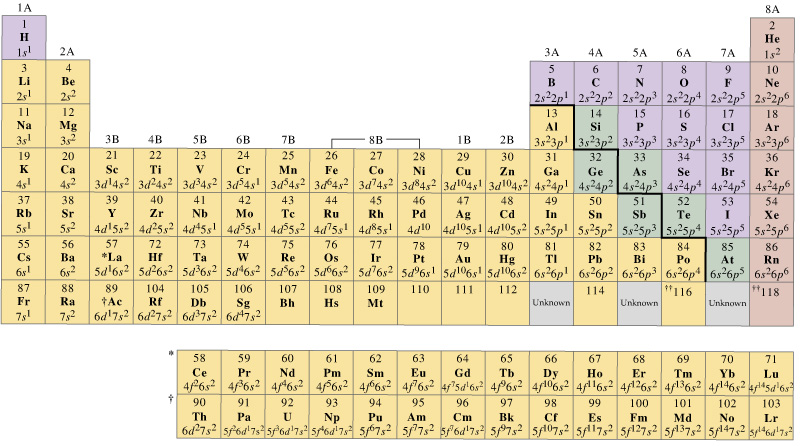
En general, los metales de transición de primera fila tienen un conjunto de orbitales de valencia que incluyen sus # 4s# y # 3d#, pero el número de electrones de valencia variará.
Por ejemplo…

- El escandio tiene sentido para tener hasta tres electrones de valencia, ya que existe un estado de oxidación #»Sc»^(+3)# (por ejemplo, #»ScCl»_3#), pero no #»Sc»^(+4)# o superior. Un estado de oxidación #+3# habría requerido la transferencia de tres electrones de valencia si se formara un catión puro.
- El cromo podría tener hasta seis electrones de valencia, que incluirían sus electrones #3d#, ya que puede lograr un estado de oxidación #+6# (es decir, en #»Cr»_2″O»_7^(2 -)#, o en # «CrO»_4^(2-)#).
- El cobre tiende a tener un estado de oxidación # + 1# (por ejemplo, #»CuCl»#), por lo que tiene sentido que use su electrón #4s# más a menudo como su electrón(s) de valencia. Pero también se conoce un estado de oxidación #+2# (por ejemplo, # «CuCl» _2#), por lo que es capaz de tomar de sus electrones #bb(3d)# también por su electrón(s) de valencia.
Por otro lado, podríamos decir fácilmente que los ORBITALES de valencia de los metales de transición de primera fila son los orbitales #4s# y #3d#.
Así que, en general, diría que el número de electrones de valencia para metales de transición (y lantánidos y actínidos) varía de manera impredecible, pero los orbitales de valencia a veces se pueden predecir con suficiente intuición química.
DESCARGO DE RESPONSABILIDAD: Sin embargo, en general es difícil para los lantánidos y actínidos predecir qué orbitales son valencia.
Por ejemplo, los actínidos tienen orbitales #5f# y #6d# muy cercanos en energía a sus orbitales #7s#, por lo que podemos ADIVINAR e incluir los #7s#, #6d# Y #5f# en el espacio de valencia (incluso si los orbitales #6d# están vacíos) al realizar cálculos de energía atómica.