Objetivos de aprendizaje
Al final de esta sección, podrá::
- Escribir símbolos de Lewis para átomos e iones neutrales
- Dibujar estructuras de Lewis que representen la unión en moléculas simples
Hemos discutido los diversos tipos de enlaces que se forman entre átomos y/o iones. En todos los casos, estos enlaces implican compartir o transferir electrones de la capa de valencia entre átomos. En esta sección, exploraremos el método típico para representar electrones de capas de valencia y enlaces químicos, a saber, símbolos de Lewis y estructuras de Lewis.
Símbolos de Lewis
Utilizamos símbolos de Lewis para describir configuraciones electrónicas de valencia de átomos e iones monatómicos. Un símbolo de Lewis consiste en un símbolo elemental rodeado por un punto para cada uno de sus electrones de valencia:
La figura 1 muestra los símbolos de Lewis para los elementos del tercer período de la tabla periódica.

Figura 1. Símbolos de Lewis que ilustran el número de electrones de valencia para cada elemento en el tercer período de la tabla periódica.
Los símbolos de Lewis también se pueden usar para ilustrar la formación de cationes a partir de átomos, como se muestra aquí para el sodio y el calcio:

Asimismo, se pueden usar para mostrar la formación de aniones a partir de átomos, como se muestra a continuación para el cloro y el azufre:

La figura 2 muestra el uso de símbolos de Lewis para mostrar la transferencia de electrones durante la formación de compuestos iónicos.

Figura 2. Los cationes se forman cuando los átomos pierden electrones, representados por menos puntos de Lewis, mientras que los aniones se forman cuando los átomos ganan electrones. El número total de electrones no cambia.
Estructuras de Lewis
También utilizamos símbolos de Lewis para indicar la formación de enlaces covalentes, que se muestran en estructuras de Lewis, dibujos que describen el enlace en moléculas e iones poliatómicos. Por ejemplo, cuando dos átomos de cloro forman una molécula de cloro, comparten un par de electrones:

La estructura de Lewis indica que cada átomo Cl tiene tres pares de electrones que no se utilizan en la unión (llamados pares solitarios) y un par de electrones compartidos (escritos entre los átomos). Un guión (o línea) a veces se usa para indicar un par de electrones compartidos:

Un solo par de electrones compartidos se denomina enlace único. Cada átomo Cl interactúa con ocho electrones de valencia: los seis en los pares solitarios y los dos en el enlace simple.
La Regla de octetos
Las otras moléculas halógenas (F2, Br2, I2 y At2) forman enlaces como los de la molécula de cloro: un enlace simple entre átomos y tres pares solitarios de electrones por átomo. Esto permite que cada átomo halógeno tenga una configuración electrónica de gas noble. La tendencia de los átomos del grupo principal a formar suficientes enlaces para obtener ocho electrones de valencia se conoce como la regla del octeto.
El número de enlaces que un átomo puede formar a menudo se puede predecir a partir del número de electrones necesarios para alcanzar un octeto (ocho electrones de valencia); esto es especialmente cierto para los no metálicos del segundo período de la tabla periódica (C, N, O y F). Por ejemplo, cada átomo de un elemento del grupo 14 tiene cuatro electrones en su capa exterior y, por lo tanto, requiere cuatro electrones más para alcanzar un octeto. Estos cuatro electrones se pueden obtener formando cuatro enlaces covalentes, como se ilustra aquí para el carbono en CCl4 (tetracloruro de carbono) y el silicio en SiH4 (silano). Debido a que el hidrógeno solo necesita dos electrones para llenar su envoltura de valencia, es una excepción a la regla del octeto. Los elementos de transición y los elementos de transición interna tampoco siguen la regla del octeto:

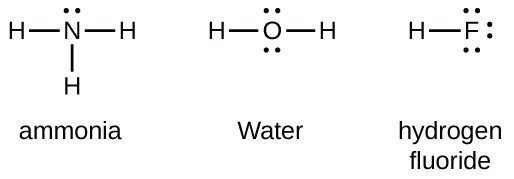
Los elementos del grupo 15, como el nitrógeno, tienen cinco electrones de valencia en el símbolo atómico de Lewis: un par solitario y tres electrones no apareados. Para obtener un octeto, estos átomos forman tres enlaces covalentes, como en NH3 (amoníaco). El oxígeno y otros átomos del grupo 16 obtienen un octeto formando dos enlaces covalentes:
Enlaces dobles y Triples
Como se mencionó anteriormente, cuando un par de átomos comparte un par de electrones, lo llamamos enlace simple. Sin embargo, un par de átomos puede necesitar compartir más de un par de electrones para lograr el octeto requerido. Un doble enlace se forma cuando dos pares de electrones se comparten entre un par de átomos, como entre los átomos de carbono y oxígeno en CH2O (formaldehído) y entre los dos átomos de carbono en C2H4 (etileno):
Un enlace triple se forma cuando tres pares de electrones son compartidos por un par de átomos, como en el gas nitrógeno (N2):
Escribiendo Estructuras de Lewis con la Regla de Octetos
Para moléculas muy simples e iones moleculares, podemos escribir las estructuras de Lewis simplemente emparejando los electrones no emparejados en los átomos constituyentes. Vea estos ejemplos:

Para moléculas e iones moleculares más complicados, es útil seguir el procedimiento paso a paso descrito aquí:
- Determinar el número total de electrones de valencia (capa exterior).
- Dibuja una estructura esquelética de la molécula, ordenando los átomos alrededor de un átomo central. (Generalmente, el elemento menos electronegativo debe colocarse en el centro.) Conecte cada átomo al átomo central con un enlace simple (un par de electrones).
- Distribuir los electrones restantes como pares solitarios en los átomos terminales (excepto el hidrógeno), completando un octeto alrededor de cada átomo.
- Coloque todos los electrones restantes en el átomo central.
- Reorganizar los electrones de los átomos externos para hacer múltiples enlaces con el átomo central con el fin de obtener octetos siempre que sea posible.
Determinemos la estructura de Lewis de PBr3 utilizando los pasos anteriores:
- Paso 1: Determine el número total de electrones de valencia (capa exterior).
\gran \begin{array}{l}\\ \phantom{\rule{0.8 em}{0ex}}{\text{PBr}}_{3}\\ \phantom{\rule{0.8 em}{0ex}}\text{P: 5 electrones de valencia/atom}\times \text{1 átomo}=5\\ \underline{+\text{Br: 7 electrones de valencia/atom}\times \text{3 átomos}=21}\\ \\ \phantom{\rule{15.95em}{0ex}}= \ text{26 electrones de valencia} \ end{matriz}
- Paso 2: Dibuja una estructura de esqueleto de la molécula, organizando los átomos alrededor de un átomo central. (Generalmente, el elemento menos electronegativo debe colocarse en el centro.) Conecte cada átomo al átomo central con un enlace simple (un par de electrones).

- Paso 3: Distribuye los electrones restantes como pares solitarios en los átomos terminales (excepto el hidrógeno), completando un octeto alrededor de cada átomo.
-
 Paso 4: Coloque todos los electrones restantes en el átomo central.
Paso 4: Coloque todos los electrones restantes en el átomo central.

Nota: Paso 5: No es necesario ya que todos los átomos tienen un octeto.
Determinemos la estructura de Lewis de CH2O.
- Paso 1: Determine el número total de electrones de valencia (capa exterior).
\gran \begin{array}{l}\\ \phantom{\rule{0.8 em}{0ex}}{\text{H}_{2}}\text{CO}\\ \phantom{\rule{0.8 em}{0ex}}\text{H: 1 electrón de valencia/átomo}\times \text{2 átomo}=2\\\text{C: 4 electrones de valencia/átomo}\times \text{1 átomo}=4\\ \subrayado{+\text{O: 6 electrones de valencia/átomo}\tiempos \text{1 átomos}=6}\\ \\ \phantom{\rule{15.95 em}{0ex}}=\text{12 electrones de valencia}\end{matriz}
- Paso 2: Dibuja una estructura de esqueleto de la molécula, organizando los átomos alrededor de un átomo central. (Generalmente, el elemento menos electronegativo debe colocarse en el centro.) Conecte cada átomo al átomo central con un enlace simple (un par de electrones).

- Paso 3: Distribuye los electrones restantes como pares solitarios en los átomos terminales (excepto el hidrógeno), completando un octeto alrededor de cada átomo.

- Paso 4: No es necesario, ya que se han colocado todos los electrones. Sin embargo, el carbono no tiene un octeto,
- Paso 5: Reorganiza los electrones de los átomos externos para hacer múltiples enlaces con el átomo central con el fin de obtener octetos siempre que sea posible.

Ejemplo 1: Escribiendo Estructuras de Lewis
La misión Cassini-Huygens de la NASA detectó una gran nube de cianuro de hidrógeno tóxico (HCN) en Titán, una de las lunas de Saturno. ¿Cuáles son las estructuras de Lewis de estas moléculas?
El dióxido de carbono, CO2, es un producto de la combustión de combustibles fósiles. El CO2 se ha visto implicado en el cambio climático mundial. ¿Cuál es la estructura de Lewis del CO2?
Conceptos clave y resumen
Las estructuras electrónicas de Valencia se pueden visualizar dibujando símbolos de Lewis (para átomos e iones monatómicos) y estructuras de Lewis (para moléculas e iones poliatómicos). Pares solitarios, electrones no emparejados y enlaces simples, dobles o triples se utilizan para indicar dónde se encuentran los electrones de valencia alrededor de cada átomo en una estructura de Lewis. La mayoría de las estructuras, especialmente las que contienen elementos de segunda fila, obedecen la regla del octeto, en la que cada átomo (excepto H) está rodeado por ocho electrones. Las excepciones a la regla de octetos ocurren para moléculas de electrones impares (radicales libres), moléculas deficientes de electrones e hipervalentes.
Ejercicios
- Escribir los símbolos de Lewis para cada uno de los siguientes iones:
- As3–
- I–
- Be2+
- O2
- Ga3+
- Li+
- N3–
- Muchos iones monoatómicos se encuentran en el agua de mar, incluidos los iones formados a partir de la siguiente lista de elementos. Escriba los símbolos de Lewis para los iones monoatómicos formados a partir de los siguientes elementos:
- Cl
- Na
- Mg
- Ca
- K
- Br
- Sr
- F
- Escribir los símbolos de Lewis de los iones en cada uno de los siguientes compuestos iónicos y los símbolos de Lewis del átomo del que se forman:
- Mg
- Al2O3
- GaCl3
- K2O
- Li3N
- KF
- En las estructuras de Lewis enumerados a continuación, M y X representan diversos elementos en el tercer período de la tabla periódica. Escriba la fórmula de cada compuesto utilizando los símbolos químicos de cada elemento:
- Escribe la estructura de Lewis para la molécula diatómica P2, una forma inestable de fósforo que se encuentra en el vapor de fósforo a alta temperatura.
- Escribir estructuras de Lewis para los siguientes:
- H2
- HBr
- PCl3
- Escribir estructuras de Lewis para los siguientes:
- O2
- H2CO
- AsF3
- SiCl4
Glosario
enlace doble: enlace covalente en el que se comparten dos pares de electrones entre dos átomos
radical libre: molécula que contiene un número impar de electrones
molécula hipervalente: molécula que contiene al menos un elemento del grupo principal que tiene más de ocho electrones en su envoltura de valencia
Estructura de Lewis: diagrama que muestra pares solitarios y pares de electrones enlazantes en una molécula o un ion
Símbolo de Lewis: símbolo de un elemento o ion monatómico que usa un punto para representar cada electrón de valencia en el elemento o ion
par solitario: dos (un par de) electrones de valencia que no se utilizan para formar un enlace covalente
regla de octetos: guía que establece que los átomos del grupo principal formarán estructuras en las que ocho electrones de valencia interactúan con cada núcleo, contando los electrones de enlace como interactuando con ambos átomos conectados por el enlace
enlace simple: enlace en el que una un solo par de electrones se comparte entre dos átomos
enlace triple: enlace en el que tres pares de electrones se comparten entre dos átomos


 HCN: no quedan electrones
HCN: no quedan electrones




















