Introducción
La enfermedad de Peyronie (EP) es un trastorno localizado del tejido conectivo del pene que cicatriza las heridas y se caracteriza por la cicatrización de la túnica albugínea. Esta cicatriz fibrosa inelástica provoca dolor en el pene, deformidad en el pene y disfunción eréctil (DE) con dificultad para realizar el coito. François de la Peyronie describió por primera vez la enfermedad en 1743, cuando era cirujano de Luis XIV de Francia. Aunque estudios anteriores informaron una incidencia de 0,3-0,7%, publicaciones recientes han mostrado una incidencia general de 3,2-8,9%, con más del 75% de los casos en hombres entre 45 y 65 años de edad (1,2). Cabe destacar que el 10% de los pacientes experimentan el inicio de los síntomas antes de los 40 años de edad (2). Además, se ha informado que la incidencia de DP después de una prostatectomía radical es de hasta 15,9%, y un estudio reciente mostró que la curvatura del pene es un hallazgo común (38,6%) en el momento de la cirugía de implantación de prótesis de pene inflables para la disfunción eréctil después del tratamiento del cáncer de próstata (3,4).
El tratamiento para la EP comienza con una historia clínica enfocada y un examen físico. Una historia clínica detallada debe evaluar la información sobre el inicio y la duración de la enfermedad, la etiología traumática asociada, el grado de curvatura del pene, la pérdida de longitud durante la erección y el nivel subjetivo de la función sexual. Con respecto a la evaluación sexual subjetiva, los cuestionarios estandarizados como el Índice Internacional de Función Eréctil (IIEF) permiten evaluaciones iniciales objetivas y subjetivas y una herramienta para medir la eficacia durante el tratamiento. El examen físico del sistema genitourinario debe incluir la longitud del pene mientras está estirado, la ubicación de la placa y el tamaño. El grado de curvatura puede ser evaluado por el paciente tomando fotografías del falo erecto o por inyecciones vasoactivas en combinación con ultrasonido Doppler dúplex del pene.
Comprender la historia natural y la patogénesis de la EP es importante para seleccionar los regímenes de tratamiento adecuados. Si bien la fisiopatología no se entiende completamente, se plantea la hipótesis de que el evento incitante es un desgarro traumático subclínico en la túnica albugínea. El desgarro conduce a una reacción fibrótica proliferativa, lo que resulta en una cicatriz inelástica. El tratamiento para la EP se divide en aquellos dentro de la fase aguda y aquellos en la fase de estabilización crónica. El tiempo de fase aguda se define vagamente como menos de 12 meses desde el inicio de los síntomas. Durante este tiempo, la cicatriz del paciente continúa modificándose y cambiando. La fase crónica se determina una vez que la curvatura del paciente se ha mantenido estable durante al menos 6 meses. Si bien el tratamiento quirúrgico sigue siendo el estándar de oro para la EP, se ofrece principalmente a hombres en la fase crónica de la enfermedad. Para aquellos pacientes en fase aguda, la farmacoterapia ofrece el potencial de mejorar la función, reducir la deformidad y estabilizar la progresión de la cicatriz (5). En el presente documento, revisamos el conocimiento actual disponible con respecto a las opciones de tratamiento oral para la EP. Es importante tener en cuenta que, si bien algunas de las recomendaciones enumeradas se basan en conclusiones basadas en pruebas, otras reflejan la opinión de expertos (Tabla 1).

Tabla completa
Para-aminobenxoato de potasio (POTABA)
La POTABA es un compuesto conocido por sus propiedades antifibróticas y antiinflamatorias que ayudan en el tratamiento de trastornos fibróticos como la dermatomiositis y esclerodermia. Se cree que su eficacia se debe a una reducción en la formación de colágeno a través de la disminución de los niveles de serotonina, el aumento de la actividad de la monoaminooxidasa y la inhibición de la secreción de glucosaminoglicanos de fibroblastos (6). El primer uso propuesto de POTABA para tratar la EP fue en 1959 por Zarafonetis y Horrax (7). En 2005, Weidner et al. se realizó un ensayo multicéntrico, aleatorizado, doble ciego controlado con placebo de POTABA (51 pacientes) versus placebo (52 pacientes) en pacientes con EP sin tratamiento previo con placa no calcificada. El grupo de ensayo recibió 3 g de POTABA por vía oral, 4 veces al día durante 12 meses. Después de 12 meses, los pacientes tratados con POTABA tuvieron una mejora significativa en el tamaño de la placa del pene en comparación con los tratados con placebo. Además, se observó un empeoramiento de la curvatura en los pacientes que recibieron placebo. Los autores concluyeron que la POTABA puede ayudar a estabilizar el tejido cicatricial, lo que evitaría la progresión de la curvatura (6). No se han realizado más ensayos de control aleatorizados para evaluar la eficacia de POTABA. Esto se debe quizás a su perfil de efectos secundarios, que incluye malestar gastrointestinal, diarrea, hepatitis aguda e hipoglucemia (8).
Vitamina E
La vitamina E, un antioxidante soluble en grasa, inactiva los radicales libres que saturan el óxido nítrico (NO), manteniendo así los niveles de NO activos elevados para permitir la cicatrización adecuada de las heridas. Al limitar el estrés oxidativo, también ofrece potencialmente un efecto antiinflamatorio. Se describió por primera vez para el tratamiento de la EP en 1948 (9) y, debido a su bajo costo y disponibilidad, sigue siendo el agente oral más prescrito para la EP (10). A pesar de su uso en las últimas siete décadas, múltiples diseños controlados con placebo no han mostrado una mejora significativa en el dolor, el grado de curvatura, el tamaño de la placa o la capacidad de tener relaciones sexuales. En 1983, Pryor y Farrell completaron un ensayo doble ciego controlado con placebo de vitamina E en 40 pacientes con DP, y no encontraron una mejora significativa en el tamaño de la placa o la curvatura del pene (11). Además, un estudio más reciente realizado en 2007 por Safarinejad et al. proporcionó el ensayo más grande hasta la fecha para evaluar la vitamina E para la EP. Los autores compararon la vitamina E sola y en combinación con L-carnitina con un placebo en 236 hombres con EP crónica temprana; clasificado como paciente con dolor durante las erecciones, curvatura del pene que no interfiere con la penetración vaginal, cicatriz palpable no dolorosa, lesión hiperecoica en la ecografía del pene, ausencia de calcificación y área total de placa <2 cm2. El grupo 1 (58 hombres) recibió 300 mg de vitamina E por vía oral dos veces al día. El grupo 2 (59 hombres) recibió propionil-L-carnitina, 1 g por vía oral dos veces al día. El grupo 3 (60 hombres) recibió 300 mg de vitamina E por vía oral dos veces al día, así como 1 g de propionil-L-carnitina por vía oral dos veces al día. Por último, el grupo 4 recibió un régimen similar de placebo durante el período de prueba de 6 meses. Después del tratamiento, no hubo cambios significativos en la reducción de la curvatura del pene entre los cuatro grupos (P=0,9), ni disminución del tamaño de la placa (P=0,1) (12).
A pesar de la falta de evidencia que demuestre la eficacia de la vitamina E, todavía se prescribe con frecuencia y, a menudo, se administra simultáneamente con otras modalidades de tratamiento con la esperanza de un papel sinérgico. Los efectos adversos comunes del uso de vitamina E incluyen náuseas, vómitos, diarrea y un mayor riesgo de cáncer de próstata y eventos cerebrovasculares (13).
Colchicina
Aunque la colchicina es principalmente conocida por su tratamiento de la gota, también exhibe propiedades que ayudan en el tratamiento de la EP. La colchicina despolimeriza la tubulina, inhibiendo así la mitosis celular, la adhesión de leucocitos y el transporte de colágeno. Aplicando esta propiedad, la colchicina debería disminuir teóricamente la contracción de la herida al inhibir la deposición de colágeno (14). La mayoría de los estudios que evaluaron la colchicina describieron alguna mejoría en la curvatura, pero estos estudios no fueron aleatorizados ni proporcionaron mediciones objetivas para definir la mejoría. Safarinejad et al. resultó ser uno de los pocos ensayos que evaluaron los efectos terapéuticos de la colchicina al completar un ensayo de un solo centro, aleatorizado, doble ciego, controlado con placebo de 84 pacientes con EP sin placas calcificadas (15). Los pacientes del grupo de colchicina fueron tratados con 0,5-2,5 mg de colchicina al día durante 4 meses. Al final del ensayo, el grupo de colchicina no demostró una mejoría objetiva en la curvatura del pene o el tamaño de la placa. Otros estudios han evaluado los efectos sinérgicos de la colchicina con la vitamina E. Prieto Castro et al. se informó de una mejora significativa en el tamaño de la placa y la curvatura del pene en pacientes que usaban diariamente vitamina E y colchicina en comparación con ibuprofeno solo (16). Cabe destacar que solo hubo 45 pacientes en este ensayo y no hubo grupo de placebo. Sin embargo, un estudio retrospectivo posterior de 100 hombres no expuso diferencias estadísticamente significativas en la eficacia para el alivio del dolor, la curvatura del pene o el tamaño de la placa entre la colchicina y la colchicina combinada con vitamina E (17).
Tamoxifeno
El tamoxifeno es un antagonista de los receptores de estrógeno no esteroideo. En el tratamiento de la EP, se ha demostrado que disminuye la fibrogénesis en la túnica albugínea a través de la modulación de la liberación de TGF-β liberado de los fibroblastos (18). Ralph et al. propuso por primera vez su tratamiento en 1992 como resultado de un estudio no controlado que demostró una mejora en la deformidad del pene en 11 de 31 hombres. Sin embargo, estos hallazgos no fueron reproducibles cuando se evaluó el tamoxifeno en un ensayo prospectivo controlado con placebo en 25 pacientes con EP sin placas calcificadas. A pesar del uso de 20 mg de tamoxifeno dos veces al día, no hubo una mejora significativa en el dolor, la curvatura o el tamaño de la placa en comparación con el placebo (19).
Carnitina
La carnitina es un inhibidor de la acetil coenzima-A que permite la disminución de la formación de radicales libres durante tiempos de estrés celular. En 2001, Biagiotti et al. se realizó un ensayo aleatorizado de 96 pacientes con EP a L-carnitina versus tamoxifeno. Los resultados mostraron una mejora significativa de la curvatura del pene en el grupo de L carnitina (20). Como se mencionó anteriormente, el ensayo Safarinejad 2007 de 4 grupos (vitamina E, carnitina, vitamina E y carnitina, y placebo) no demostró una mejora significativa en la curvatura del pene, el tamaño de la placa o el dolor (12).
Ácido graso omega 3
Al igual que otros agentes orales, los ácidos grasos omega-3 se han evaluado en el tratamiento de la EP debido a sus conocidas propiedades antiinflamatorias. En 2009, Safarinejad et al. publicaron sus resultados en un ensayo prospectivo, aleatorizado, doble ciego, de ácidos grasos omega-3 versus placebo. Un total de 224 pacientes con EP en estadio crónico temprano fueron aleatorizados a 1.84 g de suplementos diarios de omega-3 versus placebo durante 6 meses. Los pacientes fueron evaluados con IIEF – 5 y PDDU antes y después de los 6 meses de medicación. Desafortunadamente, no hubo una mejora significativa con respecto al volumen de la placa, la curvatura del pene, el dolor durante la erección y la función eréctil (21). Actualmente, hay una falta de datos que respalden un efecto beneficioso de la suplementación con omega-3 en la etapa crónica temprana de la EP.
Procarbazina
La procarbazina es un medicamento quimioterapéutico alquilante que a menudo se usa para tratar el linfoma del SNC, el linfoma de Hodgkin y los gliomas de grado alto. En 1968, Aron et al. se observó una regresión de la enfermedad de Dupuytren en pacientes sometidos a tratamiento de la enfermedad de Hodgkin con procarbazina, lo que sugiere su uso en una enfermedad con proliferación de tejido conectivo (22). Con esta premisa, en la década de 1970, Byström propuso la procarbazina para el tratamiento de la EP, pero los estudios posteriores no revelaron ningún beneficio objetivo. Además, los estudios revelaron efectos secundarios significativos del medicamento citotóxico, y se recomendó no usarlo en la enfermedad benigna de la EP. Los efectos secundarios incluyen mielosupresión, hepatotoxicidad, fatiga, malestar gastrointestinal y alteraciones del SNC (23,24).
Inhibidores de la fosfodiesterasa tipo 5 (inhibidores de la PDE-5)
Aunque se suele pensar que los inhibidores de la PDE-5 son un tratamiento para la disfunción eréctil, estudios recientes han demostrado su uso potencial en el tratamiento de la DP en pacientes con o sin disfunción eréctil. Los inhibidores de la PDE – 5 aumentan el monofosfato cíclico de guanosina (GMPc) al inhibir la degradación de GMPc a GMP. Con el aumento de GMPc y NO, la síntesis y deposición de colágeno se inhiben y se produce la apoptosis de fibroblastos y miofibroblastos (25). Debido a esta propiedad, los inhibidores de la PDE-5 pueden resultar ventajosos para la remodelación de cicatrices. En un modelo de EP en ratas, se demostró que sildenafilo causaba una reducción significativa de la relación colágeno-fibroblastos en la túnica albugínea, así como del tamaño de la placa (25). Chung y sus colegas estudian el uso de tadalafilo para el tratamiento de la EP en seres humanos. Informaron que 2.la administración de 5 mg de tadalafilo al día durante 6 meses dio lugar a la resolución de la cicatriz septal en el 69% (24/35) de los pacientes sin placa palpable del pene. Solo el 10% del grupo que no recibió tratamiento observó la resolución de la cicatriz. Es importante mencionar que la cicatriz septal no era clínicamente palpable y la mayoría de los pacientes en este estudio no tenían curvatura (26). Más recientemente, un estudio de 2014 informó de los resultados del tratamiento de pacientes con EP que usaron 50 mg de sildenafilo al día o 400 UI de vitamina E durante 3 meses. Después de 12 semanas, ambos grupos mostraron una reducción similar en el volumen de placa y la curvatura del pene que fue estadísticamente significativa. Sin embargo, las diferencias entre los dos grupos no fueron estadísticamente significativas. La cohorte de sildenafilo mostró una mejoría estadísticamente significativa en las puntuaciones de IIEF y reducción del dolor en comparación con la vitamina E sola (27). Sería necesario realizar un ensayo de placebo doble ciego a gran escala y validar el beneficio clínico del inhibidor de la PDE-5, pero la investigación actual es prometedora (Tabla 2).
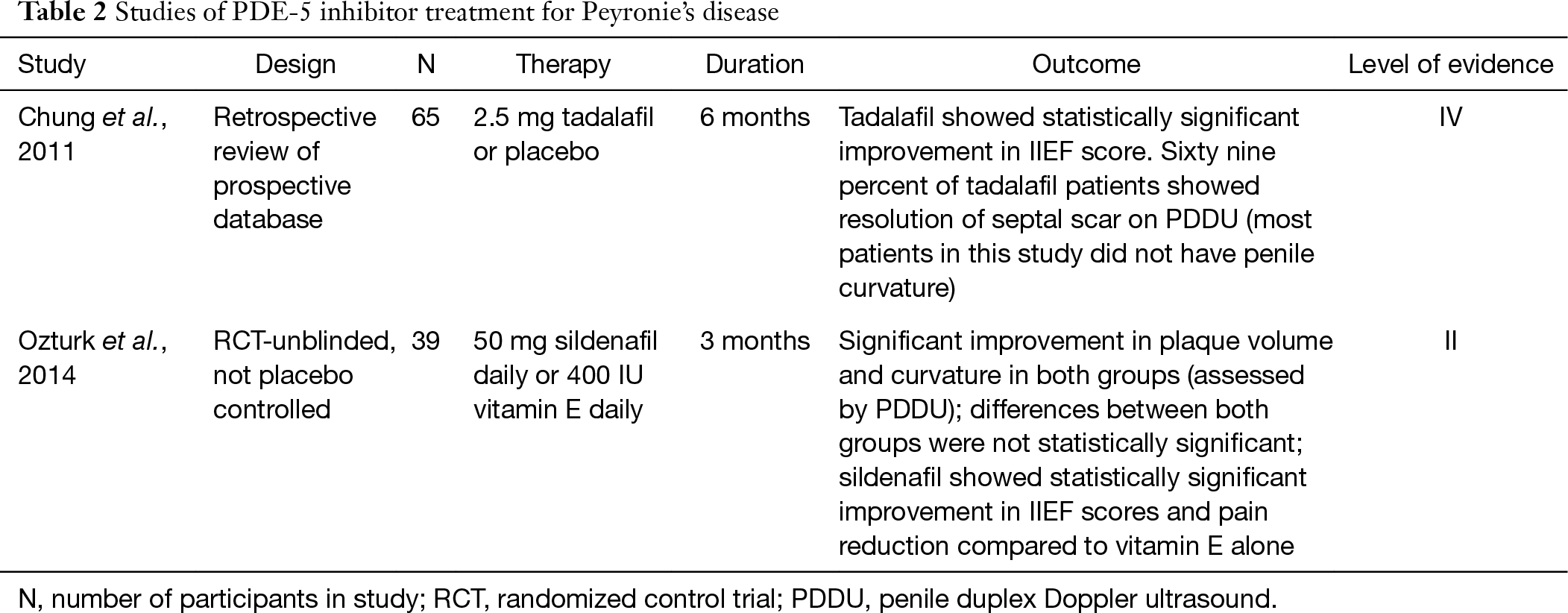
Tabla completa
L-arginina
La L-arginina es un precursor SIN efecto estimulante de la NO sintasa. Esto causa un aumento del NO, así como una reducción de los fibroblastos debido a la apoptosis. Se cree que estas dos propiedades son los mecanismos detrás de la L-arginina como agente antifibrótico (25). Como se mencionó anteriormente, Valente et al. se evaluaron placas peneales en modelos de ratas tratadas con inhibidores de la PDE-5, pero también con l-arginina. De manera similar a los inhibidores de la PDE-5, la L-arginina mostró una reducción significativa en el tamaño de la placa, así como en la proporción de colágeno a fibroblastos (25). Un estudio posterior de Medeiros et al. se demostró que la arginina también tiene un efecto protector contra la formación de tejido cicatricial cuando se somete el pene de ratas a radiación pélvica (28). En 2012, Abern et al. se observó una tendencia hacia la mejora de la curvatura en pacientes con EP tratados con terapia de tracción del pene en combinación con verapamilo intralesional, L-arginina oral y pentoxifilina oral (PTX) (29). Si bien este estudio tiene numerosas variables que podrían contribuir a la mejora de la curvatura, resulta ser uno de los pocos ensayos en humanos en los que se usó L-arginina para tratar la EP. Dados estos hallazgos, la L-arginina puede ser una opción de tratamiento valiosa para la EP, pero se necesitan más ensayos en humanos.
Pentoxifilina (PTX)
Aunque la mayoría de los medicamentos orales investigados para el tratamiento de la EP han mostrado resultados pobres o indeterminados en estudios controlados, a la PTX le ha ido mucho mejor. PTX es un derivado de la xantina que funciona como un inhibidor inespecífico de la fosfodiesterasa con propiedades antiinflamatorias y antifibrógenas conocidas (30). Se ha propuesto para el tratamiento de la EP debido a un estudio in vitro que muestra que previene la proliferación de fibroblastos de túnica albugínea, atenúa la deposición de colágeno mediada por TGF-B, reduce la deposición de elastina y aumenta la actividad fibrinolítica (31-33). Dadas estas propiedades, un estudio doble ciego controlado con placebo de 2010 buscó determinar el efecto de la PTX en pacientes con EP crónica temprana (30). Doscientos veintiocho pacientes fueron aleatorizados para recibir 400 mg de liberación sostenida de PTX versus placebo durante 6 meses. La mayoría de los participantes habían fracasado al menos un tratamiento previo para la EP. El grupo de placebo tuvo 4 veces más probabilidades (42%) de tener progresión de la enfermedad en comparación con el grupo de tratamiento (11%). Además, el grupo PTX mostró una mejoría significativa en las medidas tanto objetivas como subjetivas; (I) mejoría en la curvatura del pene medida por ultrasonido dúplex antes y después de la inyección corporal con prostaglandina E1; (II) volumen de placa y (III) puntuaciones IIEF (30). Estudios más recientes han evaluado PTX oral junto con antioxidantes orales, PTX intralesional y verapamilo intralesional con resultados variables (34,35). Si bien la PTX sigue siendo un fuerte competidor para el tratamiento de la EP, se necesitarán más ensayos multicéntricos grandes para garantizar que los resultados sean reproducibles (Tabla 3).

Tabla completa
Conclusiones
A pesar de décadas de investigación en DP, la etiología y fisiopatología definitivas no se han aclarado completamente. Si bien la terapia quirúrgica sigue siendo el estándar de oro para la EP crónica grave, hay una miríada de otras opciones de tratamiento menos invasivas, a saber, medicamentos orales e intralesionales. En el presente documento, hemos revisado los agentes orales recetados o discutidos con mayor frecuencia para el tratamiento de la EP. Aunque varios estudios bien diseñados han descubierto respuestas positivas con medicamentos orales, su pequeño tamaño de muestra limita la potencia y la reproducibilidad del estudio. En la actualidad, las directrices de la Asociación Americana de Urología establecen que los médicos no deben ofrecer terapia oral con vitamina E, tamoxifeno, ácido graso omega-3 o combinación de vitamina E con L-carnitina. Del mismo modo, la Consulta Internacional sobre Medicina Sexual de 2010 no apoyó el uso clínico rutinario de agentes orales para la EP (5). Dos medicamentos orales no restringidos por las pautas son los inhibidores de la PDE – 5 y el PTX. Se necesitan más investigaciones sobre PDE-5 y PTX, para incluir grandes ensayos multicéntricos, doble ciego, aleatorizados y de control, para determinar su eficacia. Ambas clases de medicamentos dan esperanza a la ausencia de medicamentos orales permitidos para el tratamiento de la EP.
Agradecimientos
Ninguno.
Nota al pie de página
Conflictos de intereses: Los autores no tienen conflictos de intereses que declarar.
- Mulhall JP, Creech SD, Boorjian SA, et al. Análisis subjetivo y objetivo de la prevalencia de la enfermedad de Peyronie en una población de hombres que se presentaron para exámenes de detección del cáncer de próstata. J Urol 2004; 171: 2350-3.
- Mulhall JP, Schiff J, Guhring P. An analysis of the natural history of Peyronie’s disease. J Urol 2006;175: 2115-8; discusión 2118.
- Tal R, Heck M, Teloken P, et al. Enfermedad de Peyronie después de una prostatectomía radical: incidencia y predictores. J Sex Med 2010; 7: 1254-61.
- Lin H, Alba F, Romero C, et al. 1815 la curvatura del pene es un hallazgo común en la implantación de prótesis de pene para pacientes con disfunción eréctil después de una prostatectomía radical. J Urol 2011; 185: e728-e729.
- Ralph D, Gonzalez-Cadavid N, Mirone V, et al. The management of Peyronie’s disease: evidence-based 2010 guidelines (en inglés). J Sex Med 2010; 7: 2359-74.
- Weidner W, Hauck EW, Schnitker J, et al. Paraaminobenzoato de potasio (POTABA) en el tratamiento de la enfermedad de Peyronie: un estudio prospectivo, controlado con placebo y aleatorizado. Eur Urol 2005; 47: 530-5; debate 535-6.
- Zarafonetis CJ, Horrax TM. Tratamiento de la enfermedad de Peyronie con para-aminobenzoato de potasio (potaba). J Urol 1959; 81: 770-2.
- Roy J, Carrier S. Hepatitis aguda asociada con el tratamiento de la enfermedad de Peyronie con para-aminobenzoato de potasio (Potaba). J Sex Med 2008; 5: 2967-9.
- Scott WW, Scardino PL. Un nuevo concepto en el tratamiento de la enfermedad de Peyronie. South Med J 1948; 41: 173-7.
- Levine LA, Burnett AL. Procedimientos operativos estándar para la enfermedad de Peyronie. J Sex Med 2013; 10: 230-44.
- Pryor JP, Farrell CF. Ensayo clínico controlado de vitamina E en la enfermedad de Peyronie. Prog Reprod Biol 1983; 9: 41-5.
- Safarinejad MR, Hosseini SY, Kolahi AA. Comparación de vitamina E y propionil-L-carnitina, por separado o en combinación, en pacientes con enfermedad crónica temprana de Peyronie: un estudio aleatorizado, controlado con placebo y doble ciego. J Urol 2007; 178: 1398-403; discusión 1403.
- Klein EA, Thompson IM Jr, Tangen CM, et al. Vitamina E y el riesgo de cáncer de próstata: el Ensayo de Prevención del Cáncer con Selenio y Vitamina E (SELECT). JAMA 2011; 306: 1549-56.
- El-Sakka AI, Bakircioglu ME, Bhatnagar RS, et al. Los efectos de la colchicina en una condición similar a la de Peyronie en un modelo animal. J Urol 1999; 161: 1980-3.
- Safarinejad MR. Efectos terapéuticos de la colchicina en el tratamiento de la enfermedad de Peyronie: un estudio aleatorizado, doble ciego, controlado con placebo. Int J Impot Res 2004; 16: 238-43.
- Prieto Castro RM, Leva Vallejo ME, Regueiro Lopez JC, et al. Tratamiento combinado con vitamina E y colchicina en las primeras etapas de la enfermedad de Peyronie. BJU Int 2003; 91: 522-4.
- Cortés-González JR, Glina S. Tratamiento conservador de la enfermedad de Peyronie: colchicina vs. colchicina más vitamina E. Actas Urol Esp 2010; 34: 444-9.
- Ralph DJ, Brooks MD, Bottazzo GF, et al. El tratamiento de la enfermedad de Peyronie con tamoxifeno. Br J Urol 1992; 70: 648-51.
- Teloken C, Rhoden EL, Grazziotin TM, et al. Tamoxifeno versus placebo en el tratamiento de la enfermedad de Peyronie. J Urol 1999; 162: 2003-5.
- Biagiotti G, Cavallini G. Acetil-L-carnitina vs tamoxifeno en la terapia oral de la enfermedad de Peyronie: un informe preliminar. BJU Int 2001; 88: 63-7.
- Safarinejad MR. Eficacia y seguridad de los omega – 3 para el tratamiento de la enfermedad de Peyronie en estadio temprano: Un estudio prospectivo, aleatorizado, doble ciego controlado con placebo. J Sex Med 2009; 6: 1743-54.
- Aron E. Tratamiento médico de la enfermedad de Dupuytren con un agente citostático (metilhidracina). Presse Med 1968; 76: 1956.
- Byström J, Johansson B, Edsmyr F, et al. Induratio penis plastica (enfermedad de Peyronie). Los resultados de las diversas formas de tratamiento. Scand J Urol Nephrol 1972; 6:1-5.
- Oosterlinck W, Hace G. Tratamiento de la enfermedad de Peyronie con procarbazina. Br J Urol 1975; 47: 219-20.
- Valente EG, Vernet D, Ferrini MG, et al. Los inhibidores de L-arginina y fosfodiesterasa (PDE) contrarrestan la fibrosis en la placa fibrótica de Peyronie y cultivos de fibroblastos relacionados. Nitric Oxide 2003; 9: 229-44.
- Chung E, Deyoung L, Brock GB. The role of PDE5 inhibitors in penile septal scar remodeling: assessment of clinical and radiological outcomes. J Sex Med 2011; 8:1472-7.
- Ozturk U, Yesil S, Goktug HN, et al. Efectos del tratamiento con sildenafilo en pacientes con enfermedad de Peyronie y disfunción eréctil. Ir J Med Sci 2014;183: 449-53.
- Medeiros JL Jr, Costa WS, Felix-Patricio B, et al. Efectos protectores de la suplementación nutricional con arginina y glutamina en el pene de ratas sometidas a radiación pélvica. Andrology 2014; 2: 943-50.
- Abern MR, Larsen S, Levine LA. Combinación de tracción del pene, verapamilo intralesional y terapias orales para la enfermedad de Peyronie. J Sex Med 2012; 9:288-95.
- Safarinejad MR, Asgari MA, Hosseini SY, et al. Un estudio doble ciego controlado con placebo de la eficacia y seguridad de la pentoxifilina en la enfermedad crónica temprana de Peyronie. BJU Int 2010; 106: 240-8.
- Raetsch C, Jia JD, Boigk G, et al. La pentoxifilina regula a la baja la expresión de citocinas profibrogénicas y procolágeno I en la fibrosis biliar secundaria de ratas. Gut 2002; 50: 241-7.
- Schandené L, Vandenbussche P, Crusiaux A, et al. Efectos diferenciales de la pentoxifilina en la producción de factor de necrosis tumoral alfa (TNF-alfa) e interleucina 6 (IL-6) por monocitos y células T. Immunology 1992; 76: 30-4.
- Shindel AW, Lin G, Ning H, et al. La pentoxifilina atenúa la deposición de colágeno estimulada por el factor de crecimiento transformador β1 y la elastogénesis en fibroblastos derivados de túnica albugínea humana parte 1: impacto en la matriz extracelular. J Sex Med 2010; 7: 2077-85.
- Paulis G, Barletta D, Turchi P, et al. Evaluación de la eficacia y seguridad de la pentoxifilina asociada con otros antioxidantes en el tratamiento médico de la enfermedad de Peyronie: un estudio de casos y controles. Res Rep Urol 2015; 8: 1-10.
- Alizadeh M, Karimi F, Fallah MR. Evaluación de la eficacia del verapamilo en la enfermedad de Peyronie en comparación con la pentoxifilina. Glob J Health Sci 2014; 6: 23-30.
- Smith JF, Shindel AW, Huang YC, et al. Tratamiento con pentoxifilina y calcificaciones del pene en hombres con enfermedad de Peyronie. Asian J Androl 2011; 13: 322-5.