bevisen bakom naturliga interventioner för nonalcoholic fet leversjukdom: växter, näringsämnen och probiotika för behandling av denna vanliga sjukdom
med tanke på ökningen av nonalcoholic fettleversjukdom (NAFLD) hos både vuxna och barn och bristen på en indikerad farmaceutisk behandling,, naturliga strategier för behandling av detta tillstånd står väl redo som ”nästa bästa sak.”Flera näringstillskott och växter har studerats kliniskt och visar löfte för behandling av NAFLD och dess inflammatoriska motsvarighet, alkoholfri steatohepatit (NASH). Med tanke på hur många av dessa terapier adresserar de faktorer som bidrar till utvecklingen av NAFLD, tar det inte mycket resonemang för att förstå hur de effektivt kan ta itu med några av de grundläggande orsakerna till sjukdom, snarare än att bara ta itu med ett symptom.
fem kompletterande ingrepp med kliniska eller epidemiologiska bevis för deras användning vid NAFLD är fosfatidylkolin, som ger fosfolipider och kolin, vitamin E, både som alfa-tokoferoler och en blandning av delta-och gammatokotrienoler, mjölktistelfröextrakt, berberin och probiotika.
- Fettleverförändringar: korrelerad med en Fosfatidylkolinbrist?
- Vitamin E
- mjölktistel
- berberin
- probiotika
- slutsats
- Dr. Carrie Decker, nd tog examen med hedersbetygelser från National College of Natural Medicine (nu National University of Natural Medicine) i Portland, Oregon. Dr. Decker ser patienter på distans, med fokus på gastrointestinala sjukdomar, humörobalanser, ätstörningar, autoimmun sjukdom och kronisk trötthet. Innan han blev naturläkare var Dr. Decker ingenjör och fick examen i biomedicinsk och maskinteknik från University of Wisconsin-Madison respektive University of Illinois i Urbana-Champaign. Dr. Decker fortsätter att njuta av akademisk forskning och skrivning och använder dessa färdigheter för att stödja integrativ medicinutbildning som författare och bidragsgivare till olika resurser. Dr. Decker stöder Allergy Research Group som medlem i deras utbildnings-och produktutvecklingsteam.
- källor:
- Spengler EK, Loomba R. rekommendationer för diagnos, remiss för leverbiopsi och behandling av icke-alkoholisk fet leversjukdom och icke-alkoholisk steatohepatit. Mayo Clinic Förfaranden. 2015;90(9):1233–1246.
- Berardis S, Sokal E. pediatrisk alkoholfri fettlever: en ökande folkhälsoproblem. Eur J Pediatr. 2014 februari; 173 (2):131-9.
- Jadeja R, et al. Växtbaserade läkemedel för behandling av nonalcoholic steatohepatit: nuvarande scenario och framtidsutsikter. Evid Baserat Komplement Alternat Med. 2014:648308.
- Pomorski T, et al. Lipidfördelning och transport över cellmembran. Semin Cell Dev Biol. 2001 April;12 (2): 139-48.
- Yamaji-Hasegawa A, et al. Asymmetrisk fördelning av fosfolipider i biomembran. Biol Pharm Bull. 2006 augusti;29 (8): 1547-53.
- Hej på dig. Biliär lipidsekretion. Turk J Gastroenterol. 2007 juni; 18 (2): 65-70.
- Fischer LM, et al. Kön och menopausal status påverkar mänskliga kostbehov för näringsämnet Kolin. Am J Clin Nutr. 2007 maj; 85 (5):1275-85.
- Wallace TC, et al. Vanliga kolinintag är förknippade med ägg-och Proteinmatkonsumtion i USA. Näringsämne. 2017 Augusti 5; 9 (8).
- Zeisel SH. Genresponselement, genetiska polymorfismer och epigenetik påverkar det mänskliga kostbehovet för kolin. IUBMB liv. 2007 juni; 59 (6):380-7.
- Zeisel SH. Genresponselement, genetiska polymorfismer och epigenetik påverkar det mänskliga kostbehovet för kolin. IUBMB liv. 2007 juni; 59 (6):380-7.
- Guerrerio AL, et al. Kolinintag i en stor kohort av patienter med alkoholfri fettlever. Am J Clin Nutr. 2012 april; 95 (4):892-900.
- Ma X, et al. Polyenylfosfatidylkolin dämpar alkoholfri leverfibros och accelererar dess regression. J Hepatol. 1996 maj; 24 (5): 604-13.
- Lieber CS, et al. Fosfatidylkolin skyddar mot fibros och cirros i babian. Gastroenterologi. 1994 januari; 106 (1): 152-9.
- Chanussot F, et al. Förebyggande genom diet (n-6) fleromättade fosfatidylkoliner av intrahepatisk kolestas inducerad av cyklosporin A hos djur. Life Sci. 2003 juni 13; 73 (4):381-92.
- Karaman A, et al. Skyddande effekt av fleromättad fosfatidylkolin på leverskador inducerad av gallvägsobstruktion hos råttor. J Pediatric Surg. 2003 September; 38 (9): 1341-7.
- Karaman A, et al. Skyddande effekt av fleromättad fosfatidylkolin på leverskador inducerad av gallvägsobstruktion hos råttor. J Pediatric Surg. 2003 September; 38 (9): 1341-7.
- Stremmel W, et al. Slemhinneskydd med fosfatidylkolin. Gräv Dis. 2012; 30 Suppl 3: 85-91.
- Parlesak A, et al. Konjugerade primära gallsalter minskar permeabiliteten hos endotoxin genom tarmepitelceller och synergiserar med fosfatidylkolin vid undertryckande av inflammatorisk cytokinproduktion. Crit Vård Med. 2007 oktober; 35 (10): 2367-74.
- Mitzscherling K, et al. Fosfatidylkolin reverserar etanolinducerad ökning av transepitelial endotoxinpermeabilitet och avskaffar transepitelial leukocytaktivering. Alkohol Clin Exp Res. 2009 Mar;33 (3): 557-62.
- Buzzetti E, et al. Den multipla hit-patogenesen av alkoholfri fettleversjukdom (NAFLD). Ämnesomsättning. 2016 Aug;65 (8):1038-48.
- El Hadi H, et al. E-Vitamin som behandling för alkoholfri fettlever: verklighet eller myt? Antioxidanter (Basel). 2018 januari 16; 7 (1).
- Bugianesi E, et al. En randomiserad kontrollerad studie av metformin kontra vitamin E eller receptbelagd diet vid icke-alkoholisk fet leversjukdom. Am J Gastroenterol. 2005 maj; 100 (5):1082-90.
- Sanyal AJ, et al. Pioglitazon, vitamin E eller placebo för icke-alkoholhaltig steatohepatit. N Engl J Med. 2010 maj 6; 362 (18): 1675-85.
- Lavine JE. Vitamin E behandling av alkoholfri steatohepatit hos barn: pilotstudie. J Pediatr. 2000 juni; 136 (6):734-8.
- Peh HY, et al. Vitamin E-terapi utöver cancer: tokoferol kontra tocotrienol. Pharmacol Ther. 2016 Juni; 162: 152-69.
- Qureshi AA, et al. Dosberoende modulering av lipidparametrar, cytokiner och RNA av delta-tocotrienol hos hyperkolesterolemiska personer begränsade till Aha-Steg-1-diet. Brit J av Med & Med Res. 2015; 6 (4):351-66.
- Qureshi AA, et al. Inverkan av delta-tocotrienol på inflammatoriska biomarkörer och oxidativ stress hos hyperkolesterolema ämnen. Clin Exp Kardiologi. 2015;6(4):1000367.
- Zaiden N, et al. Gamma delta-tokotrienoler minskar leverns triglyceridsyntes och VLDL-utsöndring. J Atheroscler Thromb. 2010 oktober 27; 17 (10): 1019-32.
- Magosso E, et al. Tokotrienoler för normalisering av leverekogent svar i icke-alkoholisk fettlever: en randomiserad placebokontrollerad klinisk studie. Nutr J. 2013 December 27; 12 (1): 166.
- Pervez MA, et al. Effekter av Delta-tocotrienol-tillskott på leverenzymer, Inflammation, oxidativ stress och leverstatos hos patienter med alkoholfri fettlever. Turk J Gastroenterol. 2018 Mars;29 (2):170-176.
- Abenavoli L, et al. Mjölktistel i leversjukdomar: förflutna, nutid, framtid. Phytother Res. 2010 Oktober; 24 (10): 1423-32.
- Valenzuela A, et al. Selektivitet av silymarin på ökningen av GSH-innehållet i olika vävnader hos råttan. Planta Med. 1989 oktober; 55 (5):420-2.
- Rui YC. Framsteg i farmakologiska studier av silymarin. Mem Inst Oswaldo Cruz. 1991; 86 Suppl 2: 79-85.
- Gu M, et al. Silymarin förbättrar metabolisk dysfunktion associerad med Dietinducerad fetma via aktivering av Farnesyl X-receptorn. Främre Pharmacol. 2016 September 28; 7: 345.
- Ali AH, et al. Nya framsteg i utvecklingen av farnesoid X-receptoragonister. Ann Transl Med. 2015 Januari; 3 (1):5.
- Traussnigg S, et al. Effekt och säkerhet för den icke-steroida farnesoid X-receptoragonisten PX-104 hos patienter med alkoholfri fettlever (NAFLD). Zeitschrift f brasilir gastroenterologi. 2017 Mer; 55 (05):A71.
- Zhong S, et al. Den terapeutiska effekten av silymarin vid behandling av icke-alkoholisk fettsjukdom: en metaanalys (PRISMA) av randomiserade kontrollstudier. Medicin (Baltimore). 2017 December;96 (49): e9061.
- Hajiaghamohammadi AA, et al. Effekter av metformin, pioglitazon och silymarinbehandling på alkoholfri fettlever: en randomiserad kontrollerad pilotstudie. Hepat Mon. 2012 Augusti; 12 (8):e6099.
- Birdsall TC, et al. Berberin: terapeutisk potential hos en alkaloid som finns i flera medicinska växter. Altern Med Rev. 1997; 2: 94-103.
- Imanshahidi M, et al. Farmakologiska och terapeutiska effekter av Berberis vulgaris och dess aktiva beståndsdel, berberin. Phytother Res. 2008 Aug; 22 (8):999-1012.
- Zhu X, et al. De potentiella mekanismerna för berberin vid behandling av icke-alkoholhaltig fettlever. Molekyl. 2016 Oktober 14; 21 (10).
- Lan J, et al. Metaanalys av effekten och säkerheten av berberin vid behandling av typ 2-diabetes mellitus, hyperlipemi och hypertoni. J Ethnopharmacol. 2015 Februari 23; 161: 69-81.
- Sun R, et al. Oralt administrerat berberin modulerar Leverlipidmetabolism genom att förändra mikrobiell Gallsyrametabolism och Tarmfxr-signalvägen. Mol Pharmacol. 2017 februari; 91 (2):110-122.
- Guo T, et al. Berberin förbättrar leverstatos och undertrycker lever-och Fettvävnadsinflammation hos möss med Dietinducerad fetma. Sci Rep. 2016 Mar 3; 6: 22612.
- Schattenberg JM, et al. JNK1 men inte JNK2 främjar utvecklingen av steatohepatit hos möss. Hepatologi. 2006 Januari; 43 (1): 163-72.
- Han J, et al. Modulerande tarmmikrobiota som en anti-diabetisk mekanism av berberin. Med Sci Monit. 2011; 17: RA164-7.
- Gu L, et al. Berberine förbättrar tarmepitelial tight-junction skada och nedreglerar myosinljuskedjkinasvägar i en musmodell av endotoxinemi. J Infektera Dis. 2011 juni 1; 203 (11): 1602-12.
- Li N, et al. Berberin dämpar proinflammatorisk cytokininducerad tät korsningsstörning i en in vitro-modell av tarmepitelceller. Eur J Pharm Sci. 2010 April 16; 40 (1): 1-8.
- Ma X, et al. Patogenesen av Diabetes Mellitus genom oxidativ Stress och Inflammation: dess hämning av berberin. Främre Pharmacol. 2018 juli 27; 9: 782.
- Yan HM, et al. Effekt av berberin hos patienter med alkoholfri fettlever. PLoS One. 2015 Augusti 7;10 (8):e0134172.
- Ma YY, et al. Effekter av probiotika på alkoholfri fettlever: en metaanalys. Världen J Gastroenterol. 2013 Oktober 28; 19 (40):6911-8.
- Vajro P, et al. Effekter av Lactobacillus rhamnosus stam GG i pediatrisk fetma-relaterad leversjukdom. J Pediatr Gastroenterol Nutr. 2011 juni; 52 (6):740-3.
- Alisi A, et al. Randomiserad klinisk studie: de positiva effekterna av VSL # 3 hos överviktiga barn med alkoholfri steatohepatit. Aliment Pharmacol Ther. 2014 juni; 39 (11): 1276-85.
- p oc-Rrez-Rubio KG, et al. Effekt av berberinadministration på metaboliskt syndrom, insulinkänslighet och insulinsekretion. Metab Syndr Relat Disord. 2013 oktober;11 (5):366-9.
- Iacono A, et al. Probiotika som en framväxande terapeutisk strategi för att behandla NAFLD: fokusera på molekylära och biokemiska mekanismer. J Nutr Biochem. 2011 augusti; 22 (8):699-711.
- Honda Y, et al. Effekt av glutation för behandling av icke-alkoholisk fettlever: en öppen, enarmad, multicenter, pilotstudie. BMC Gastroenterol. 2017 Augusti 8;17 (1):96.
- Dentico P, et al. . Recenti Prog Med. 1995 Juli-Augusti; 86 (7-8):290-3.
- Khoshbaten M, et al. N-acetyl-cystein förbättrar leverfunktionen hos patienter med alkoholfri fettlever. Hepatit Mon. 2010;10(1):12-16.
- Muto C, et al. Gamma-tocotrienol minskar triacylglycerolnivån i råttans primära hepatocyter genom reglering av fettsyrametabolism. J Clin Biochem Nutr. 2013;52(1):32-37.
- Parker HM, et al. Omega – 3-tillskott och alkoholfri fet leversjukdom: en systematisk granskning och metaanalys. J Hepatol. 2012;56(4):944-51.
Fettleverförändringar: korrelerad med en Fosfatidylkolinbrist?
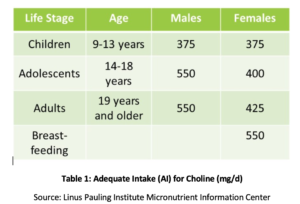
fosfatidylkolin (PC) är avgörande för hälsan hos alla celler i kroppen och är en av de viktigaste fosfolipiderna som cellmembran består av., PC omfattar över 90% av den totala gallfosfolipidhalten och underlättar fettemulgering, absorption och transport. Studier har visat att det rekommenderade adekvata intaget (AI) av kolin (se Tabell 1) kanske inte är tillräckligt för att förebygga symtom på brist, såsom fettleverförändringar eller muskelskador. Dessutom fann en ny studie att endast 8% av amerikanska vuxna uppfyller den rekommenderade AI av kolin, med vegetarianer, postmenopausala kvinnor och män med störst risk för otillräcklighet., Genetiska polymorfismer kan också öka behovet av kolin, vilket också är en källa till metylgrupper i kroppen.
hos postmenopausala kvinnor med NAFLD har minskat kolinintag visat sig vara signifikant associerat med en ökad risk för fibros. Hos djur har PC visat sig skydda mot fibros i samband med leverinflammation., Ökat intag av PC har visat sig förbättra galllipidsekretion och därigenom förhindra kolestas och efterföljande leverskada via många mekanismer, inklusive undertryckande av kärnfaktor kappa B (NF-kB), en väl förstådd molekylär utlösare av inflammation., I en djurmodell av gallvägsobstruktion har kompletterande PC visat sig minska leverskador, duktal proliferation och fibros.
PC är också viktigt för tarmens hälsa och är en primär komponent i det skyddande tarmslemskiktet. I cellkulturer har behandling med PC visat sig minska migrationen av endotoxin genom tarmepitelceller, vilket ytterligare undertrycker det associerade inflammatoriska cytokinsvaret. PC minskar också endotoxintranslokation vid inställning av alkoholinducerade ökningar i tarmpermeabilitet. Denna fördelaktiga effekt har föreslagits som en av de mekanismer genom vilka PC kan betraktas som terapeutisk vid alkoholisk leversjukdom.
Vitamin E
som en oxidativ stress hit och minskat antioxidant försvar har föreslagits som en faktor som leder utvecklingen av NAFLD, bör det inte vara förvånande att antioxidanter har undersökts som en potentiell behandling för tillståndet.
 E-Vitamin har studerats i flera kliniska prövningar för behandling av NAFLD, både som en fristående och tilläggsbehandling. I en genomgång av dessa studier varierade dosen av E-vitamin från 400 till 1200 IE/dag och studietiden var från 24 veckor till mer än två år. Resultaten var generellt positiva, vilket visade att när E-vitamin inkluderades sågs förbättringar i histologi, steatos och/eller transaminasnivåer., I barnläkemedel med NAFLD har E-vitamin också studerats som en terapi. I en öppen pilotstudie med 11 barn med NAFLD befanns tillskott av mellan 400 och 1200 IE vitamin E i fyra till tio månader normalisera transaminas-och alkaliska fosfatasnivåer under behandlingen, men de återvände till onormala när behandlingen avbröts. Hepatisk ekogenitet förändrades inte under behandlingens gång.
E-Vitamin har studerats i flera kliniska prövningar för behandling av NAFLD, både som en fristående och tilläggsbehandling. I en genomgång av dessa studier varierade dosen av E-vitamin från 400 till 1200 IE/dag och studietiden var från 24 veckor till mer än två år. Resultaten var generellt positiva, vilket visade att när E-vitamin inkluderades sågs förbättringar i histologi, steatos och/eller transaminasnivåer., I barnläkemedel med NAFLD har E-vitamin också studerats som en terapi. I en öppen pilotstudie med 11 barn med NAFLD befanns tillskott av mellan 400 och 1200 IE vitamin E i fyra till tio månader normalisera transaminas-och alkaliska fosfatasnivåer under behandlingen, men de återvände till onormala när behandlingen avbröts. Hepatisk ekogenitet förändrades inte under behandlingens gång.
tokotrienoler är den mindre studerade familjen av de naturligt förekommande formerna av E-vitamin, med tokoferolerna, som oftare finns i naturen, dominerar vetenskaplig forskning. Tokotrienoler är dock potenta antioxidanter, citerade i viss forskning som 40 till 60 gånger antioxidantpotentialen hos tokoferoler. Tokotrienoler har visat sig förbättra totalt kolesterol och dess fraktioner, vilket minskar totalt och LDL-kolesterol med 15 till 20%, och triglycerider upp till nästan 30%. Tokotrienoler har också visat sig ha antiinflammatoriska och antioxidantiska effekter in vivo, Sänka högkänsliga C-reaktiva proteinnivåer (hs-CRP) och minska LDL-oxidation.
tokotrienoler har också studerats som en behandling för NAFLD. Hos patienter med ultraljudsdiagnostiserad NAFLD visade sig 200 mg blandade tocotrienoler (från palmolja, med en hög gammafraktion och ytterligare 61 mg alfa-tokoferoler) som togs två gånger dagligen under ett år signifikant normalisera leverekogen respons och remissionshastighet jämfört med placebo. I en andra studie, inklusive patienter med ultraljuddiagnostiserad NAFLD och transaminashöjning, minskade 300 mg tocotrienoler (en 90:10 delta:gamma-blandning) två gånger dagligen i 12 veckor signifikant aspartataminotransferas (AST), alaninaminotransferas (ALT), hs-CRP och malondialdehyd (en markör för oxidativ stress) nivåer samt fettleverindex poäng jämfört med placebo.
mjölktistel
mjölktistel (Silybum marianum) är kanske den mest kända leverskyddande botaniska. Silymarin, en blandning av de aktiva beståndsdelarna i mjölktistel och silibinin, den mest aktiva föreningen som finns i den, har visats i djurstudier för att minska leverskada orsakad av acetaminophen, alkohol, järnöverbelastning och strålning bland andra kända levertoxiska ämnen. Silymarin har visat sig öka nivåerna av glutation, en kraftfull antioxidant, i både lever och tarmar. Det minskar också lipidperoxidation, vilket skadar cellulära membran, förändrar deras funktion och eventuellt orsakar celldöd.
Silibinin och silymarin har visat sig aktivera en nukleär gallsyrareceptor som kallas farnesoid X-receptor (FXR) i levern, nedreglerande inflammatoriska vägar och korrigering av insulinresistens och dyslipidemi inducerad av hög fetthalt (HFD) utfodring. FXR är en nyckelregulator för gallsyra, glukos och lipidbalans i kroppen. Läkemedel som interagerar med FXR på ett liknande sätt som dessa mjölk tistel härledda föreningar undersöks också för behandling av NAFLD och relaterade metaboliska utmaningar.
kliniska studier har också visat att mjölktistel förbättrar olika parametrar associerade med NAFLD. En metaanalys från 2017 visade att behandling med mjölktistel signifikant minskar ALT och AST med -5,08 IE/L respektive -5,44 IE/L hos patienter med NAFLD. Doserna varierade från 140 mg en gång om dagen till 200 mg tre gånger om dagen, under en varaktighet av 8 till 24 veckor. Vid den lägsta dosen på 140 mg dagligen, efter 8 veckor, sågs signifikanta förbättringar i fastande blodglukos (FBG), lipidprofil och seruminsulinnivåer utöver AST-och ALAT-minskningar från 56 till 37.77 IE/L respektive 78, 73 till 53, 05 IE / l.
berberin
berberin, den orangegula alkaloid som finns i botaniska ämnen som Oregon grape root and bark, goldenseal och barberry, är en annan botaniskt härledd substans som har många mekanismer genom vilka den kan hjälpa till att skydda mot NAFLD och stödja dess upplösning.,,
de antidiabetiska och lipidbalanserande effekterna av berberin har visats i flera kliniska prövningar, och  kan vara medel via vilka berberin positivt påverkar leverfunktionen. Berberin har visat sig förändra metabolismrelaterat genuttryck och gallsyrametabolism via vägar som involverar FXR också. I djurstudier har berberin visat sig ha effekten att förhindra HFD-associerad fetma och ackumulering av lever triglycerider i vildtyp (normala) möss, men inte hos de som hade genetisk eliminering av intestinalt FXR-uttryck. Berberin har också visat sig undertrycka fetma-associerad inflammation och leversteatos hos möss genom att minska fosforylering av det inflammatoriska komplexet som kallas JNK1, ett proteinkinas som är inblandat i utvecklingen av steatohepatit. JNK1 aktiveras starkt av miljöstressorer och proinflammatoriska cytokiner.
kan vara medel via vilka berberin positivt påverkar leverfunktionen. Berberin har visat sig förändra metabolismrelaterat genuttryck och gallsyrametabolism via vägar som involverar FXR också. I djurstudier har berberin visat sig ha effekten att förhindra HFD-associerad fetma och ackumulering av lever triglycerider i vildtyp (normala) möss, men inte hos de som hade genetisk eliminering av intestinalt FXR-uttryck. Berberin har också visat sig undertrycka fetma-associerad inflammation och leversteatos hos möss genom att minska fosforylering av det inflammatoriska komplexet som kallas JNK1, ett proteinkinas som är inblandat i utvecklingen av steatohepatit. JNK1 aktiveras starkt av miljöstressorer och proinflammatoriska cytokiner.
berberin verkar också i tarmen. Det påverkar inte bara tarmens mikrobiella balans, utan påverkar också direkt intestinal permeabilitet, vilket förbättrar tät korsningsintegritet hos djur som utsätts för endotoxemi eller cellkulturer behandlade med proinflammatoriska cytokiner., Direkta antiinflammatoriska effekter har också visats.
fördelarna med berberin i NAFLD har också visats kliniskt i en randomiserad, parallellkontrollerad, öppen klinisk studie. Hos patienter med NAFLD visade sig berberin återställa normal leverarkitektur, lipid och blodsockermetabolism, med signifikanta förbättringar sett över befolkningen som bara genomförde livsstilsförändringar.
probiotika
med tanke på förhållandet mellan de många matsmältningssystemstörningarna och leverenzymhöjningen är det inte förvånande att probiotika också har studerats som en behandling för NAFLD. En ny metaanalys sammanfattar väl de kollektiva resultaten.
hundra trettiofyra patienter diagnostiserade med NAFL/NASH genom leverbiopsi inkluderades i denna analys, och varje ingrepp som användes i de fyra randomiserade, kontrollerade studierna som var berättigade till denna metaanalys var unik (Lactobacillus bulgaricus och Streptococcus thermophilus i tre månader; Lactobacillus GG i åtta veckor; Bifidobacterium longum och fructooligosackarider (Fos) i 24 veckor; och en egen kombination av Lactobacillus plantarum, L. delbrueckii, L. acidophilus, L. rhamnosus och Bifidobacterium bifidum i sex månader). Doseringen av probiotika varierade från 500 miljoner till 12 miljarder kolonibildande enheter (CFU) dagligen. De probiotiska behandlingarna visade sig signifikant minska ALT-och AST-nivåerna med -23.71 UI/L respektive -19.77 UI/l. Signifikanta förbättringar i totalt kolesterol, tumörnekrosfaktor (TNF)-nivåer av TNF och insulinresistens noterades också.
två ytterligare kliniska prövningar undersökte probiotika som behandling för pediatrisk NAFLD. I en dubbelblind, placebokontrollerad pilotstudie, tolv barn med en medelålder på 10 år.7 år gammal, med ultraljudsdiagnostiserade fettleverförändringar och ihållande transaminashöjning fick 12 miljarder CFU av L. rhamnosus GG eller placebo dagligen i 8 veckor. Behandling med probiotiska minskade signifikant ALT-nivåer jämfört med placebo, men leverens ekogenitet och AST-nivåer förändrades inte. Dessutom minskade Anti-peptidoglykan-polysackaridantikroppar, en indikator på bakterier eller bakteriemembrantranslokation genom tarmbarriären, signifikant hos barn som fick probiotiska jämfört med placebo. Den andra studien undersökte behandling av barn med biopsibevisad NAFLD med VSL #3, en högpotensblandning av 8 probiotiska stammar (inklusive Streptococcus thermophilus, 3 Bifidobacteria spp. och 4 Lactobacillus spp.), jämfört med placebo. Hos barn som fick probiotiska förbättrades fettlevervärdena signifikant med sannolikheten för att ingen, lätt, måttlig eller svår fettlever i slutet av studien var 21%, 70%, 9% och 0% jämfört med 0%, 7%, 76% och 17% i placebogruppen.
slutsats
det finns ett brett utbud av säkra och effektiva alternativ tillgängliga som stöder återställandet av hälsa hos dem med NAFLD. Även om varje individ kan ha olika underliggande mekanismer som bidrar till leverdysfunktion och inflammatoriska förändringar, kan var och en av dessa stödjande naturliga medel—och många andra (Se tabell 2)—stödja normal leverfunktion hos individer med dessa utmaningar.
Tabell 2: Närings-och botaniska ingrepp för NAFLD. Näringsämnen som dessa bör användas under ledning av en kvalificerad och licensierad sjukvårdspersonal.
| näringsämne | dosering | mekanism |
| fosfatidylkolin (PC), en källa till kolin i kosten | 1, 5 g två gånger dagligen med måltider (PC) eller 200 mg två gånger dagligen (Kolin) | Kolin är en vanlig kostbrist. PC är nödvändigt för produktion av galla och skyddande gastrointestinal slemhinna barriär. |
| Mjölktistelfrö | 140 till 200 mg En till tre gånger dagligen | Hepatoprotective. Stöder leverglutationnivåer, stabiliserar gallsaltexportpump (BSEP) och aktiverar FXR-vägar. |
| berberin HCl | 500 mg två till tre gånger dagligen | förbättrar serumglukos och lipidprofiler, vilket också minskar leverfettinnehållet. |
| probiotika, inklusive stammar som B. longum, B. bifidum, S. thermophilus, L. rhamnosus, L. acidophilus och L. plantarum | 12 miljarder kolonibildande enheter (CFU) dagligen | förbättrad tarmepitelial barriärfunktion och minskad tarm-och systemisk inflammation. |
| Acetyl-glutation | 300 mg dagligen | förbättrar avgiftande förmåga hepatocyter. |
| N-acetylcystein (NAC) | 500-600 mg två gånger dagligen, bäst på tom mage | NAC blockerar förökningen av lipidperoxidation och stöder leverglutationnivåer. |
| Vitamin E (tokoferoler)
eller tokotrienoler |
400 till 1200 IE dagligen med mat
200 till 300 mg två gånger dagligen med mat |
skyddande antioxidant.
tokotrienoler dämpar triglyceridackumulering genom att reglera fettsyrasyntas och karnitinpalmitoyltransferasenzymer, vilket leder till en minskning av leverinflammation och endoplasmatisk retikulumspänning. |
| Omega-3 essentiella fettsyror | 2 – 4 g dagligen, med måltider | Omega-3 fleromättade fettsyror är kända för att nedreglera sterolreglerande elementbindande protein-1c och uppreglera peroxisomproliferatoraktiverad receptor alfa, vilket gynnar fettsyraoxidation och reducerar steatos. |