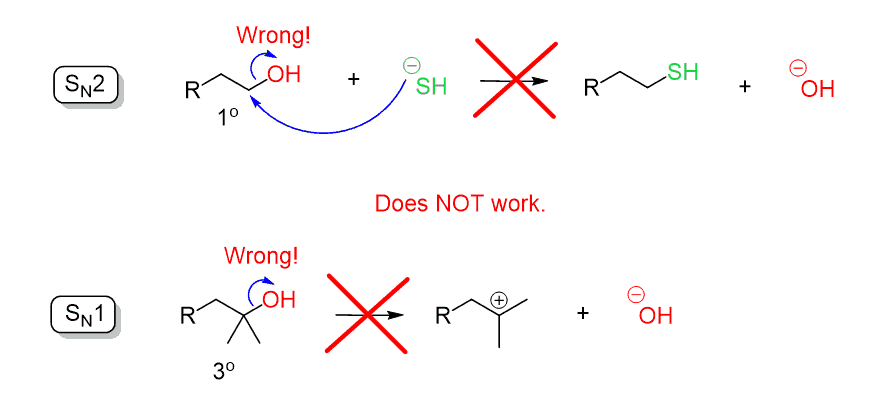
置換反応を議論するとき、水酸化物イオン(–OH)は非常に強い塩基であるため、脱離基が悪いと述べたことを覚えておいてください。 そのため、ああなれを除名することができるよう直接的求核攻撃にSN2はSN1反応:
片道換算するアルコールに置換反応がアルキルハロゲン化合物で反応させることによりその強い酸としては、塩酸、HBr、こんにちはや塩化チオニル(SOCl2)またはリンtribromide(PBr3). どちらのアプローチにおいても、この変換の背後にある原理は、OHを良好な離脱基に変換することであった。

これらの方法に加えて、P−トルエンスルホニル塩化物(Tscl)、メタンスルホニル塩化物(Mscl)、およびトリフルオロメタンスルホニル塩化物(Tfcl)のようなスルホニル塩化物と反応させることによって、O Hを良好な脱離基に変換することもできる。:

得られた生成物は、トシル酸塩(-OTs)、メシル酸塩(-OMs)およびトリフラート(-OTf)と呼ばれ、これらはすべて優れた脱離基であり、置換および脱離反応に使用することが:

さて、問題は、なぜ私たちの生活を複雑にし、酸との反応がうまくいくならば、トシル酸塩とメシル酸塩に対処する必要があるのでしょうか?
まあ、一般的に、アルキルスルホン酸塩の使用は、反応の立体化学を制御し、強酸の使用を避けるためのHX酸のより良い代替手段です。
では、反応の立体化学には正確に何が有益ですか?
覚えておいてください、酸を使用することの一つの問題は、カルボカチオンを形成し、特定のアルコールの立体化学と再配列の損失につながる可能性:

アルコールとは異なり、メシル酸塩およびトシル酸塩は、常に酸ではなくNaClまたはNaBrなどの塩と反応する。 塩の使用は、ハロゲンが陽子によって抑制されず、反応がSN2機構によって進行するため、ハロゲンが良好な求核剤の形態であることを保証するこ OHはすでに良好な脱離であるため、酸を使用する必要はなく、これは反応がより穏やかな条件で行われるため、別の利点である。
メシル酸塩とトシル酸塩はアルコールのハロゲン化にのみ使用されていないことにも言及する価値があります。 それらは簡単な取り替えおよび除去の反作用に加わることができる後でよい去るグループにオハイオ州を変えます:
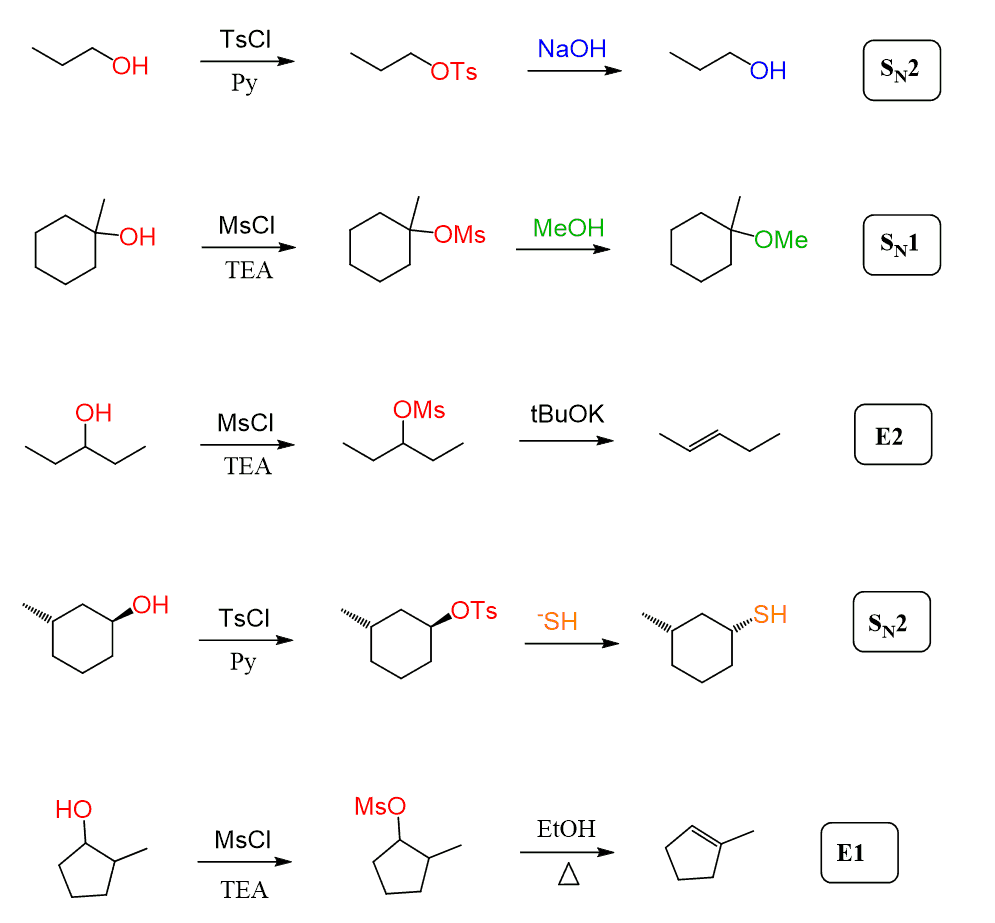
さて、我々は、この時点で、これらの試薬を使用するアイデアを議論してきましたが、どのように動作しますか、メシル化とトシル化のメカニズムは何ですか?
これに1つずつ対処しましょう:
良い求核剤と2つの反応を比較しましょう:

第二のものは非常にうまく動作しながら、どのように最初の反応が動作しません来ますか? TosylateがOHよりも優れた脱離基である理由は何ですか?
共鳴安定化を思い出したら、よくやった–それはそれです。 OH基の酸素は単独で完全な負電荷を有するが、スルホン酸イオンは水酸基の唯一のものよりも優れている負電荷を処理するための3つの酸素を有:

(R)-2-ブタノールをトシル酸塩に変換し、続いてSN2機構を介して置換反応を起こすメカニズムについて議論しましょう。
最初のステップでは、アルコールは塩化物を置き換えるために硫黄を攻撃する求核剤として作用する。
立体中心を持つ炭素はこのステップに関与せず、その構成は依然として保持されていることに注意してください:

ピリジンを塩基として添加して中間体を脱プロトン化し、トルエンスルホン酸エステル(トシル酸塩)を形成するプロセスをスピードアップする。
このステップの後、OHは求核剤によって追い出されることができる良好な脱離基に変わります:

メシル化はわずかに異なるメカニズムによって行く。 ここでの最初のステップは、スルフェンを形成するメタンスルホニルクロリドからの塩基による酸性γプロトンの脱プロトン化である。 スルフェンは非常に求電子性であり、アルコールと迅速に反応する:

これらの反応は、多くの場合、我々は学部のコースでtosylationのために見たメカニズムで示されます。
tosylationと同じメカニズムがmesylationのために受諾可能であるかどうか教官に尋ねなさい。
反応性スルフェン中間体の形成は、tsclと非常にゆっくりと反応するため、第三級アルコールを扱うときにメシル酸塩にわずかな利点を与える。
トシル化の利点は、それがより大きな分子であり、いくつかの液体アルコールを固体に変えることであり、取り扱いが容易であるため、時には好まれる。 また、tosylatesの芳香環はTLCの版のよりよい視覚化を可能にする。
しかし、もう一度、それが大きいという事実は、その調製を少し遅くし、置換反応においても反応性がない。
トリフラートイオンも優れた脱離基であるが、学部の教科書ではあまり取り上げられていないため、対応するメカニズムについてはあまり詳しくは触れない。
しかし、概念的には違いはありません–それはTsやMsの代わりにTfと略されるだけであり、運動に取り組むときには単に良い離脱グループとして扱うこ
SN1反応におけるメシル酸塩とトシル酸塩
上記のすべての例では、トシル酸塩とメシル酸塩は、ハロゲン化アルキルに変換されると常に強い求核剤と反応し、これらの場合、SN2機構が優勢であることが分かっている。
ただし、第三級アルコールまたは弱い求核剤を使用すると、メシル酸塩およびトシル酸塩もSN1およびE1脱離反応を受ける可能性があります:

一般に、これらは、反応がSN1、SN2、E1またはE2機構を通過するかどうかを決定する原理には影響しない。

求核置換-脱離実践クイズ
今すぐ取る