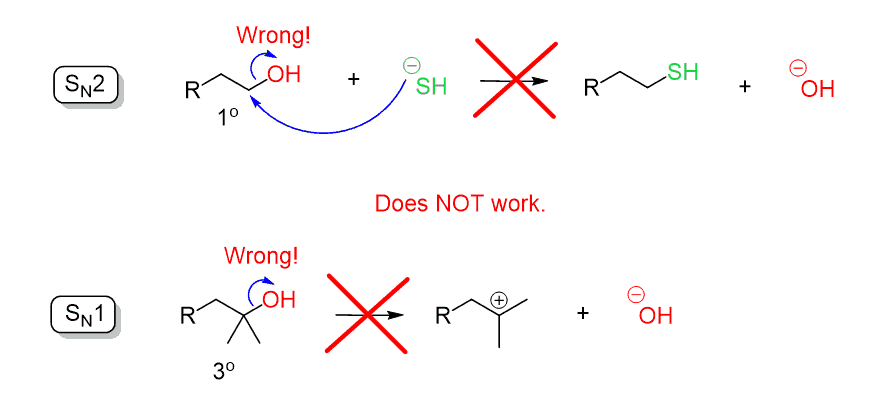
amintiți–vă când discutați despre reacțiile de substituție, am spus că ionul hidroxid (- OH) este un grup slab de plecare, deoarece este o bază destul de puternică. Prin urmare, OH nu poate fi expulzat printr-un atac nucleofil direct într-o reacție SN2 sau SN1:
o modalitate de conversie a alcoolilor în reacțiile de substituție la halogenuri de alchil este prin reacția lor cu acizi puternici precum HCl, HBr și HI sau folosind clorură de tionil (SOCl2) sau tribromură de fosfor (PBr3). În ambele abordări, principiul din spatele acestei transformări a fost transformarea OH într-un grup bun care pleacă.

în plus față de aceste metode, OH poate fi, de asemenea, transformat într-un grup de plecare bun prin reacția cu cloruri de sulfonil, cum ar fi clorura de P-Toluensulfonil (TsCl), clorura de Metansulfonil (MsCl) și clorura de Trifluorometansulfonil (TfCl):

produsele rezultate se numesc Tosilați (- OTs), Mesilați (- OMs) și Triflați (- OTf), toate acestea fiind grupuri excelente de plecare și pot fi utilizate în reacțiile de substituție și eliminare:

acum, întrebarea este de ce trebuie să ne complicăm viața și să ne ocupăm de tosilați și mesilați dacă reacția cu acizii funcționează bine, nu?
Ei bine, în general, utilizarea sulfonaților de alchil este o alternativă mai bună la acizii HX pentru controlul stereochimiei reacției și, de asemenea, evitarea utilizării acizilor puternici.
deci, ce anume este benefic pentru stereochimia reacției?
amintiți-vă, o problemă cu utilizarea acizilor este mecanismul SN1 posibil care formează o carbocație și poate duce la pierderea stereochimiei și rearanjări pentru anumiți alcooli:

spre deosebire de alcooli, mesilații și tosilații reacționează întotdeauna cu o sare precum NaCl sau NaBr și nu cu acizii. Utilizarea sărurilor este de a se asigura că halogenii sunt sub formă de nucleofili buni, deoarece nu sunt suprimați de protoni și reacția trece prin mecanismul SN2. Nu este nevoie să utilizați un acid, deoarece OH este deja o plecare bună, ceea ce reprezintă un alt avantaj, deoarece reacția se desfășoară în condiții mai blânde.
de asemenea, merită menționat faptul că mesilații și tosilații nu sunt utilizați numai pentru halogenarea alcoolilor. Ei transformă simplu OH într-un grup bun de plecare, după care pot participa la orice reacție de substituție și eliminare:
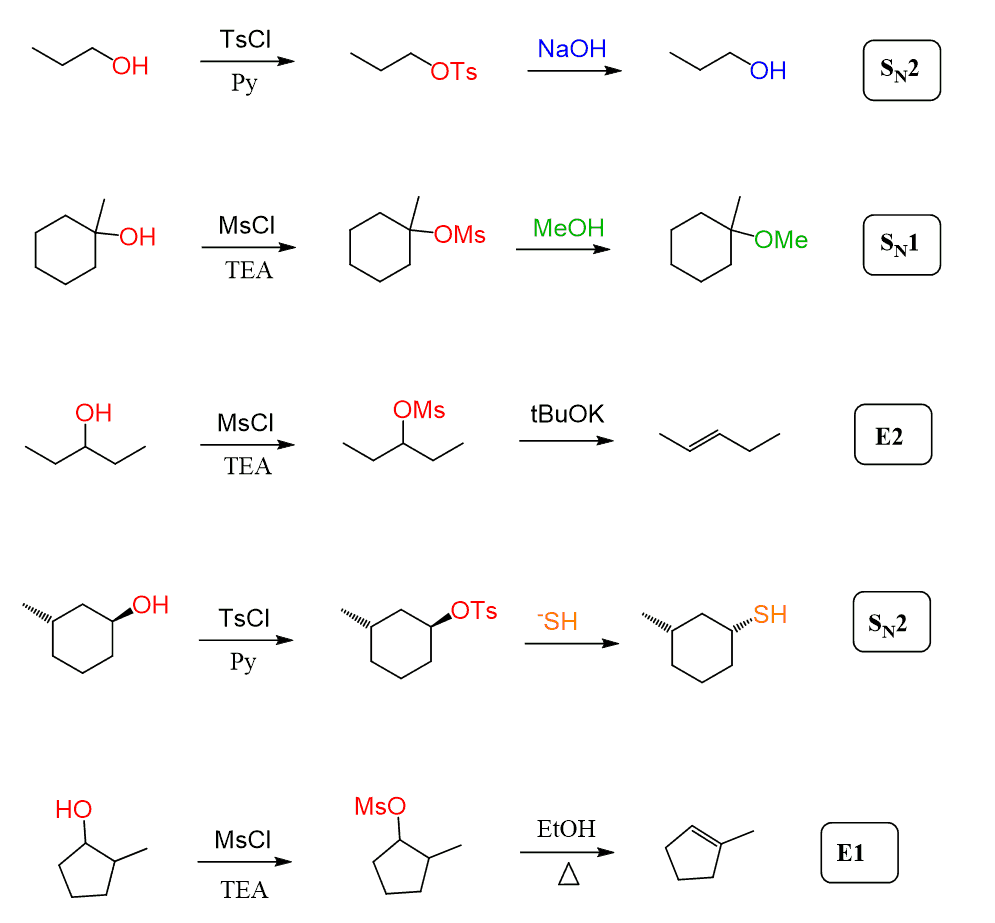
bine, am discutat, în acest moment, ideea utilizării acestor reactivi, dar cum funcționează, care este mecanismul de mezilare și tosilare?
să abordăm acest lucru unul câte unul:
să comparăm două reacții cu un nucleofil bun:

cum se face că prima reacție nu funcționează în timp ce a doua funcționează foarte bine? De ce este tosilatul un grup de plecare mai bun decât OH?
dacă ați amintit stabilizarea rezonanței, bine făcut – asta este. În timp ce oxigenul grupului OH poartă sarcina negativă completă pe cont propriu, ionul sulfonat are trei oxigeni pentru a gestiona sarcina negativă, care este mai bună decât singura din gruparea hidroxil:

să discutăm mecanismul de conversie A (R)-2-Butanolului într-un tosilat urmat de o reacție de substituție prin mecanismul SN2.
în prima etapă, alcoolul acționează ca un nucleofil care atacă sulful pentru a înlocui clorura.
observați că carbonul cu Centrul stereogen nu este implicat în această etapă și configurația sa este încă păstrată:

piridina este adăugată ca bază pentru a deprotona intermediarul și a accelera procesul de formare a esterului Toluenesulfonat (tosilat).
după acest pas, OH este acum transformat într-un grup bun care pleacă, care poate fi dat afară de un nucleofil:

Mesilarea are un mecanism ușor diferit. Primul pas aici este deprotonarea protonului acid de la baza din clorura de metansulfonil care formează un sulfen. Sulfenul este foarte electrofil și reacționează rapid cu alcoolul:

aceste reacții vor fi adesea arătate cu mecanismul pe care l-am văzut pentru tosilare în cursurile universitare.
întrebați instructorul dacă același mecanism ca și pentru tosilare este acceptabil pentru mesilare.
formarea intermediarului reactiv de sulfen oferă un ușor avantaj mesilatului atunci când se lucrează cu alcooli terțiari, deoarece reacționează foarte lent cu TsCl.
avantajul tosilării este că este o moleculă mai mare și transformă alcoolul lichid în solide, care uneori sunt preferate, deoarece sunt mai ușor de manevrat. De asemenea, inelul aromatic al tosilaților permite o vizualizare mai bună pe o placă TLC.
dar încă o dată, faptul că este mai mare face ca pregătirea sa să fie puțin mai lentă și nu este la fel de reactivă și în reacțiile de substituție.
ionul Triflat este, de asemenea, un grup excelent de plecare, cu toate acestea, nu este acoperit atât de mult în manualele universitare, prin urmare, nu vom intra prea mult în detalii despre mecanismele corespunzătoare.
cu toate acestea, conceptual, nu există nicio diferență – va fi prescurtat doar ca Tf în loc de Ts sau Ms și îl puteți trata pur și simplu ca un grup bun de plecare atunci când lucrați la un exercițiu.
Mesilați și Tosilați în reacțiile SN1
în toate exemplele de mai sus, am văzut că tosilații și mesilații reacționează întotdeauna cu nucleofili puternici atunci când sunt transformați în halogenuri de alchil și, în aceste cazuri, mecanismul SN2 va predomina.
cu toate acestea, mesilații și tosilații pot suferi, de asemenea, reacții de eliminare SN1 și E1 atunci când se utilizează un alcool terțiar sau un nucleofil slab:

în general, acestea nu afectează principiile de a determina dacă reacția trece printr-un mecanism SN1, SN2, E1 sau E2.

substituție nucleofilă și practică de eliminare test
ia acum