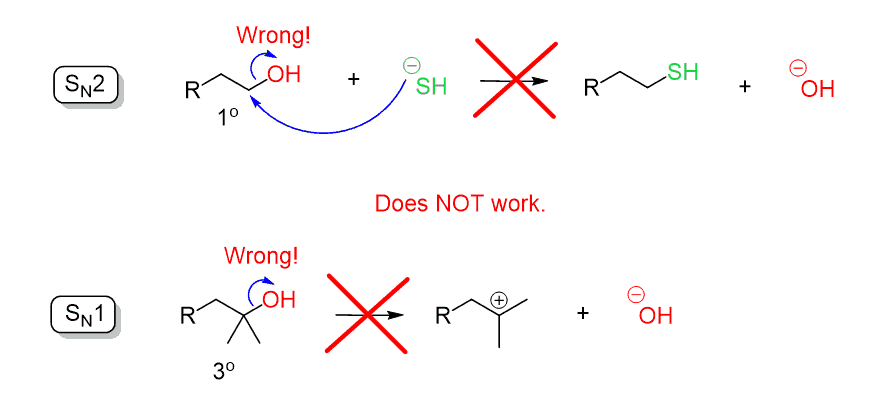
Husk, når vi diskuterer substitutionsreaktionerne, sagde vi, at hydroksidionen (–OH) er en dårlig forlader gruppe, da det er en ret stærk base. Derfor kan OH ikke udvises ved et direkte nukleofilt angreb i en SN2-eller SN1-reaktion:
en måde at omdanne alkoholer i substitutionsreaktioner på alkylhalogenider er ved at reagere dem med stærke syrer, såsom HCI, HBr og HI eller ved hjælp af thionylchlorid (SOCl2) eller phosphorstribromid (PBr3). I begge tilgange var princippet bag denne transformation omdannelsen af OH til en god forlader gruppe.

ud over disse metoder kan OH også omdannes til en god afgangsgruppe ved at reagere med sulfonylchlorider, såsom p-Toluensulfonylchlorid (TsCl), Methansulfonylchlorid (MsCl) og Trifluoromethansulfonylchlorid (TfCl):

de resulterende produkter kaldes Tosylater (- OTs), Mesylater (- OMs) og Triflater (- OHF), som alle er fremragende forlader grupper og kan bruges i substitutions-og eliminationsreaktioner:

nu er spørgsmålet, Hvorfor skal vi komplicere vores liv og håndtere tosylater og mesylater, hvis reaktionen med syrer fungerer fint, ikke?
generelt er brugen af alkylsulfonater et bedre alternativ til HKS-syrer til styring af reaktionens stereokemi og også undgåelse af brugen af stærke syrer.
så hvad er nøjagtigt gavnligt for reaktionens stereokemi?
husk, et problem med at bruge syrerne er den mulige SN1-mekanisme, der danner en carbocation og kan føre til tab af stereokemi og omlejringer for visse alkoholer:

i modsætning til alkoholer omsættes mesylater og tosylater altid med et salt som NaCl eller NaBr og ikke syrerne. Anvendelsen af salte er at sikre, at halogenerne er i en form for gode nukleofiler, da de ikke undertrykkes af protonerne, og reaktionen går ved SN2-mekanismen. Ingen grund til at bruge en syre, da OH allerede er en god afgang, hvilket er en anden fordel, fordi reaktionen udføres under mildere forhold.
det er også værd at nævne, at mesylater og tosylater ikke kun anvendes til halogenering af alkoholer. De konverterer simpelthen OH til en god forladelsesgruppe, hvorefter de kan deltage i enhver substitutions-og eliminationsreaktion:
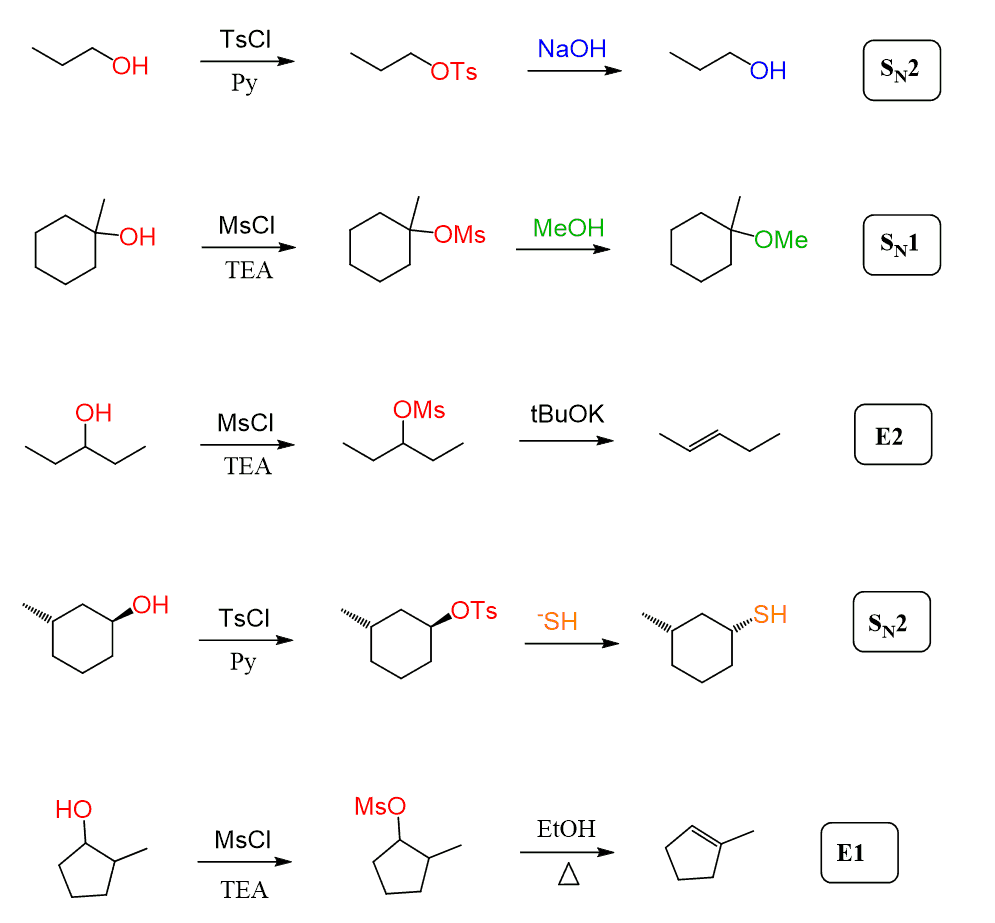
Okay, vi har diskuteret på dette tidspunkt ideen om at bruge disse reagenser, men hvordan fungerer de, hvad er mekanismen for mesylation og tosylation?
lad os adressere denne en efter en:
lad os sammenligne to reaktioner med en god nukleofil:

Hvordan kommer den første reaktion ikke, mens den anden fungerer meget pænt? Hvorfor er tosylate en bedre forlader gruppe end OH?
hvis du huskede resonanstabiliseringen, godt klaret – det er hvad det er. Mens ilt fra OH-gruppen bærer den fulde negative ladning alene, har sulfonationen tre ilt til at håndtere den negative ladning, som er bedre end den eneste i hydroksyl-gruppen:

lad os diskutere mekanismen til konvertering (R)-2-Butanol til et tosylat efterfulgt af en substitutionsreaktion via SN2-mekanismen.
i det første trin fungerer alkoholen som en nukleofil, der angriber svovlet for at erstatte klorid.
Bemærk, at kulstof med det stereogene center ikke er involveret i dette trin, og dets konfiguration bevares stadig:

pyridinen tilsættes som en base for at deprotonere mellemproduktet og fremskynde processen med dannelse af Toluensulfonatesteren (tosylat).
efter dette trin er OH nu omdannet til en god forlader gruppe, som kan sparkes ud af en nukleofil:

Mesylation går af en lidt anden mekanisme. Det første trin her er deprotonering af den sure purpurproton ved basen fra methansulfonylchlorid, der danner en sulfen. Sulfen er meget elektrofil og reagerer hurtigt med alkoholen:

disse reaktioner vil ofte blive vist med den mekanisme, vi så til tosylering i bacheloruddannelser.
spørg din instruktør, om den samme mekanisme som for tosylering er acceptabel til mesylation.
dannelsen af det reaktive sulfen-mellemprodukt giver en lille fordel ved mesylat, når man arbejder med tertiære alkoholer, da de reagerer meget langsomt med TsCl.
fordelen ved tosylering er, at det er et større molekyle og omdanner noget flydende alkohol til faste stoffer, som undertiden foretrækkes, da de er lettere at håndtere. Tosylaternes aromatiske ring giver også mulighed for bedre visualisering på en TLC-plade.
men endnu en gang gør det faktum, at det er større, sin forberedelse lidt langsommere, og det er ikke så reaktivt i substitutionsreaktioner også.
Triflate ion er også en fremragende afgangsgruppe, men den er ikke dækket så meget i Bachelor-lærebøger, derfor vil vi ikke gå for meget i detaljer om de tilsvarende mekanismer.
men konceptuelt er der ingen forskel – det forkortes kun som Tf i stedet for Ts eller Ms, og du kan simpelthen behandle det som en god afgangsgruppe, når du arbejder på en øvelse.
Mesylater og Tosylater i SN1-reaktioner
i alle eksemplerne ovenfor har vi set, at tosylater og mesylater altid omsættes med stærke nukleofiler, når de omdannes til alkylhalogenider, og i disse tilfælde vil SN2-mekanismen dominere.
imidlertid kan mesylater og tosylater også gennemgå SN1-og E1-eliminationsreaktioner, når der anvendes en tertiær alkohol eller en svag nukleofil:

generelt påvirker disse ikke principperne for at bestemme, om reaktionen går gennem en SN1 -, SN2 -, E1-eller E2-mekanisme.

nukleofil substitutions-og Eliminationspraksis
Tag nu