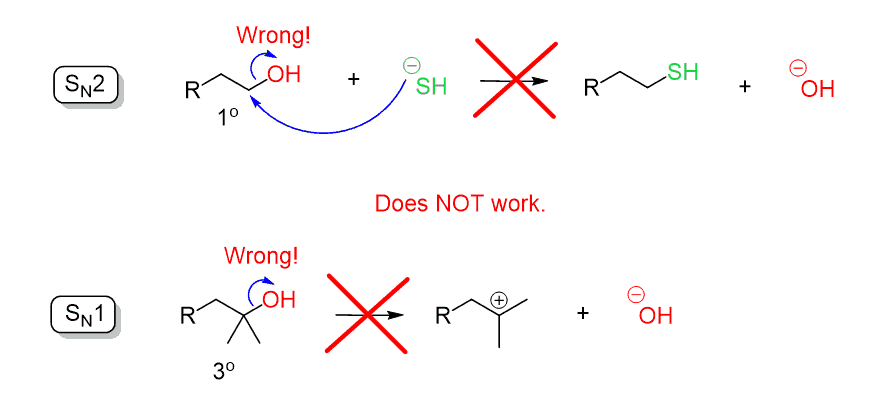
lembre–se ao discutir as reações de substituição, dissemos que o íon hidróxido (- OH) é um grupo de saída pobre, uma vez que é uma base bastante forte. Portanto, OH não podem ser expulsos por nucleophilic ataque em um SN2 ou reação SN1:
Uma forma de conversão de álcoois em substituição reações de halogenetos de alquilo está reagindo-los com ácidos fortes, tais como HCl, HBr e HI ou usando thionyl cloreto (SOCl2) ou fósforo tribromide (PBr3). Em ambas as abordagens, o princípio por trás desta transformação foi a conversão do OH em um bom grupo de saída.

além desses métodos, a AH também pode ser convertido em um bom deixando grupo reagindo com sulfonil cloretos, como a p-Toluenesulfonyl (cloreto de TsCl), Methanesulfonyl (cloreto de MsCl), e Trifluoromethanesulfonyl (cloreto de TfCl):

Os produtos resultantes são chamados de Tosylates (OTs), Ergolóides (-OMs) e Triflates (-OTf) os quais são excelentes deixando grupos e pode ser usado em reações de substituição e eliminação:

Agora, a pergunta é por que precisamos para complicar a nossa vida e lidar com tosylates e ergolóides, se a reacção com ácidos funciona muito bem, certo?
Well, in general, the use of alkyl sulfonates is a better alternative to HX acids for controlling the stereochemistry of the reaction and also avoiding the use of strong acids. Então, o que exatamente é benéfico para a estereoquímica da reação?
Lembre-se, um problema com o uso de ácidos é o possível mecanismo SN1 que forma um carbocation e pode levar à perda de estereoquímica e rearranjos para certos álcoois:

ao contrário de álcoois, ergolóides e tosylates são sempre reagiu com um sal, tais como NaCl ou NaBr e não ácidos. O uso de sais é para garantir que os halogéneos estão em uma forma de bons nucleófilos como eles não são suprimidos pelos prótons e a reação vai pelo mecanismo SN2. Não há necessidade de usar um ácido já que o OH já é uma boa saída, o que é outra vantagem porque a reação é realizada em condições mais amenas.Também vale a pena mencionar que mesilatos e tosilatos não são usados apenas para a halogenação de álcoois. Eles simples converter o OH em um bom deixando o grupo após o qual eles podem participar de qualquer substituição e eliminação de reação:
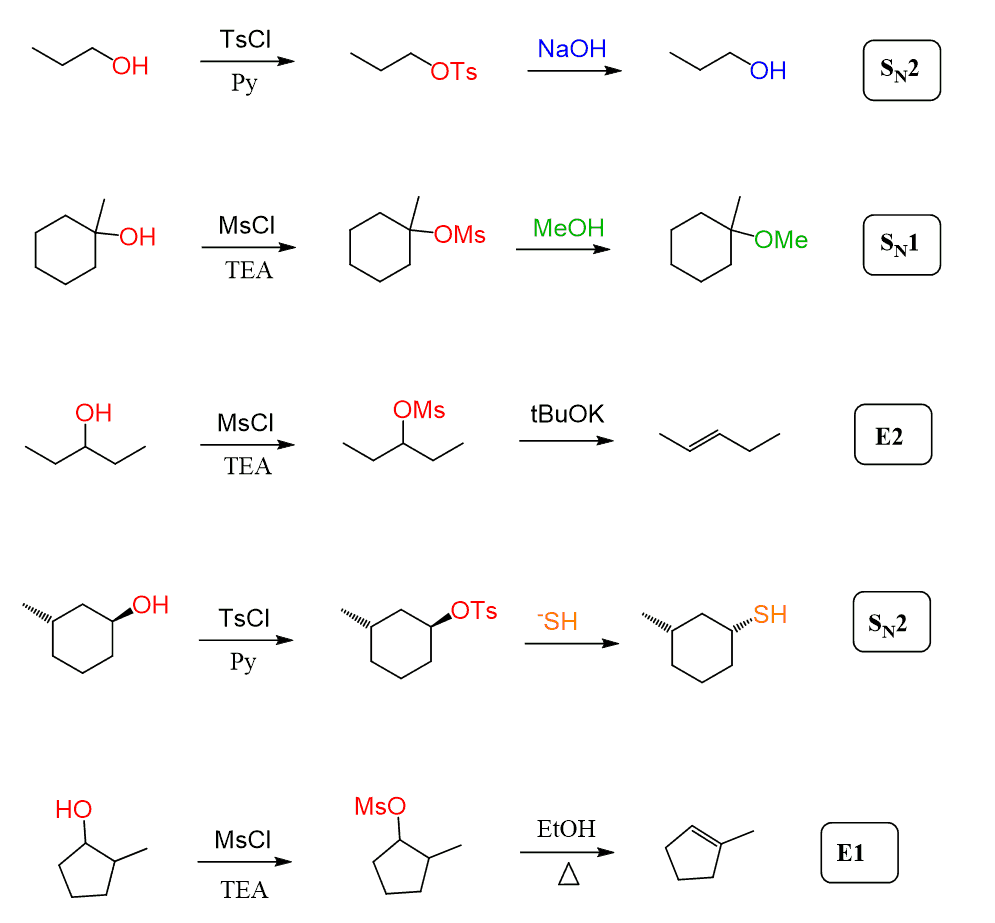
tudo Bem, nós discutimos, neste ponto, a ideia de utilizar estes reagentes mas como eles funcionam, que é o mecanismo de mesylation e tosylation?
Vamos abordar este um por um:
Vamos comparar duas reações com um bom nucleophile:

Como é a primeira reação não funciona, enquanto o segundo funciona muito bem? Porque é que a tosilato é um grupo de saída melhor do que o OH?Se você se lembrou da estabilização da ressonância, bem feito – é o que é. Enquanto o oxigênio do grupo OH carrega a carga negativa completa por si só, o íon sulfonato tem três oxigenos para lidar com a carga negativa que é melhor do que o único no grupo hidroxilo:

vamos discutir o mecanismo de conversão (R)-2-Butanol para um tosilato seguido por uma reação de substituição através do mecanismo SN2.No primeiro passo, o álcool atua como um nucleófilo atacando o enxofre para substituir o cloreto.
Observe que o carbono com o stereogenic centro não está envolvido nesta etapa e a sua configuração ainda é mantida:

O nucleotides é adicionado como uma base para deprotonate intermediário e acelerar o processo de formação de Toluenesulfonate éster (tosylate).
após este passo, o OH é agora transformado em um bom grupo de saída que pode ser expulso por um nucleófilo:

a Mesilação passa por um mecanismo ligeiramente diferente. O primeiro passo aqui é a desprotonação do próton ácido ɑ pela base do cloreto de metanossulfonila que forma um sulfeno. O sulfeno é muito electrofílico e reage rapidamente com o álcool:

estas reacções serão frequentemente mostradas com o mecanismo que vimos para a tosilação em cursos de graduação.Pergunte ao seu instrutor se o mesmo mecanismo que para a tosilação é aceitável para a mesilação.
a formação do intermediário reativo do sulfeno dá uma pequena vantagem ao mesilato quando se trabalha com álcoois terciários, uma vez que eles reagem muito lentamente com TsCl.
a vantagem da tosilação é que é uma molécula maior e transforma algum álcool líquido em sólidos que às vezes são preferidos, uma vez que são mais fáceis de manusear. Além disso, o anel aromático dos tosilatos permite uma melhor visualização em uma placa TLC.
mas, mais uma vez, o facto de ser maior torna a sua preparação um pouco mais lenta e não é tão reactiva nas reacções de substituição também.
o íon Triflato é também um excelente grupo de saída, no entanto, ele não é tanto coberto em livros de graduação, portanto, não iremos muito em detalhes sobre os mecanismos correspondentes.
no entanto, conceptualmente, não há diferença – ele só será abreviado como Tf em vez de Ts ou Ms e você pode simplesmente tratá-lo como um bom grupo de saída ao trabalhar em um exercício.
Ergolóides e Tosylates em Reações SN1
Em todos os exemplos acima, temos visto que tosylates e ergolóides são sempre reagiu com forte nucleophiles quando convertido para halogenetos de alquilo e, nesses casos, o mecanismo SN2 vai predominar.
no Entanto, ergolóides e tosylates também podem se submeter SN1 e E1 eliminação reações quando um álcool terciário ou um fraco nucleophile é usado:

Em geral, estas não afetam os princípios de determinar se a reação passa por um SN1, SN2, E1 ou E2 mecanismo.

Nucleophilic Substituição e Eliminação da Prática Quiz
Tirar Agora