Recuerde que al discutir las reacciones de sustitución, dijimos que el ion hidróxido (–OH) es un grupo salientes pobre ya que es una base bastante fuerte. Por lo tanto, el OH no puede ser expulsado por un ataque nucleofílico directo en una reacción SN2 o SN1:
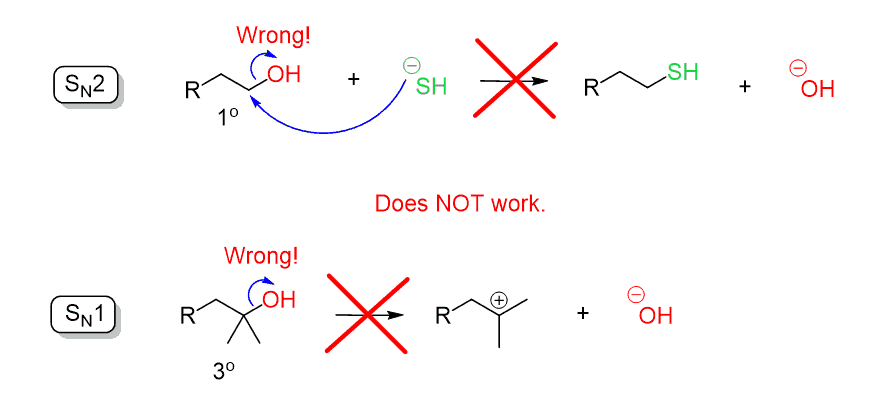
Una forma de convertir alcoholes en reacciones de sustitución a haluros de alquilo es reaccionándolos con ácidos fuertes como HCl, HBr e HI o usando cloruro de tionilo (SOCl2) o tribromuro de fósforo (PBr3). En ambos enfoques, el principio detrás de esta transformación fue la conversión del OH en un buen grupo de partida.

Además de estos métodos, el OH también se puede convertir en un buen grupo saliente al reaccionar con cloruros de sulfonilo como cloruro de p-toluenosulfonilo (TsCl), cloruro de metanosulfonilo (MsCl) y cloruro de trifluorometanosulfonilo (TfCl):

Los productos resultantes se llaman Tosilatos (- OTs), Mesilatos (- OMs) y Triflatos (- OTf), todos los cuales son excelentes grupos de salida y se pueden usar en reacciones de sustitución y eliminación:

Ahora, la pregunta es por qué necesitamos complicar nuestras vidas y tratar con tosilatos y mesilatos si la reacción con ácidos funciona bien, ¿verdad?
Bueno, en general, el uso de sulfonatos de alquilo es una mejor alternativa a los ácidos HX para controlar la estereoquímica de la reacción y también evitar el uso de ácidos fuertes.
Entonces, ¿qué es exactamente beneficioso para la estereoquímica de la reacción?
Recuerde, un problema con el uso de los ácidos es el posible mecanismo SN1 que forma un carbocatión y puede conducir a la pérdida de estereoquímica y reordenamientos para ciertos alcoholes:

A diferencia de los alcoholes, los mesilatos y los tosilatos siempre reaccionan con una sal como NaCl o NaBr y no con los ácidos. El uso de sales es para asegurar que los halógenos estén en una forma de buenos nucleófilos, ya que no son suprimidos por los protones y la reacción pasa por el mecanismo SN2. No es necesario usar un ácido, ya que el OH ya es una buena partida, lo que es otra ventaja porque la reacción se lleva a cabo en condiciones más suaves.
También vale la pena mencionar que los mesilatos y tosilatos no se utilizan solo para la halogenación de alcoholes. Simplemente convierten el OH en un buen grupo de salida, después de lo cual pueden participar en cualquier reacción de sustitución y eliminación:
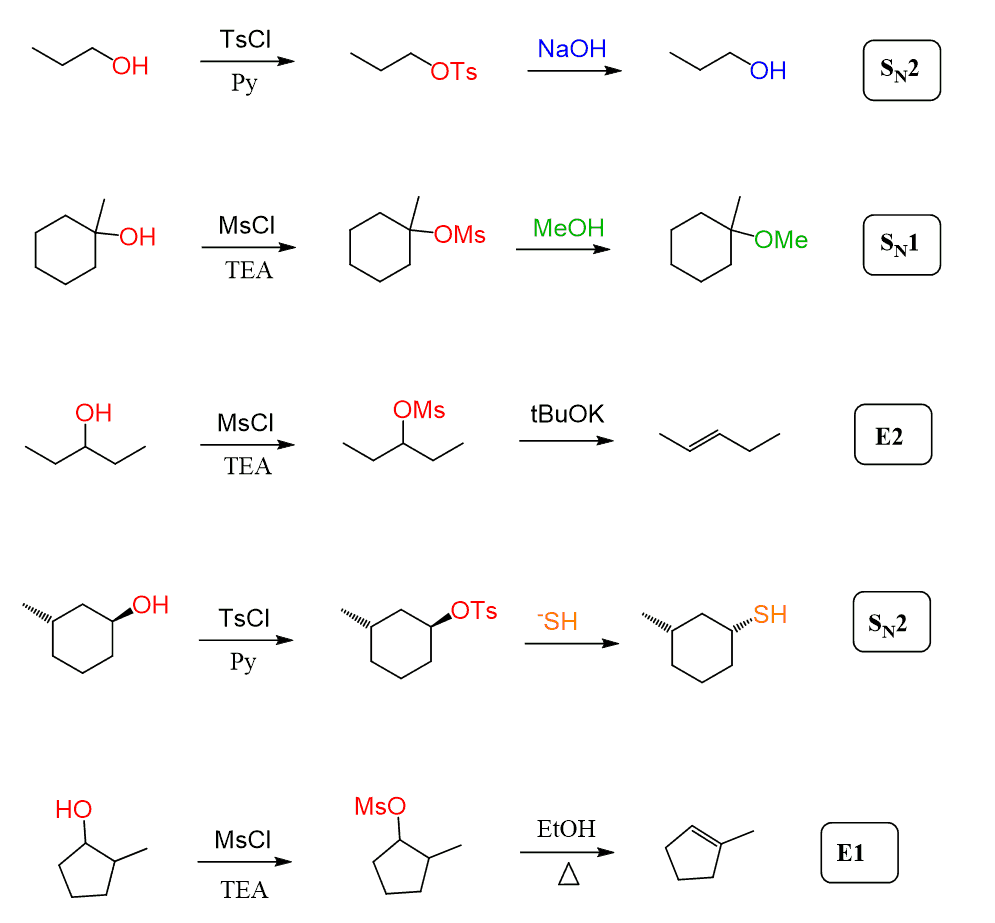
Bien, hemos discutido, en este punto, la idea de usar estos reactivos, pero ¿cómo funcionan, cuál es el mecanismo de mesilación y tosilación?
Abordemos esto uno por uno:
Comparemos dos reacciones con un buen nucleófilo:

¿Cómo es que la primera reacción no funciona mientras que la segunda funciona muy bien? ¿Por qué el tosilato es un grupo de salida mejor que el OH?
Si recordaste la estabilización de resonancia, bien hecho, eso es lo que es. Mientras que el oxígeno del grupo OH soporta la carga negativa completa por sí solo, el ion sulfonato tiene tres oxígenos para manejar la carga negativa, que es mejor que el único en el grupo hidroxilo:

Discutamos el mecanismo para convertir (R) – 2-Butanol en un tosilato seguido de una reacción de sustitución a través del mecanismo SN2.
En el primer paso, el alcohol actúa como un nucleófilo que ataca el azufre para reemplazar el cloruro.
Observe que el carbono con el centro estereogénico no está involucrado en este paso y su configuración aún se mantiene:

La piridina se agrega como base para desprotonar el intermedio y acelerar el proceso de formación del éster de toluenosulfonato (tosilato).
Después de este paso, el OH se convierte ahora en un buen grupo de salida que puede ser expulsado por un nucleófilo:

La mesilación pasa por un mecanismo ligeramente diferente. El primer paso aquí es la desprotonación del protón ácido por la base del cloruro de metanosulfonilo que forma un sulfeno. El sulfeno es muy electrofílico y reacciona rápidamente con el alcohol:

Estas reacciones a menudo se mostrarán con el mecanismo que vimos para la tosilación en los cursos de pregrado.
Pregunte a su instructor si el mismo mecanismo que para la tosilación es aceptable para la mesilación.
La formación del intermedio reactivo de sulfeno da una ligera ventaja al mesilato cuando se trabaja con alcoholes terciarios, ya que reaccionan muy lentamente con TsCl.
La ventaja de la tosilación es que es una molécula más grande y convierte un poco de alcohol líquido en sólidos que a veces se prefieren ya que son más fáciles de manejar. Además, el anillo aromático de los tosilatos permite una mejor visualización en una placa de TLC.
Pero una vez más, el hecho de que sea más grande hace que su preparación sea un poco más lenta y no sea tan reactiva en las reacciones de sustitución también.
El ion triflato también es un excelente grupo de salida, sin embargo, no está cubierto tanto en los libros de texto de pregrado, por lo tanto, no entraremos demasiado en detalles sobre los mecanismos correspondientes.
Sin embargo, conceptualmente, no hay diferencia: solo se abreviará como Tf en lugar de Ts o Ms y simplemente puede tratarlo como un buen grupo de partida cuando trabaje en un ejercicio.
Mesilatos y Tosilatos en Reacciones SN1
En todos los ejemplos anteriores, hemos visto que los tosilatos y mesilatos siempre reaccionan con nucleófilos fuertes cuando se convierten en haluros de alquilo y, en estos casos, predominará el mecanismo SN2.
Sin embargo, mesilatos y tosilatos también pueden sufrir reacciones de eliminación SN1 y E1 cuando se utiliza un alcohol terciario o un nucleófilo débil:

En general, esto no afecta a los principios para determinar si la reacción pasa por un mecanismo SN1, SN2, E1 o E2.

Sustitución Nucleófila y Eliminación de la Práctica de la Prueba
Tomar Ahora