het VOORTGEZET MEDISCH ONDERWIJS
ARTIKEL
Belangrijke complicaties van chronische nierschade
ik van der WaltI; C R SwanepoelII; B MahalaIII; Een M MeyersIV
Correspondentie
ABSTRACTE
De complicaties van een chronische nierziekte (CKD) zijn dyslipidaemia hyperkaliëmie, metabole acidose, bloedarmoede, en bot-en minerale aandoeningen. Dyslipidemie kan worden behandeld met lipoproteïneverlagende middelen met een lage dichtheid. Statines zijn niet effectief in stadia 4 en 5 CKD, maar zijn geïndiceerd voor het voorkomen van de progressie van de ziekte in de eerdere stadia. Chronische acidose is onlangs een risicofactor gebleken voor de progressie van CKD nierdisfunctie. Daarom is behandeling verplicht. Praktisch moet dit bestaan uit 1 – 2 opgehoopte theelepels natriumbicarbonaat 2-3 keer per dag, wat een goedkope en veilige therapie is die de bloeddruk ondanks de verhoogde natriumspiegel niet verhoogt. De streefwaarden voor hemoglobine liggen volgens internationale richtlijnen tussen 10 g/dL en 12 g / dL. De serumfosfaatspiegel wordt verhoogd in stadium 4 CKD, en met name in stadium 5 CKD, wat geassocieerd is met coronaire carotis en andere vasculaire calcificaties en kan leiden tot ischemische hartziekten, myocardinfarct en beroerte. Een verhoogde parathyroïdhormoonspiegel (secundaire hyperparathyroïdie) is ook een belangrijke risicofactor voor hart-en vaatziekten en wordt geassocieerd met verhoogde hypertensie en resistentie tegen de behandeling van CKD-geassocieerde anemie.
dyslipidemie
chronische nierziekte (CKD) wordt geassocieerd met veranderingen in lipoproteïnestructuur en-functie, waaronder:
- verminderde high-density lipoproteïne-cholesterol
- verhoogde intermediaire-density lipoproteïne
- verhoogde proatherogene lipidendeeltjes.
significantie van dyslipidemie controle
- succesvolle behandeling van dyslipidemie vermindert het risico op cardiovasculaire aandoeningen (CVD) en zou ook de afname van de nierfunctie moeten vertragen.
- omdat is aangetoond dat statines de uitscheiding van eiwit in de urine of albumine verminderen, worden ze aanbevolen voor CKD met proteïnurie.
- opmerkingen over het gebruik van statines in de fasen 3 – 5 CKD worden gegeven in Tabel 1.
- gelijktijdig gebruik van statines en fibraten verhoogt het risico op rabdomyolyse.
Target for low-density lipoproteïne cholesterol
- de Kidney Disease Outcomes Quality Initiative (KDOQI) richtlijnen bevelen het volgende aan voor dyslipidemietherapie bij CKD: in gevallen van low-density lipoproteïne cholesterol (LDL-C) <3.In geval van een LDL-C >3,5 mmol/l, dient een medicamenteuze behandeling overwogen te worden naast een aanpassing van de levensstijl, waaronder dieet, gewichtsbeheersing en lichaamsbeweging.
- het is essentieel dat LDL-C wordt verlaagd tot <1,8 mmol/L.
kdoqi richtlijnen voor cholesterolverlagingen bij CKD patiënten (2013):
- patiënten >50 jaar dienen een statine te krijgen.
- patiënten tussen 18 en 49 jaar dienen een statine te krijgen als een andere comorbiditeit aanwezig is.Ontvangers van een Niertransplantaat moeten een statine krijgen.
behandeling van hyperkaliëmie en metabole acidose
hyperkaliëmie
- naarmate de CKD in het stadium vordert, worden acidose en hyperkaliëmie waargenomen. Hyperkaliëmie wordt gedefinieerd als een serumkaliumspiegel >5,5 mmol/l hyperkaliëmie >7 mmol/L kan mogelijk een hartstilstand veroorzaken; dergelijke gevallen moeten als noodgevallen worden behandeld.
- indien ernstige hyperkaliëmie wordt waargenomen, ondanks de afwezigheid van een verminderde nierfunctie, dient pseudohyperkaliëmie, een artefact als gevolg van hemolyse van het bloedmonster, te worden overwogen.
- hyperkaliëmie is een risicofactor voor aritmieën. In gevallen van ernstige hyperkaliëmie moeten de noodniveaus worden bevestigd door ECG-afwijkingen zoals T-golven, verlenging van de PQ-tijden, gevolgd door het verdwijnen van de P-golf en verbreding van het QRS-complex. Patiënten met levensbedreigende ECG-bevindingen, bradycardie en hypotensie moeten onmiddellijk worden behandeld, gevolgd door een behandeling in combinatie met een nefroloog.
- geneesmiddelgeïnduceerde hyperkaliëmie bij CKD wordt voornamelijk veroorzaakt door renine-angiotensine-aldosteron-remmers zoals ACE-remmers, angiotensine II-receptorblokkers (ARB ‘ s) en spironolacton of overmatige inname van kaliumbevattend voedsel. Andere oorzaken zijn de toediening van β-blokkers, digoxine, niet-steroïde anti-inflammatoire geneesmiddelen (NSAID ‘ s), trimethoprim of pentamidine.
- CKD veroorzaakt door diabetische nefropathie kan gepaard gaan met hyporeninemisch hypoaldosteronisme, wat hyperkaliëmie kan veroorzaken ondanks een relatief goed bewaarde nierfunctie. Dit staat bekend als type IV renale tubulaire acidose.
spoedbehandeling
- de eerste stap is het stabiliseren van het myocardium. De intraveneuze toediening van calciumgluconaat verandert het plasmakalium niet, maar verbetert Tijdelijk het ECG. De toediening van calciumgluconaat 20 mL intraveneus gedurende 1 minuut kan worden herhaald als er binnen 3 – 5 minuten geen verbetering in het ECG optreedt.
- de tweede stap is het verschuiven van het Kalium van het extracellulaire naar het intracellulaire compartiment om te proberen de serumkaliumspiegel snel te verlagen. Dit kan op drie verschillende manieren:
- intraveneuze insuline gecombineerd met glucose. Dien 10 u kortwerkende insuline toe in combinatie met 50 mL 50% dextrose als bolus, gevolgd door een intraveneuze infusie van 5% dextrose om hypoglykemie te voorkomen.
- β2-agonist. Dien 20 mg salbutamol, een β2-agonist, toe door inademing gedurende 10 minuten, met inwerking van de werking ongeveer 30 minuten. (Dit is meestal niet nodig.)
- natriumbicarbonaat bij CKD-patiënten die nog niet worden gedialyseerd. Toediening van bicarbonaat kan het serumkalium verlagen door de renale kaliumexcretie te verhogen. Het effect is zeer traag en niet van toepassing in een acute situatie, tenzij de patiënt ernstige metabole acidose heeft die een behandeling met bicarbonaat nodig heeft.
- zodra de vorige tijdelijke maatregelen zijn uitgevoerd, worden verdere interventies ondernomen om kalium uit het lichaam te verwijderen.
- lisdiuretica zijn alleen succesvol bij patiënten met een adequate nierfunctie.
- de harswisselaar natriumpolystyreensulfonaat (Kexelaat) verwijdert kalium uit het bloed in de darm in ruil voor een gelijke hoeveelheid natrium. Het werkt traag en het plasmakalium begint pas binnen 1-2 uur af te nemen. Het kan mondeling worden gegeven of als een retentieklysma. De gegeven hoeveelheid varieert van 30 g tot 60 g. Dit kan worden herhaald, maar heeft de neiging om constipatie te veroorzaken.Hemodialyse is de voorkeursbehandeling voor patiënten met gevorderde CKD en ernstige hyperkaliëmie.
preventie
- dieetadvies over kaliumbeperking.
- vermijd geneesmiddelen die de renale excretie van kalium beïnvloeden, bijv. kaliumsparende diuretica, NSAID ‘s, ACE-remmers, ARB’ s.
- vermijd geneesmiddelen die interfereren met kaliumverschuivingen van de intracellulaire naar de extracellulaire compartimenten, bijvoorbeeld niet-selectieve β-blokkers.
- bij geselecteerde patiënten met voldoende residuele nierfunctie kan een behandeling met een lisdiureticum worden gebruikt om de urinaire kaliumuitscheiding te stimuleren.
metabole acidose
metabole acidose wordt gekenmerkt door:
- lage arteriële bloed pH (acidemie) (<7.35)
- verminderde serum HCO3-concentratie
- verlaagde pCO2 (door ademhalingscompensatie).
systemische effecten
metabole acidose kan leiden tot een verscheidenheid aan veranderingen in weefsels en organen, bijv.:
- cardiovasculaire veranderingen zoals tachycardie, bradycardie, hypotensie en hartfalen
- levensbedreigende hyperkaliëmie
- misselijkheid, braken en buikpijn
- verwardheid, met depressie van het centrale zenuwstelsel.
de geassocieerde symptomen en tekenen zijn afhankelijk van de snelheid en omvang van de daling van de pH en van de onderliggende pathologie.
uremische acidose
metabole acidose treedt op bij nierfalen als gevolg van een verminderd vermogen om H+ uit te scheiden of een onvermogen om ammoniak te produceren.
in de vroege stadia van CKD (GFR <40 mL/min) kan metabole acidose met een normale anion gap (AG) duidelijk worden. Naarmate de CKD vordert (GFR <20 mL/min), kan een hoge AG metabole acidose optreden.
in geavanceerde CKD is een verhoogde AG typisch vanwege de aanwezigheid van behouden zuren zoals sulfaten, fosfaten, uraat en hippuraat.
behandelingsprincipes
patiënten met metabole acidose zijn vaak zeer ziek en hun toestand neigt snel te verslechteren.
de routinematige toediening van natriumbicarbonaat is controversieel, hoewel dit moet worden gedaan om ernstige acidose te corrigeren.
de mogelijke complicaties van toediening van natriumbicarbonaat omvatten volumeoverbelasting, met name bij patiënten met nier-of hartfunctiestoornissen, hypernatriëmie, hypokaliëmie, hypocalciëmie en alkalose.
de benodigde hoeveelheid bicarbonaat (mmol) kan als volgt worden geschat:
target plasma HCO3 – (mmol/l) – current plasma HCO3 – (mmol/L) x 40% lichaamsgewicht (kg).Anemie bij CKD
anemie is de meest voorkomende complicatie van CKD en wordt geassocieerd met een sterk verminderde kwaliteit van leven. Een succesvolle behandeling van anemie bij nefropathie kan de afname van de nierfunctie verminderen. De streefwaarden voor hemoglobine zijn 10-12 g / dL bij de behandeling van anemie bij CKD. De behandeling is duur en daarom is rationele overweging verplicht.
renale anemie
renale anemie is typisch normochromisch normocytisch. Het wordt hoofdzakelijk veroorzaakt door de verminderde productie van erythropoëtine door de nier en gedeeltelijk door uremische toxines. Andere oorzaken die een rol kunnen spelen bij CKD, vooral bij dialysepatiënten, zijn:
- erytropoëtine resistentie (meest significant)
- beenmerg toxinen (nog geen geïsoleerd)
- beenmergfibrose, secundair aan hyperparathyreoïdie
- aanhoudende ontstekingsprocessen, bijv. onbehandelde infecties
- hematinedeficiëntie (ijzer, folaat en vitamine B12)
- verhoogde afbraak van rode bloedcellen
- abnormale membranen van rode bloedcellen, die verhoogde fragiliteit van de osmose
- verhoogd bloedverlies door occulte gastro-intestinale bloedingen en bloedmonsters en tijdens hemodialyse
- ACE-remming veroorzaken.Erytropoëtine is een glycoproteïne hormoon dat de productie van rode bloedcellen stimuleert door binding aan erytropoëtinereceptoren, gevestigd op vroege erytroïde voorlopercellen in het beenmerg.
de binding van erythropoëtine aan deze voorlopercellen bespaart hen apoptose en maakt daardoor celdeling en rijping tot rode bloedcellen mogelijk. Bij CKD kunnen de erythropoëtinespiegels normaal zijn, maar onvoldoende voor de graad van anemie. De mechanismen die de productie van erythropoëtine in zieke nieren belemmeren, blijven slecht begrepen. Remming van erytropoëse door uremische remmers is ook mogelijk en kan in belangrijke mate bijdragen tot de anemie van CKD; dergelijke factoren zijn niet geïdentificeerd. Dialyse kan de renale anemie en de werkzaamheid van erytropoëtine-stimulerende middelen verbeteren. Patiënten met een nieraandoening kunnen chronische infecties en andere chronische ziekten ontwikkelen. Chronische ziekte draagt in dergelijke gevallen bij aan anemie. Anemie bij chronische aandoeningen wordt gemedieerd door ontstekingscytokines door remming van de productie en werkzaamheid van erythropoëtine en een verminderde ijzerbeschikbaarheid.
Hepcidin is de belangrijkste mediator van ijzermetabolisme. In inflammatoire toestanden blokkeert hepcidin de ijzerabsorptie in de darm en bevordert het de ijzervastlegging in macrofagen.
andere oorzaken
anemie geassocieerd met CKD is hoogstwaarschijnlijk renale anemie; echter, het verschil voor andere ziekten moet worden beschouwd als waar voor de stadia 1 – 3 CKD.
de evaluatie van anemie bij patiënten met CKD dient een complete bloedtelling met indices van rode bloedcellen te omvatten (gemiddelde corpusculaire hemoglobineconcentratie, gemiddeld corpusculair volume). Renale anemie is gewoonlijk normochromisch en normocytisch. Vitamine B12 – en folaatdeficiëntie kan leiden tot macrocytose, terwijl ijzertekort of erfelijke aandoeningen van hemoglobine microcytose kunnen veroorzaken. Er dienen ijzerstudies te worden uitgevoerd om de ijzerspiegel in weefselopslagplaatsen of de toereikendheid van de ijzervoorraad voor erytropoëse te beoordelen.Anemie kan wijzen op de aanwezigheid van ondervoeding of systemische ziekte. Het is een onafhankelijke risicofactor voor ziekenhuisopname, CVD en mortaliteit. ACE-remmers kunnen anemie verergeren.
behandeling van anemie beschermt het hart
anemie verergert hartfalen. Behandeling van anemie is gunstig voor de levensverwachting en kan ook de prognose van CVD verbeteren. De kwaliteit van leven is verbeterd bij personen met een hemoglobinegehalte binnen het streefbereik.
streefwaarde hemoglobine
de Kidney Disease Improving Global Outcome (Kdigo) richtlijnen stellen dat het hemoglobinegehalte moet variëren van 10,0 g/dL tot 12 g/dL bij CKD patiënten die dialyse ondergaan. Predialyseniveaus dienen 10 g/dL te zijn.
rolverdeling tussen nefrologen en eerstelijnsartsen
vroegtijdige verwijzing naar een nefroloog is raadzaam. Zodra de behandelingsstrategie is vastgesteld, gaan nefrologen en eerstelijnsartsen samen verder met het management.
evaluatie van ijzertekort
evaluatie van het ijzertekort en de juiste ijzervoorraad is belangrijk bij de behandeling van anemie. Anemie kan verbeteren met de toediening van ijzersupplementen, zelfs wanneer de patiënt niet schijnbaar ijzertekort heeft, omdat het gebruik van recombinant erytropoëtine een relatieve ijzertekort kan veroorzaken.
de KDOQI-richtlijnen voor recombinant humaan erytropoëtine bij CKD zijn::
- serumferritine >100 ng / mL vóór dialyse
- serumferritine >200 ng / mL bij dialysepatiënten
- transferrinesaturatie > 20%.
ijzer kan intraveneus of oraal worden toegediend. Intraveneus ijzer is werkzamer, vooral bij dialysepatiënten en patiënten die met erytropoëtine worden behandeld.
gebruik van exogene erythropoëtines
er is momenteel een aantal erytropoëtine-stimulerende middelen beschikbaar, waaronder oudere, korter werkende en nieuwe, langer werkende middelen. Het juiste middel en de juiste dosis zijn afhankelijk van een aantal factoren, waaronder kosten, werkzaamheid en gemak. Aangezien deze geneesmiddelen duur zijn en bijwerkingen hebben, wordt hun beheer het best overgelaten aan een nefroloog.
bot-en mineraalaandoeningen
hyperfosfatemie is de belangrijkste afwijking die een cascade van metabole voorvallen veroorzaakt, resulterend in botmineraaldichtheid van CKD.
fosfaat wordt behouden naarmate de nierfunctie verslechtert – ongeveer hetzelfde als creatinine wordt behouden. Deze retentie wordt duidelijk als stadium 3b CKD wordt bereikt. Het zal steeds erger worden naarmate het eindstadium nadert en moet worden verlaagd tot binnen de normale grenzen.
een fosfaatrijk dieet stimuleert osteocyten tot de aanmaak van fibroblastgroeifactor 23, die op zijn beurt de hydroxylering van vitamine D tot actieve vitamine D3 van 1,25 remt. Zonder vitamine D3 neemt de calciumabsorptie en botremodellering af. De resulterende hypocalciëmie is een belangrijke stimulans voor de afgifte van parathyroïdhormoon (PTH), met als gevolg de ontwikkeling van nierbotziekte. Alkalische fosfatase in Serum is een marker van verhoogde botomzetting. Daarom vertonen hoge bloedspiegels PTH-activiteit.Zowel hyperfosfatemie als vitamine D3-deficiëntie resulteren in een verhoogde PTH-secretie.
aanvankelijk kan de stimulus voor PTH-secretie onder controle worden gehouden door het serumcalcium te verhogen, de fosfaatspiegels in het bloed te verlagen en vitamine D3 voor te schrijven. Dit is het secundaire stadium van hyperparathyreoïdie (Tabel 2). Met de tijd en ongecontroleerde, langdurige stimulatie van PTH-secretie worden de bijschildklierhormonen echter autonoom en wordt het stadium van autonome hyperparathyreoïdie bereikt (Tabel 3). Parathyroïdectomie kan nu nodig zijn of dure calcimimetic drugs moeten worden toegediend om te proberen om de wanordelijke metabolische omgeving te herstellen.


er is onzekerheid over de interpretatie van vitamine D3-niveaumetingen. Als ze moeten worden gemeten, dan worden 25-OH-vitamine D3 spiegels aanbevolen voor de beoordeling.
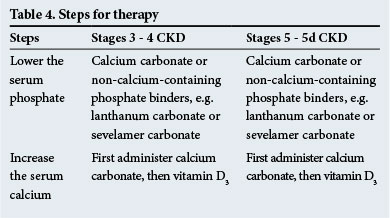
therapie
de stappen voor therapie zijn weergegeven in Tabel 4. Niet-calciumbevattende fosfaatbinders worden aanbevolen wanneer er sprake is van significante gemetastaseerde calcificatie en/of wanneer hypercalciëmie aanwezig is.
Calcimimetica, die de bijschildklieren sensibiliseren voor serumcalcium, zijn nuttig voor te schrijven bij hyperparathyreoïdie wanneer de serum PTH – spiegels hoog zijn (2 – 9 keer boven het normale bereik-controleer met het laboratorium voor normale waarden). Zij hebben een rol te spelen in het verminderen van PTH niveaus in om het even welke klinische situaties die in CKD voorkomen.
Follow-up bloedmetingen
deze worden gegeven in Tabel 5.
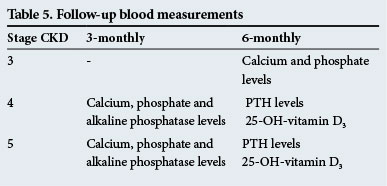
deze follow-up tijden zijn alleen richtlijnen en de tests moeten vaker worden uitgevoerd als er significante afwijkingen.
speciale punten om op te merken
- hebben betrekking op een nefroloog vroeg in de kuur van CKD.
- vermijd over-suppressie van de bijschildklieren, aangezien dit zal leiden tot dynamische botziekte.
- het exacte PTH-niveau waarop secundaire en autonome hyperparathyreoïdie wordt gediagnosticeerd is onzeker, vanwege verschillende tests. De biochemie, zoals hierboven beschreven (samen met röntgenfoto ‘ s van botten), moet dan worden gebruikt om te helpen bij de diagnose.
- zich bewust zijn van de ontwikkeling van de alkalische fosfatasespiegels in serum; het gehalte kan binnen het normale bereik liggen, maar kan ten opzichte van de vorige meting verdubbeld zijn.
- osteoporose gaat gepaard met botziekte die optreedt bij CKD. Bisfosfonaten mogen niet worden gebruikt bij patiënten met de fase 3 – 5 CKD.